+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 3zvq | ||||||
|---|---|---|---|---|---|---|---|
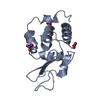
| タイトル | Crystal Structure of proteolyzed lysozyme | ||||||
 要素 要素 | (LYSOZYME C) x 2 | ||||||
 キーワード キーワード |  HYDROLASE (加水分解酵素) / HYDROLASE (加水分解酵素) /  PROTEOLYSIS (タンパク質分解) / PROTEOLYSIS (タンパク質分解) /  PMSF (フッ化フェニルメチルスルホニル) / PMSF (フッ化フェニルメチルスルホニル) /  SUBTILISIN (サブチリシン) SUBTILISIN (サブチリシン) | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 抗微生物ペプチド / Neutrophil degranulation / 抗微生物ペプチド / Neutrophil degranulation /  beta-N-acetylglucosaminidase activity / cell wall macromolecule catabolic process / beta-N-acetylglucosaminidase activity / cell wall macromolecule catabolic process /  リゾチーム / リゾチーム /  lysozyme activity / killing of cells of another organism / defense response to Gram-negative bacterium / defense response to Gram-positive bacterium / defense response to bacterium ... lysozyme activity / killing of cells of another organism / defense response to Gram-negative bacterium / defense response to Gram-positive bacterium / defense response to bacterium ... 抗微生物ペプチド / Neutrophil degranulation / 抗微生物ペプチド / Neutrophil degranulation /  beta-N-acetylglucosaminidase activity / cell wall macromolecule catabolic process / beta-N-acetylglucosaminidase activity / cell wall macromolecule catabolic process /  リゾチーム / リゾチーム /  lysozyme activity / killing of cells of another organism / defense response to Gram-negative bacterium / defense response to Gram-positive bacterium / defense response to bacterium / lysozyme activity / killing of cells of another organism / defense response to Gram-negative bacterium / defense response to Gram-positive bacterium / defense response to bacterium /  小胞体 / 小胞体 /  extracellular space / identical protein binding / extracellular space / identical protein binding /  細胞質 細胞質類似検索 - 分子機能 | ||||||
| 生物種 |   GALLUS GALLUS (ニワトリ) GALLUS GALLUS (ニワトリ) | ||||||
| 手法 |  X線回折 / X線回折 /  分子置換 / 解像度: 2 Å 分子置換 / 解像度: 2 Å | ||||||
 データ登録者 データ登録者 | Kishan, K.V. / Sharma, A. | ||||||
 引用 引用 |  ジャーナル: Protein Pept.Lett. / 年: 2010 ジャーナル: Protein Pept.Lett. / 年: 2010タイトル: Salt-assisted religation of proteolyzed Glutathione-S-transferase follows Hofmeister series. 著者: Kishan, K.V. / Sharma, A. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  3zvq.cif.gz 3zvq.cif.gz | 43.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb3zvq.ent.gz pdb3zvq.ent.gz | 31.2 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  3zvq.json.gz 3zvq.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/zv/3zvq https://data.pdbj.org/pub/pdb/validation_reports/zv/3zvq ftp://data.pdbj.org/pub/pdb/validation_reports/zv/3zvq ftp://data.pdbj.org/pub/pdb/validation_reports/zv/3zvq | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  193lS S: 精密化の開始モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 7958.802 Da / 分子数: 1 / 断片: RESIDUES 19-88 / 由来タイプ: 天然 / 由来: (天然)   GALLUS GALLUS (ニワトリ) / 参照: UniProt: P00698, GALLUS GALLUS (ニワトリ) / 参照: UniProt: P00698,  リゾチーム リゾチーム |
|---|---|
| #2: タンパク質 | 分子量: 6333.320 Da / 分子数: 1 / 断片: RESIDUES 90-147 / 由来タイプ: 天然 / 由来: (天然)   GALLUS GALLUS (ニワトリ) / 参照: UniProt: P00698, GALLUS GALLUS (ニワトリ) / 参照: UniProt: P00698,  リゾチーム リゾチーム |
| #3: 水 | ChemComp-HOH /  水 水 |
| 配列の詳細 | THE SEQUENCE DIFFERS FROM THE ONE IN THE UNIPROT DATABASE DUE TO EXCLUSION OF THE N-TERMINAL SIGNAL PEPTIDE |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.11 Å3/Da / 溶媒含有率: 41.62 % / 解説: NONE |
|---|---|
結晶化 | 温度: 298 K / 詳細: 20MG/ML PROTEOLYZED LYSOZYME, 15%PEG3500, 25C |
-データ収集
| 回折 | 平均測定温度: 298 K |
|---|---|
| 放射光源 | 由来:  回転陽極 / 波長: 1.54 回転陽極 / 波長: 1.54 |
| 検出器 | タイプ: MARRESEARCH / 検出器: IMAGE PLATE / 詳細: OSMIC MIRRORS |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長 : 1.54 Å / 相対比: 1 : 1.54 Å / 相対比: 1 |
| 反射 | 解像度: 2→24.84 Å / Num. obs: 7699 / % possible obs: 93.9 % / Observed criterion σ(I): 2 / 冗長度: 4.5 % / Biso Wilson estimate: 20 Å2 / Rmerge(I) obs: 0.1 |
| 反射 シェル | 最高解像度: 2 Å / 冗長度: 4.2 % / Rmerge(I) obs: 0.38 / % possible all: 90.4 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  分子置換 分子置換開始モデル: PDB ENTRY 193L 解像度: 2→24.84 Å / Isotropic thermal model: RESTRAINED / 交差検証法: RANDOM / σ(F): 0 / 立体化学のターゲット値: ENGH & HUBER
| ||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 溶媒モデル: FLAT MODEL / Bsol: 64.83 Å2 / ksol: 0.45 e/Å3 | ||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 20.27 Å2
| ||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2→24.84 Å
| ||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||
| Xplor file |
|
 ムービー
ムービー コントローラー
コントローラー










































































































































































































































































 PDBj
PDBj





