+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2y83 | ||||||
|---|---|---|---|---|---|---|---|
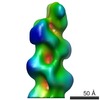
| タイトル | Actin filament pointed end | ||||||
 要素 要素 | ACTIN, ALPHA SKELETAL MUSCLE | ||||||
 キーワード キーワード | CONTRACTILE PROTEIN / CYTOSKELETON / CELL MOTILITY | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cytoskeletal motor activator activity / tropomyosin binding / myosin heavy chain binding / mesenchyme migration / troponin I binding / filamentous actin / actin filament bundle / skeletal muscle thin filament assembly / actin filament bundle assembly / striated muscle thin filament ...cytoskeletal motor activator activity / tropomyosin binding / myosin heavy chain binding / mesenchyme migration / troponin I binding / filamentous actin / actin filament bundle / skeletal muscle thin filament assembly / actin filament bundle assembly / striated muscle thin filament / skeletal muscle myofibril / actin monomer binding / skeletal muscle fiber development / stress fiber / titin binding / actin filament polymerization / filopodium / actin filament / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / calcium-dependent protein binding / lamellipodium / cell body / hydrolase activity / protein domain specific binding / calcium ion binding / positive regulation of gene expression / magnesium ion binding / ATP binding / identical protein binding / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 22.9 Å | ||||||
 データ登録者 データ登録者 | Narita, A. / Oda, T. / Maeda, Y. | ||||||
 引用 引用 |  ジャーナル: EMBO J / 年: 2011 ジャーナル: EMBO J / 年: 2011タイトル: Structural basis for the slow dynamics of the actin filament pointed end. 著者: Akihiro Narita / Toshiro Oda / Yuichiro Maéda /  要旨: The actin filament has clear polarity where one end, the pointed end, has a much slower polymerization and depolymerization rate than the other end, the barbed end. This intrinsic difference of the ...The actin filament has clear polarity where one end, the pointed end, has a much slower polymerization and depolymerization rate than the other end, the barbed end. This intrinsic difference of the ends significantly affects all actin dynamics in the cell, which has central roles in a wide spectrum of cellular functions. The detailed mechanism underlying this difference has remained elusive, because high-resolution structures of the filament ends have not been available. Here, we present the structure of the actin filament pointed end obtained using a single particle analysis of cryo-electron micrographs. We determined that the terminal pointed end subunit is tilted towards the penultimate subunit, allowing specific and extra loop-to-loop inter-strand contacts between the two end subunits, which is not possible in other parts of the filament. These specific contacts prevent the end subunit from dissociating. For elongation, the loop-to-loop contacts also inhibit the incorporation of another actin monomer at the pointed end. These observations are likely to account for the less dynamic pointed end. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2y83.cif.gz 2y83.cif.gz | 685.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2y83.ent.gz pdb2y83.ent.gz | 566.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2y83.json.gz 2y83.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  2y83_validation.pdf.gz 2y83_validation.pdf.gz | 1 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  2y83_full_validation.pdf.gz 2y83_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  2y83_validation.xml.gz 2y83_validation.xml.gz | 59.4 KB | 表示 | |
| CIF形式データ |  2y83_validation.cif.gz 2y83_validation.cif.gz | 90.7 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/y8/2y83 https://data.pdbj.org/pub/pdb/validation_reports/y8/2y83 ftp://data.pdbj.org/pub/pdb/validation_reports/y8/2y83 ftp://data.pdbj.org/pub/pdb/validation_reports/y8/2y83 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 41862.613 Da / 分子数: 6 / 由来タイプ: 天然 / 由来: (天然)  #2: 化合物 | ChemComp-ADP / #3: 化合物 | ChemComp-CA / |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: FILAMENT / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: RABBIT SKELETAL ACTIN / タイプ: COMPLEX |
|---|---|
| 緩衝液 | 名称: 50 MM NACL, 10 MM SODIUM PHOSPHATE BUFFER PH 7.4 3 MM MGCL2, 0.005% (W/V) NAN3, 0.7 MM DTT. pH: 7.4 詳細: 50 MM NACL, 10 MM SODIUM PHOSPHATE BUFFER PH 7.4 3 MM MGCL2, 0.005% (W/V) NAN3, 0.7 MM DTT. |
| 試料 | 濃度: 0.05 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | 詳細: HOLEY CARBON |
| 急速凍結 | 凍結剤: ETHANE 詳細: VITRIFICATION 1 - CRYOGEN- ETHANE, HUMIDITY- 90%, TEMPERATURE- 4 DEGREES CELSIUS. METHOD- BLOT FOR 3 SECONDS BEFORE PLUNGING. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 顕微鏡 | モデル: JEOL 3200FSC |
|---|---|
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 40000 X / 最大 デフォーカス(公称値): 8000 nm / 最小 デフォーカス(公称値): 5000 nm |
| 試料ホルダ | 温度: 4 K |
| 撮影 | 電子線照射量: 34 e/Å2 / フィルム・検出器のモデル: KODAK SO-163 FILM |
| 画像スキャン | デジタル画像の数: 142 |
- 解析
解析
| EMソフトウェア | 名称: EOS / カテゴリ: 3次元再構成 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | 詳細: PHASE AND AMPLITUDE | ||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||
| 3次元再構成 | 手法: SINGLE PARTICLE ANALYSIS / 解像度: 22.9 Å / 粒子像の数: 714 / ピクセルサイズ(公称値): 3.4125 Å / ピクセルサイズ(実測値): 3.4125 Å 詳細: SUBMISSION BASED ON EXPERIMENTAL DATA FROM EMDB EMD-1872. 対称性のタイプ: POINT | ||||||||||||
| 原子モデル構築 | プロトコル: FLEXIBLE FIT / 空間: REAL 詳細: METHOD--RIGID BODY AND MOLECULAR DYNAMICS REFINEMENT PROTOCOL--EM | ||||||||||||
| 原子モデル構築 | PDB-ID: 2ZWH Accession code: 2ZWH / Source name: PDB / タイプ: experimental model | ||||||||||||
| 精密化 | 最高解像度: 22.9 Å | ||||||||||||
| 精密化ステップ | サイクル: LAST / 最高解像度: 22.9 Å
|
 ムービー
ムービー コントローラー
コントローラー




































































 PDBj
PDBj







