+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-10205 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Molecular structure of mouse apoferritin resolved at 2.7 Angstroms with the Glacios cryo-microscope | |||||||||
 マップデータ マップデータ | Post-processed map of apoferritin at 200 kV resolved with the FEI Glacios microscope at 2.7 A | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Apoferritin / iron binding / iron storing / complex / METAL BINDING PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Iron uptake and transport / Golgi Associated Vesicle Biogenesis / iron ion sequestering activity / negative regulation of ferroptosis / ferroxidase / autolysosome / intracellular sequestering of iron ion / ferroxidase activity / negative regulation of fibroblast proliferation / endocytic vesicle lumen ...Iron uptake and transport / Golgi Associated Vesicle Biogenesis / iron ion sequestering activity / negative regulation of ferroptosis / ferroxidase / autolysosome / intracellular sequestering of iron ion / ferroxidase activity / negative regulation of fibroblast proliferation / endocytic vesicle lumen / autophagosome / Neutrophil degranulation / ferric iron binding / ferrous iron binding / iron ion transport / immune response / iron ion binding / negative regulation of cell population proliferation / mitochondrion / extracellular region / identical protein binding / membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.73 Å | |||||||||
 データ登録者 データ登録者 | Hamdi F / Tueting C | |||||||||
 引用 引用 |  ジャーナル: PLoS One / 年: 2020 ジャーナル: PLoS One / 年: 2020タイトル: 2.7 Å cryo-EM structure of vitrified M. musculus H-chain apoferritin from a compact 200 keV cryo-microscope. 著者: Farzad Hamdi / Christian Tüting / Dmitry A Semchonok / Koen M Visscher / Fotis L Kyrilis / Annette Meister / Ioannis Skalidis / Lisa Schmidt / Christoph Parthier / Milton T Stubbs / Panagiotis L Kastritis /   要旨: Here we present the structure of mouse H-chain apoferritin at 2.7 Å (FSC = 0.143) solved by single particle cryogenic electron microscopy (cryo-EM) using a 200 kV device, the Thermo Fisher Glacios®. ...Here we present the structure of mouse H-chain apoferritin at 2.7 Å (FSC = 0.143) solved by single particle cryogenic electron microscopy (cryo-EM) using a 200 kV device, the Thermo Fisher Glacios®. This is a compact, two-lens illumination system with a constant power objective lens, without any energy filters or aberration correctors, often thought of as a "screening cryo-microscope". Coulomb potential maps reveal clear densities for main chain carbonyl oxygens, residue side chains (including alternative conformations) and bound solvent molecules. We used a quasi-crystallographic reciprocal space approach to fit model coordinates to the experimental cryo-EM map. We argue that the advantages offered by (a) the high electronic and mechanical stability of the microscope, (b) the high emission stability and low beam energy spread of the high brightness Field Emission Gun (X-FEG), (c) direct electron detection technology and (d) particle-based Contrast Transfer Function (CTF) refinement have contributed to achieving high resolution. Overall, we show that basic electron optical settings for automated cryo-electron microscopy imaging can be used to determine structures approaching atomic resolution. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_10205.map.gz emd_10205.map.gz | 8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-10205-v30.xml emd-10205-v30.xml emd-10205.xml emd-10205.xml | 25.8 KB 25.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_10205_fsc.xml emd_10205_fsc.xml | 9.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_10205.png emd_10205.png | 103.4 KB | ||
| マスクデータ |  emd_10205_msk_1.map emd_10205_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-10205.cif.gz emd-10205.cif.gz | 6.2 KB | ||
| その他 |  emd_10205_additional.map.gz emd_10205_additional.map.gz emd_10205_half_map_1.map.gz emd_10205_half_map_1.map.gz emd_10205_half_map_2.map.gz emd_10205_half_map_2.map.gz | 59.8 MB 45.9 MB 45.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-10205 http://ftp.pdbj.org/pub/emdb/structures/EMD-10205 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10205 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10205 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_10205_validation.pdf.gz emd_10205_validation.pdf.gz | 582.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_10205_full_validation.pdf.gz emd_10205_full_validation.pdf.gz | 582.5 KB | 表示 | |
| XML形式データ |  emd_10205_validation.xml.gz emd_10205_validation.xml.gz | 16.2 KB | 表示 | |
| CIF形式データ |  emd_10205_validation.cif.gz emd_10205_validation.cif.gz | 21.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10205 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10205 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10205 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10205 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_10205.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_10205.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Post-processed map of apoferritin at 200 kV resolved with the FEI Glacios microscope at 2.7 A | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.96 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
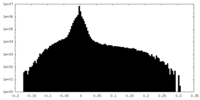
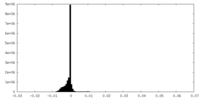
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_10205_msk_1.map emd_10205_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: Post-processed (unmasked) map of apoferritin at 200 kV...
| ファイル | emd_10205_additional.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Post-processed (unmasked) map of apoferritin at 200 kV resolved with the FEI Glacios microscope at 2.7 A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Refined half-map of apoferritin at 200 kV resolved...
| ファイル | emd_10205_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Refined half-map of apoferritin at 200 kV resolved with the FEI Glacios microscope | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Refined half-map of apoferritin at 200 kV resolved...
| ファイル | emd_10205_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Refined half-map of apoferritin at 200 kV resolved with the FEI Glacios microscope | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Mouse apoferritin
| 全体 | 名称: Mouse apoferritin |
|---|---|
| 要素 |
|
-超分子 #1: Mouse apoferritin
| 超分子 | 名称: Mouse apoferritin / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 480 KDa |
-分子 #1: Ferritin heavy chain
| 分子 | 名称: Ferritin heavy chain / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: ferroxidase |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 21.097631 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTTASPSQVR QNYHQDAEAA INRQINLELY ASYVYLSMSC YFDRDDVALK NFAKYFLHQS HEEREHAEKL MKLQNQRGGR IFLQDIKKP DRDDWESGLN AMECALHLEK SVNQSLLELH KLATDKNDPH LCDFIETYYL SEQVKSIKEL GDHVTNLRKM G APEAGMAE YLFDKHTLGH GDES UniProtKB: Ferritin heavy chain |
-分子 #2: FE (III) ION
| 分子 | 名称: FE (III) ION / タイプ: ligand / ID: 2 / コピー数: 1 / 式: FE |
|---|---|
| 分子量 | 理論値: 55.845 Da |
-分子 #3: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 3 / コピー数: 1 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #4: water
| 分子 | 名称: water / タイプ: ligand / ID: 4 / コピー数: 72 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 4.0 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 45 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 詳細 | microscope model is Thermofisher Glacios 200 kV |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 300 / 平均露光時間: 30.0 sec. / 平均電子線量: 28.0 e/Å2 / 詳細: pixel size was 0.96 Angstroms |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 最大 デフォーカス(補正後): 1.6 µm / 最小 デフォーカス(補正後): 0.8 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.6 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


















































 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)