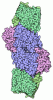
登録情報 データベース : PDB / ID : 7jl0タイトル Cryo-EM structure of MDA5-dsRNA in complex with TRIM65 PSpry domain (Monomer) Interferon-induced helicase C domain-containing protein 1 RNA (5'-R(P*GP*AP*CP*UP*GP*AP*CP*UP*GP*AP*CP*UP*GP*A)-3')RNA (5'-R(P*UP*CP*AP*GP*UP*CP*AP*GP*UP*CP*AP*GP*UP*C)-3')Tripartite motif-containing protein 65 キーワード / / / / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト)手法 / / / 解像度 : 4.3 Å データ登録者 Kato, K. / Ahmad, S. / Hur, S. 資金援助 組織 認可番号 国 National Institutes of Health/National Institute Of Allergy and Infectious Diseases (NIH/NIAID)
ジャーナル : Mol Cell / 年 : 2021タイトル : Structural analysis of RIG-I-like receptors reveals ancient rules of engagement between diverse RNA helicases and TRIM ubiquitin ligases.著者 : Kazuki Kato / Sadeem Ahmad / Zixiang Zhu / Janet M Young / Xin Mu / Sehoon Park / Harmit S Malik / Sun Hur / 要旨 : RNA helicases and E3 ubiquitin ligases mediate many critical functions in cells, but their actions have largely been studied in distinct biological contexts. Here, we uncover evolutionarily conserved ... RNA helicases and E3 ubiquitin ligases mediate many critical functions in cells, but their actions have largely been studied in distinct biological contexts. Here, we uncover evolutionarily conserved rules of engagement between RNA helicases and tripartite motif (TRIM) E3 ligases that lead to their functional coordination in vertebrate innate immunity. Using cryoelectron microscopy and biochemistry, we show that RIG-I-like receptors (RLRs), viral RNA receptors with helicase domains, interact with their cognate TRIM/TRIM-like E3 ligases through similar epitopes in the helicase domains. Their interactions are avidity driven, restricting the actions of TRIM/TRIM-like proteins and consequent immune activation to RLR multimers. Mass spectrometry and phylogeny-guided biochemical analyses further reveal that similar rules of engagement may apply to diverse RNA helicases and TRIM/TRIM-like proteins. Our analyses suggest not only conserved substrates for TRIM proteins but also, unexpectedly, deep evolutionary connections between TRIM proteins and RNA helicases, linking ubiquitin and RNA biology throughout animal evolution. 履歴 登録 2020年7月29日 登録サイト / 処理サイト 改定 1.0 2020年12月9日 Provider / タイプ 改定 1.1 2021年1月20日 Group / カテゴリ Item / _citation.pdbx_database_id_PubMed / _citation.title改定 1.2 2021年2月17日 Group / カテゴリ Item _citation.journal_volume / _citation.page_first ... _citation.journal_volume / _citation.page_first / _citation.page_last / _citation.year 改定 1.3 2024年3月6日 Group / Database references / カテゴリ / chem_comp_bond / database_2Item / _database_2.pdbx_database_accession
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) データ登録者
データ登録者 米国, 1件
米国, 1件  引用
引用 ジャーナル: Mol Cell / 年: 2021
ジャーナル: Mol Cell / 年: 2021

 構造の表示
構造の表示 ムービービューア
ムービービューア Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 7jl0.cif.gz
7jl0.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb7jl0.ent.gz
pdb7jl0.ent.gz PDB形式
PDB形式 7jl0.json.gz
7jl0.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 7jl0_validation.pdf.gz
7jl0_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 7jl0_full_validation.pdf.gz
7jl0_full_validation.pdf.gz 7jl0_validation.xml.gz
7jl0_validation.xml.gz 7jl0_validation.cif.gz
7jl0_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/jl/7jl0
https://data.pdbj.org/pub/pdb/validation_reports/jl/7jl0 ftp://data.pdbj.org/pub/pdb/validation_reports/jl/7jl0
ftp://data.pdbj.org/pub/pdb/validation_reports/jl/7jl0 リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト)
Homo sapiens (ヒト) Homo sapiens (ヒト)
Homo sapiens (ヒト) Homo sapiens (ヒト) / 遺伝子: IFIH1, MDA5, RH116 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: IFIH1, MDA5, RH116 / 発現宿主: 
 Homo sapiens (ヒト) / 遺伝子: TRIM65 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: TRIM65 / 発現宿主: 





 試料調製
試料調製 Homo sapiens (ヒト)
Homo sapiens (ヒト)
 電子顕微鏡撮影
電子顕微鏡撮影
 FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM
FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM 解析
解析 ムービー
ムービー コントローラー
コントローラー





















 PDBj
PDBj