+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-20390 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Activated Class III PI-3 Kinase by NRBF2 | |||||||||
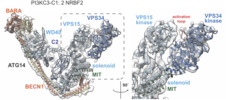
 マップデータ マップデータ | Full length NRBF2 pushes PI3KC3-C1 to an activate conformation in which peripheral membrane binding protein VPS34 is posed to phosphorylate substrate phosphatidylinositol. | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
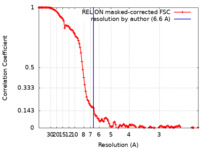
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.6 Å | |||||||||
 データ登録者 データ登録者 | Young LN / Goerdeler F / Hurley JH | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2019 ジャーナル: Proc Natl Acad Sci U S A / 年: 2019タイトル: Structural pathway for allosteric activation of the autophagic PI 3-kinase complex I. 著者: Lindsey N Young / Felix Goerdeler / James H Hurley /  要旨: Autophagy induction by starvation and stress involves the enzymatic activation of the class III phosphatidylinositol (PI) 3-kinase complex I (PI3KC3-C1). The inactive basal state of PI3KC3-C1 is ...Autophagy induction by starvation and stress involves the enzymatic activation of the class III phosphatidylinositol (PI) 3-kinase complex I (PI3KC3-C1). The inactive basal state of PI3KC3-C1 is maintained by inhibitory contacts between the VPS15 protein kinase and VPS34 lipid kinase domains that restrict the conformation of the VPS34 activation loop. Here, the proautophagic MIT domain-containing protein NRBF2 was used to map the structural changes leading to activation. Cryoelectron microscopy was used to visualize a 2-step PI3KC3-C1 activation pathway driven by NRFB2 MIT domain binding. Binding of a single NRBF2 MIT domain bends the helical solenoid of the VPS15 scaffold, displaces the protein kinase domain of VPS15, and releases the VPS34 kinase domain from the inhibited conformation. Binding of a second MIT stabilizes the VPS34 lipid kinase domain in an active conformation that has an unrestricted activation loop and is poised for access to membranes. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_20390.map.gz emd_20390.map.gz | 12.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-20390-v30.xml emd-20390-v30.xml emd-20390.xml emd-20390.xml | 13.2 KB 13.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_20390_fsc.xml emd_20390_fsc.xml | 12.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_20390.png emd_20390.png | 414.4 KB | ||
| マスクデータ |  emd_20390_msk_1.map emd_20390_msk_1.map | 166.4 MB |  マスクマップ マスクマップ | |
| その他 |  emd_20390_additional.map.gz emd_20390_additional.map.gz emd_20390_additional_1.map.gz emd_20390_additional_1.map.gz | 155.6 MB 155.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-20390 http://ftp.pdbj.org/pub/emdb/structures/EMD-20390 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-20390 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-20390 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_20390_validation.pdf.gz emd_20390_validation.pdf.gz | 78.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_20390_full_validation.pdf.gz emd_20390_full_validation.pdf.gz | 77.2 KB | 表示 | |
| XML形式データ |  emd_20390_validation.xml.gz emd_20390_validation.xml.gz | 494 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20390 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20390 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20390 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20390 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_20390.map.gz / 形式: CCP4 / 大きさ: 166.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_20390.map.gz / 形式: CCP4 / 大きさ: 166.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Full length NRBF2 pushes PI3KC3-C1 to an activate conformation in which peripheral membrane binding protein VPS34 is posed to phosphorylate substrate phosphatidylinositol. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.137 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_20390_msk_1.map emd_20390_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
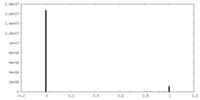
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: Unsharpened map.
| ファイル | emd_20390_additional.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened map. | ||||||||||||
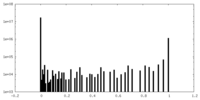
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: Unsharpened map.
| ファイル | emd_20390_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened map. | ||||||||||||
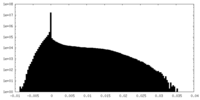
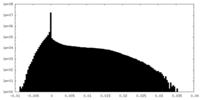
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Class III PI 3-Kinase Complex 1 containing NRBF2-MIT-linker-BECN1...
| 全体 | 名称: Class III PI 3-Kinase Complex 1 containing NRBF2-MIT-linker-BECN1, ATG14, VPS34, VPS15 |
|---|---|
| 要素 |
|
-超分子 #1: Class III PI 3-Kinase Complex 1 containing NRBF2-MIT-linker-BECN1...
| 超分子 | 名称: Class III PI 3-Kinase Complex 1 containing NRBF2-MIT-linker-BECN1, ATG14, VPS34, VPS15 タイプ: complex / ID: 1 / 親要素: 0 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  Homo sapiens (ヒト) / 組換株: HEK 293 GNTI / 組換細胞: Kidney cells / 組換プラスミド: pCAG vectors Homo sapiens (ヒト) / 組換株: HEK 293 GNTI / 組換細胞: Kidney cells / 組換プラスミド: pCAG vectors |
| 分子量 | 理論値: 400 KDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.2 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 88 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均露光時間: 6.4 sec. / 平均電子線量: 0.98 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)