+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8gfv | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
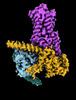
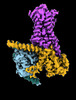
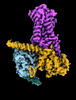
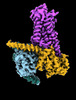
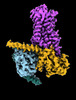
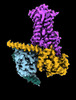
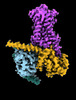
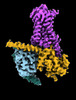
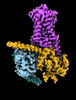
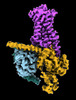
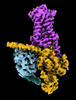
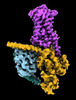
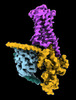
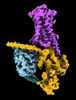
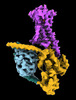
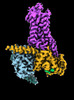
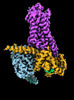
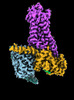
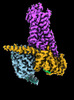
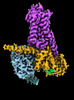
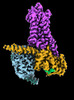
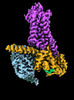
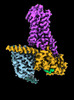
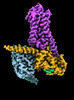
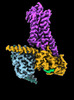
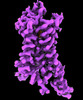
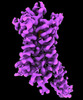
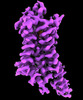
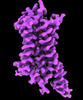
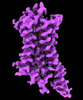
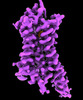
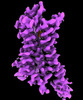
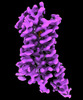
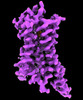
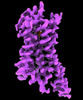
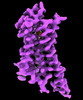
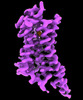
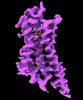
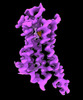
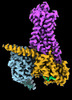
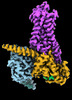
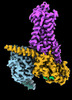
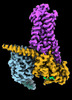
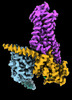
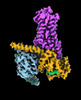
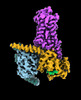
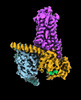
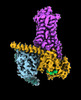
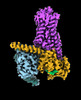
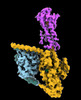
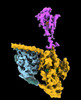
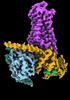
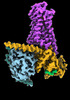
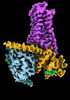
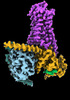
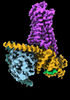
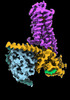
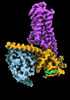
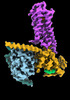
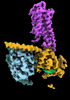
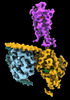
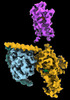
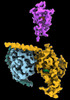
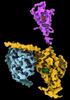
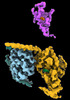
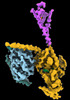
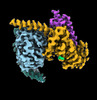
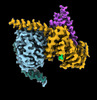
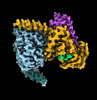
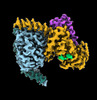
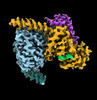
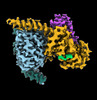
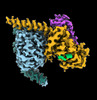
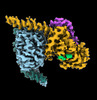
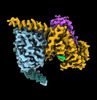
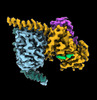
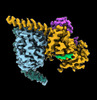
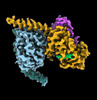
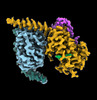
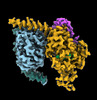
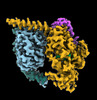
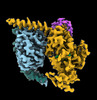
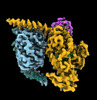
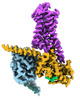
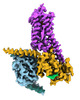
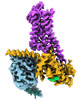
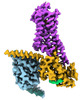
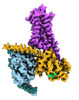
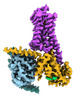
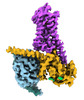
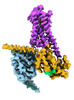
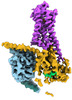
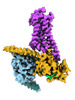
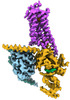
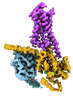
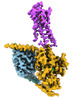
| タイトル | CryoEM structure of beta-2-adrenergic receptor in complex with GTP-bound Gs heterotrimer (transition intermediate #1 of 20) | |||||||||
 要素 要素 |
| |||||||||
 キーワード キーワード |  SIGNALING PROTEIN / SIGNALING PROTEIN /  GPCR (Gタンパク質共役受容体) / GPCR (Gタンパク質共役受容体) /  Adrenergic / Receptor / Adrenergic / Receptor /  G protein (Gタンパク質) G protein (Gタンパク質) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報desensitization of G protein-coupled receptor signaling pathway by arrestin / beta2-adrenergic receptor activity / norepinephrine-epinephrine-mediated vasodilation involved in regulation of systemic arterial blood pressure / positive regulation of mini excitatory postsynaptic potential / positive regulation of cAMP-dependent protein kinase activity /  norepinephrine binding / norepinephrine binding /  アドレナリン受容体 / アドレナリン受容体 /  熱力学 / positive regulation of autophagosome maturation / positive regulation of AMPA receptor activity ...desensitization of G protein-coupled receptor signaling pathway by arrestin / beta2-adrenergic receptor activity / norepinephrine-epinephrine-mediated vasodilation involved in regulation of systemic arterial blood pressure / positive regulation of mini excitatory postsynaptic potential / positive regulation of cAMP-dependent protein kinase activity / 熱力学 / positive regulation of autophagosome maturation / positive regulation of AMPA receptor activity ...desensitization of G protein-coupled receptor signaling pathway by arrestin / beta2-adrenergic receptor activity / norepinephrine-epinephrine-mediated vasodilation involved in regulation of systemic arterial blood pressure / positive regulation of mini excitatory postsynaptic potential / positive regulation of cAMP-dependent protein kinase activity /  norepinephrine binding / norepinephrine binding /  アドレナリン受容体 / アドレナリン受容体 /  熱力学 / positive regulation of autophagosome maturation / positive regulation of AMPA receptor activity / activation of transmembrane receptor protein tyrosine kinase activity / negative regulation of smooth muscle contraction / positive regulation of lipophagy / response to psychosocial stress / negative regulation of multicellular organism growth / endosome to lysosome transport / adrenergic receptor signaling pathway / neuronal dense core vesicle / diet induced thermogenesis / positive regulation of protein kinase A signaling / PKA activation in glucagon signalling / hair follicle placode formation / 熱力学 / positive regulation of autophagosome maturation / positive regulation of AMPA receptor activity / activation of transmembrane receptor protein tyrosine kinase activity / negative regulation of smooth muscle contraction / positive regulation of lipophagy / response to psychosocial stress / negative regulation of multicellular organism growth / endosome to lysosome transport / adrenergic receptor signaling pathway / neuronal dense core vesicle / diet induced thermogenesis / positive regulation of protein kinase A signaling / PKA activation in glucagon signalling / hair follicle placode formation /  adenylate cyclase binding / smooth muscle contraction / developmental growth / adenylate cyclase binding / smooth muscle contraction / developmental growth /  D1 dopamine receptor binding / potassium channel regulator activity / D1 dopamine receptor binding / potassium channel regulator activity /  intracellular transport / Hedgehog 'off' state / positive regulation of bone mineralization / positive regulation of cAMP-mediated signaling / adenylate cyclase-activating adrenergic receptor signaling pathway / brown fat cell differentiation / regulation of sodium ion transport / intracellular transport / Hedgehog 'off' state / positive regulation of bone mineralization / positive regulation of cAMP-mediated signaling / adenylate cyclase-activating adrenergic receptor signaling pathway / brown fat cell differentiation / regulation of sodium ion transport /  bone resorption / activation of adenylate cyclase activity / adenylate cyclase activator activity / response to cold / bone resorption / activation of adenylate cyclase activity / adenylate cyclase activator activity / response to cold /  receptor-mediated endocytosis / trans-Golgi network membrane / Olfactory Signaling Pathway / G-protein beta/gamma-subunit complex binding / clathrin-coated endocytic vesicle membrane / Activation of the phototransduction cascade / G beta:gamma signalling through PLC beta / Presynaptic function of Kainate receptors / Thromboxane signalling through TP receptor / receptor-mediated endocytosis / trans-Golgi network membrane / Olfactory Signaling Pathway / G-protein beta/gamma-subunit complex binding / clathrin-coated endocytic vesicle membrane / Activation of the phototransduction cascade / G beta:gamma signalling through PLC beta / Presynaptic function of Kainate receptors / Thromboxane signalling through TP receptor /  骨 / adenylate cyclase-modulating G protein-coupled receptor signaling pathway / G-protein activation / positive regulation of protein serine/threonine kinase activity / G protein-coupled acetylcholine receptor signaling pathway / Activation of G protein gated Potassium channels / Inhibition of voltage gated Ca2+ channels via Gbeta/gamma subunits / adenylate cyclase-activating G protein-coupled receptor signaling pathway / Prostacyclin signalling through prostacyclin receptor / Glucagon signaling in metabolic regulation / G beta:gamma signalling through CDC42 / ADP signalling through P2Y purinoceptor 12 / G beta:gamma signalling through BTK / Synthesis, secretion, and inactivation of Glucagon-like Peptide-1 (GLP-1) / Sensory perception of sweet, bitter, and umami (glutamate) taste / photoreceptor disc membrane / 骨 / adenylate cyclase-modulating G protein-coupled receptor signaling pathway / G-protein activation / positive regulation of protein serine/threonine kinase activity / G protein-coupled acetylcholine receptor signaling pathway / Activation of G protein gated Potassium channels / Inhibition of voltage gated Ca2+ channels via Gbeta/gamma subunits / adenylate cyclase-activating G protein-coupled receptor signaling pathway / Prostacyclin signalling through prostacyclin receptor / Glucagon signaling in metabolic regulation / G beta:gamma signalling through CDC42 / ADP signalling through P2Y purinoceptor 12 / G beta:gamma signalling through BTK / Synthesis, secretion, and inactivation of Glucagon-like Peptide-1 (GLP-1) / Sensory perception of sweet, bitter, and umami (glutamate) taste / photoreceptor disc membrane /  血小板 / Adrenaline,noradrenaline inhibits insulin secretion / 血小板 / Adrenaline,noradrenaline inhibits insulin secretion /  認識 / Glucagon-type ligand receptors / Vasopressin regulates renal water homeostasis via Aquaporins / positive regulation of GTPase activity / G alpha (z) signalling events / cellular response to catecholamine stimulus / Glucagon-like Peptide-1 (GLP1) regulates insulin secretion / ADORA2B mediated anti-inflammatory cytokines production / adenylate cyclase-activating dopamine receptor signaling pathway / ADP signalling through P2Y purinoceptor 1 / G beta:gamma signalling through PI3Kgamma / cellular response to prostaglandin E stimulus / Cooperation of PDCL (PhLP1) and TRiC/CCT in G-protein beta folding / sensory perception of taste / GPER1 signaling / cellular response to amyloid-beta / G-protein beta-subunit binding / Inactivation, recovery and regulation of the phototransduction cascade / 認識 / Glucagon-type ligand receptors / Vasopressin regulates renal water homeostasis via Aquaporins / positive regulation of GTPase activity / G alpha (z) signalling events / cellular response to catecholamine stimulus / Glucagon-like Peptide-1 (GLP1) regulates insulin secretion / ADORA2B mediated anti-inflammatory cytokines production / adenylate cyclase-activating dopamine receptor signaling pathway / ADP signalling through P2Y purinoceptor 1 / G beta:gamma signalling through PI3Kgamma / cellular response to prostaglandin E stimulus / Cooperation of PDCL (PhLP1) and TRiC/CCT in G-protein beta folding / sensory perception of taste / GPER1 signaling / cellular response to amyloid-beta / G-protein beta-subunit binding / Inactivation, recovery and regulation of the phototransduction cascade /  heterotrimeric G-protein complex / G alpha (12/13) signalling events / heterotrimeric G-protein complex / G alpha (12/13) signalling events /  extracellular vesicle / signaling receptor complex adaptor activity / sensory perception of smell / Thrombin signalling through proteinase activated receptors (PARs) / Cargo recognition for clathrin-mediated endocytosis / retina development in camera-type eye / extracellular vesicle / signaling receptor complex adaptor activity / sensory perception of smell / Thrombin signalling through proteinase activated receptors (PARs) / Cargo recognition for clathrin-mediated endocytosis / retina development in camera-type eye /  GTPase binding / GTPase binding /  Clathrin-mediated endocytosis / Ca2+ pathway / phospholipase C-activating G protein-coupled receptor signaling pathway / positive regulation of cold-induced thermogenesis / Clathrin-mediated endocytosis / Ca2+ pathway / phospholipase C-activating G protein-coupled receptor signaling pathway / positive regulation of cold-induced thermogenesis /  amyloid-beta binding / G alpha (i) signalling events / fibroblast proliferation / G alpha (s) signalling events amyloid-beta binding / G alpha (i) signalling events / fibroblast proliferation / G alpha (s) signalling events類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.1 Å クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Papasergi-Scott, M.M. / Skiniotis, G. | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2024 ジャーナル: Nature / 年: 2024タイトル: Time-resolved cryo-EM of G-protein activation by a GPCR. 著者: Makaía M Papasergi-Scott / Guillermo Pérez-Hernández / Hossein Batebi / Yang Gao / Gözde Eskici / Alpay B Seven / Ouliana Panova / Daniel Hilger / Marina Casiraghi / Feng He / Luis Maul / ...著者: Makaía M Papasergi-Scott / Guillermo Pérez-Hernández / Hossein Batebi / Yang Gao / Gözde Eskici / Alpay B Seven / Ouliana Panova / Daniel Hilger / Marina Casiraghi / Feng He / Luis Maul / Peter Gmeiner / Brian K Kobilka / Peter W Hildebrand / Georgios Skiniotis /    要旨: G-protein-coupled receptors (GPCRs) activate heterotrimeric G proteins by stimulating guanine nucleotide exchange in the Gα subunit. To visualize this mechanism, we developed a time-resolved cryo-EM ...G-protein-coupled receptors (GPCRs) activate heterotrimeric G proteins by stimulating guanine nucleotide exchange in the Gα subunit. To visualize this mechanism, we developed a time-resolved cryo-EM approach that examines the progression of ensembles of pre-steady-state intermediates of a GPCR-G-protein complex. By monitoring the transitions of the stimulatory G protein in complex with the β-adrenergic receptor at short sequential time points after GTP addition, we identified the conformational trajectory underlying G-protein activation and functional dissociation from the receptor. Twenty structures generated from sequential overlapping particle subsets along this trajectory, compared to control structures, provide a high-resolution description of the order of main events driving G-protein activation in response to GTP binding. Structural changes propagate from the nucleotide-binding pocket and extend through the GTPase domain, enacting alterations to Gα switch regions and the α5 helix that weaken the G-protein-receptor interface. Molecular dynamics simulations with late structures in the cryo-EM trajectory support that enhanced ordering of GTP on closure of the α-helical domain against the nucleotide-bound Ras-homology domain correlates with α5 helix destabilization and eventual dissociation of the G protein from the GPCR. These findings also highlight the potential of time-resolved cryo-EM as a tool for mechanistic dissection of GPCR signalling events. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8gfv.cif.gz 8gfv.cif.gz | 194.9 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8gfv.ent.gz pdb8gfv.ent.gz | 142.1 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8gfv.json.gz 8gfv.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/gf/8gfv https://data.pdbj.org/pub/pdb/validation_reports/gf/8gfv ftp://data.pdbj.org/pub/pdb/validation_reports/gf/8gfv ftp://data.pdbj.org/pub/pdb/validation_reports/gf/8gfv | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ | 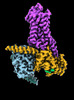 29985MC  8gdzC  8ge1C  8ge2C  8ge3C  8ge4C  8ge5C  8ge6C  8ge7C  8ge8C  8ge9C  8geaC  8gebC  8gecC  8gedC  8geeC  8gefC  8gegC  8gehC  8geiC  8gejC  8gfwC  8gfxC  8gfyC  8gfzC  8gg0C  8gg1C  8gg2C  8gg3C  8gg4C  8gg5C  8gg6C  8gg7C  8gg8C  8gg9C  8ggaC  8ggbC  8ggcC  8ggeC  8ggfC  8ggiC  8ggjC  8ggkC  8gglC  8ggmC  8ggnC  8ggoC  8ggpC  8ggqC  8ggrC  8ggsC  8ggtC  8gguC  8ggvC  8ggwC  8ggxC  8ggyC  8ggzC  8gh0C  8gh1C  8unlC  8unmC  8unnC  8unoC  8unpC  8unqC  8unrC  8unsC  8untC  8unuC  8unvC  8unwC  8unxC  8unyC  8unzC  8uo0C  8uo1C  8uo2C  8uo3C  8uo4C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-Guanine nucleotide-binding protein ... , 3種, 3分子 ABG
| #1: タンパク質 | 分子量: 44326.160 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: GNAS, GNAS1, GSP / 発現宿主: Homo sapiens (ヒト) / 遺伝子: GNAS, GNAS1, GSP / 発現宿主:   Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P63092 Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P63092 |
|---|---|
| #2: タンパク質 | 分子量: 37573.988 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: GNB1 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: GNB1 / 発現宿主:   Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P62873 Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P62873 |
| #3: タンパク質 | 分子量: 7861.143 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: GNG2 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: GNG2 / 発現宿主:   Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P59768 Trichoplusia ni (イラクサキンウワバ) / 参照: UniProt: P59768 |
-タンパク質 , 1種, 1分子 R
| #4: タンパク質 |  / Beta-2 adrenoreceptor / Beta-2 adrenoceptor / Beta-2 adrenoreceptor / Beta-2 adrenoceptor分子量: 51767.242 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: ADRB2, ADRB2R, B2AR Homo sapiens (ヒト) / 遺伝子: ADRB2, ADRB2R, B2AR発現宿主:   Spodoptera frugiperda (ツマジロクサヨトウ) Spodoptera frugiperda (ツマジロクサヨトウ)参照: UniProt: P07550 |
|---|
-非ポリマー , 3種, 5分子 




| #5: 化合物 | ChemComp-GTP /  グアノシン三リン酸 グアノシン三リン酸 |
|---|---|
| #6: 化合物 | ChemComp-G1I / ( |
| #7: 水 | ChemComp-HOH /  水 水 |
-詳細
| 研究の焦点であるリガンドがあるか | N |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Complex of beta-2 adrenergic receptor and Gs heterotrimer with GTP タイプ: COMPLEX 詳細: Combined datasets of complex plunge frozen at 5 sec, 10 sec, or 17 sec after GTP addition to the sample. Entity ID: #1-#4 / 由来: MULTIPLE SOURCES | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 実験値: NO | ||||||||||||
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
| 由来(組換発現) |
| ||||||||||||
| 緩衝液 | pH: 7.5 詳細: GTP was added just prior to freezing at 5 sec, 10 sec, or 17 sec before plunging. | ||||||||||||
| 試料 | 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES | ||||||||||||
| 試料支持 | グリッドのタイプ: UltrAuFoil R1.2/1.3 | ||||||||||||
急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277.15 K 詳細: GTP was added just prior to freezing at 5 sec, 10 sec, or 17 sec before plunging. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 2000 nm / 最小 デフォーカス(公称値): 400 nm Bright-field microscopy / 最大 デフォーカス(公称値): 2000 nm / 最小 デフォーカス(公称値): 400 nm |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 電子線照射量: 50 e/Å2 / 検出モード: COUNTING / フィルム・検出器のモデル: GATAN K3 (6k x 4k) 詳細: The cryoEM map is the result of combining multiple datasets: cryo-EM imaging of the beta-2AR-Gs + GTP (5 sec) complex was performed on a Titan Krios electron microscope equipped with a K3 ...詳細: The cryoEM map is the result of combining multiple datasets: cryo-EM imaging of the beta-2AR-Gs + GTP (5 sec) complex was performed on a Titan Krios electron microscope equipped with a K3 Summit direct electron detector (Gatan). The microscope was operated at 300 kV accelerating voltage, with a nominal magnification of 105,000x in counting mode resulting in a magnified pixel size of 0.8677 Angstrom. A total exposure of 60.48 electrons/ Angstrom^2 over 63 frames with defocus ranging from -1.0 - -2.0 micrometers was used. Cryo-EM imaging of beta-2AR-Gs + GTP (10 sec) complex was performed on four separate grids over three collection sessions. The microscope was operated at 300 kV accelerating voltage, with a magnification at the camera of 58,679x in counting mode resulting in a magnified pixel size of 0.8521 Angstrom. For the first and second grids, movies were obtained at an exposure rate of 21.13 electrons/Angstrum^2/sec with defocus ranging from -0.4 - -2.0 micrometers. The total exposure time was 2.717 sec over 77 frames per movie stack. For an additional collection of the first grid, movies were obtained at an exposure rate of 20.95 electrons/ Angstrum^2/sec with defocus ranging from -0.4 -2.0 micrometers. The total exposure time was 2.717 sec over 77 frames per movie stack. For the third and fourth grids, movies were obtained at an exposure rate of 30.71 electrons/ Angstrum^2/sec with defocus ranging from -0.5 - -1.6 micrometers. The total exposure time was 2.008 sec over 79 frames per movie stack. Cryo-EM imaging of beta-2AR-Gs + GTP (17 sec) was performed on a Titan Krios equipped with a post-column energy filter, with a magnification of 105,000x in counting mode resulting in a magnified pixel size of 0.8677 Angstrom. Movies were obtained at an exposure rate of 32.46 electrons/Angstrum^2/sec with defocus ranging from -0.4 - -0.9 micrometers. The total exposure time was 1.999 sec over 79 frames per movie stack. |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | タイプ: NONE | ||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 19918625 | ||||||||||||||||||||||||||||
3次元再構成 | 解像度: 3.1 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 51197 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー




























































 PDBj
PDBj























