+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6t21 | ||||||
|---|---|---|---|---|---|---|---|
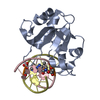
| タイトル | N-terminal domain of EcoKMcrA restriction endonuclease (NEco) in complex with T5mCGA target sequence | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | HYDROLASE / EcoKMcrA / NEco / N-TERMINAL DOMAIN / MODIFICATION DEPENDENT RESTRICTION / 5-METHYLCYTOSINE / 5MC / 5-HYDROXYMETHYLCYTOSINE / 5HMC / HNH ENDONUCLEASE / BBA-ME NUCLEASE | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報加水分解酵素; エステル加水分解酵素; 5'-リン酸モノエステル産生エンドデオキシリボヌクレアーゼ / methyl-CpG binding / DNA restriction-modification system / endonuclease activity / zinc ion binding 類似検索 - 分子機能 | ||||||
| 生物種 |  synthetic construct (人工物) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.07 Å 分子置換 / 解像度: 2.07 Å | ||||||
 データ登録者 データ登録者 | Slyvka, A. / Zagorskaite, E. / Czapinska, H. / Sasnauskas, G. / Bochtler, M. | ||||||
 引用 引用 |  ジャーナル: Nucleic Acids Res. / 年: 2019 ジャーナル: Nucleic Acids Res. / 年: 2019タイトル: Crystal structure of the EcoKMcrA N-terminal domain (NEco): recognition of modified cytosine bases without flipping. 著者: Slyvka, A. / Zagorskaite, E. / Czapinska, H. / Sasnauskas, G. / Bochtler, M. #1:  ジャーナル: Nucleic Acids Res. / 年: 2018 ジャーナル: Nucleic Acids Res. / 年: 2018タイトル: Activity and structure of EcoKMcrA. 著者: Czapinska, H. / Kowalska, M. / Zagorskaite, E. / Manakova, E. / Slyvka, A. / Xu, S.Y. / Siksnys, V. / Sasnauskas, G. / Bochtler, M. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6t21.cif.gz 6t21.cif.gz | 191.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6t21.ent.gz pdb6t21.ent.gz | 149 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6t21.json.gz 6t21.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  6t21_validation.pdf.gz 6t21_validation.pdf.gz | 455.9 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  6t21_full_validation.pdf.gz 6t21_full_validation.pdf.gz | 460.7 KB | 表示 | |
| XML形式データ |  6t21_validation.xml.gz 6t21_validation.xml.gz | 19.5 KB | 表示 | |
| CIF形式データ |  6t21_validation.cif.gz 6t21_validation.cif.gz | 29.4 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/t2/6t21 https://data.pdbj.org/pub/pdb/validation_reports/t2/6t21 ftp://data.pdbj.org/pub/pdb/validation_reports/t2/6t21 ftp://data.pdbj.org/pub/pdb/validation_reports/t2/6t21 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 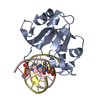
| ||||||||
| 2 | 
| ||||||||
| 単位格子 |
| ||||||||
| Components on special symmetry positions |
|
- 要素
要素
| #1: タンパク質 | 分子量: 17368.604 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  株: K12 / 遺伝子: mcrA, rglA, b1159, JW1145 / プラスミド: PET15BM / 発現宿主:  参照: UniProt: P24200, 加水分解酵素; エステル加水分解酵素; 5'-リン酸モノエステル産生エンドデオキシリボヌクレアーゼ #2: DNA鎖 | 分子量: 3009.006 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現) synthetic construct (人工物) / 発現宿主: synthetic construct (人工物) #3: DNA鎖 | 分子量: 3107.081 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現) synthetic construct (人工物) / 発現宿主: synthetic construct (人工物) #4: 水 | ChemComp-HOH / | 研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 3.05 Å3/Da / 溶媒含有率: 59.66 % |
|---|---|
| 結晶化 | 温度: 291 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 6.5 詳細: 1.8 ul of protein-DNA solution (436:523 uM) was mixed with 2.2 ul of the F1 condition of the PACT premier crystal screen (MDL) (0.2 M Sodium fluoride, 0.1 M Bis-Tris propane, pH 6.5, 20% PEG ...詳細: 1.8 ul of protein-DNA solution (436:523 uM) was mixed with 2.2 ul of the F1 condition of the PACT premier crystal screen (MDL) (0.2 M Sodium fluoride, 0.1 M Bis-Tris propane, pH 6.5, 20% PEG 3350) and cryo-protected with an addition of 25% glycerol. |
-データ収集
| 回折 | 平均測定温度: 100 K / Serial crystal experiment: N |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  PETRA III, EMBL c/o DESY PETRA III, EMBL c/o DESY  / ビームライン: P14 (MX2) / 波長: 0.9793 Å / ビームライン: P14 (MX2) / 波長: 0.9793 Å |
| 検出器 | タイプ: DECTRIS EIGER X 16M / 検出器: PIXEL / 日付: 2019年8月13日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.9793 Å / 相対比: 1 |
| 反射 | 解像度: 2.07→33.38 Å / Num. obs: 36261 / % possible obs: 99.5 % / 冗長度: 38.87 % / Biso Wilson estimate: 53 Å2 / CC1/2: 1 / Rmerge(I) obs: 0.103 / Rrim(I) all: 0.105 / Net I/σ(I): 30.17 |
| 反射 シェル | 解像度: 2.07→2.19 Å / 冗長度: 38.92 % / Rmerge(I) obs: 2.299 / Mean I/σ(I) obs: 1.98 / Num. unique obs: 5681 / CC1/2: 0.758 / Rrim(I) all: 2.329 / % possible all: 98.6 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: 6R64 解像度: 2.07→33.38 Å / Cor.coef. Fo:Fc: 0.976 / Cor.coef. Fo:Fc free: 0.961 / SU B: 7.669 / SU ML: 0.103 / 交差検証法: THROUGHOUT / σ(F): 0 / ESU R: 0.148 / ESU R Free: 0.141 詳細: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS. TLS REFINEMENT HAS BEEN USED. U VALUES : WITH TLS ADDED. THE CLUSTERS OF SOLVENT MOLECULES BETWEEN RESIDUES 46 AND 94 AND NEXT TO RESIDUE 54 ...詳細: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS. TLS REFINEMENT HAS BEEN USED. U VALUES : WITH TLS ADDED. THE CLUSTERS OF SOLVENT MOLECULES BETWEEN RESIDUES 46 AND 94 AND NEXT TO RESIDUE 54 OF CHAIN B LIKELY CORRESPOND TO DISORDERED GLYCEROL MOLECULES. THE ELECTRON DENSITY IS NOT DEFINED ENOUGH TO UNAMBIGUOUSLY MODEL THEM.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | イオンプローブ半径: 0.8 Å / 減衰半径: 0.8 Å / VDWプローブ半径: 1.2 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso max: 135.27 Å2 / Biso mean: 52.793 Å2 / Biso min: 33.27 Å2
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: final / 解像度: 2.07→33.38 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル | 解像度: 2.07→2.12 Å / Rfactor Rfree error: 0
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLS | 手法: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLSグループ |
|
 ムービー
ムービー コントローラー
コントローラー












 PDBj
PDBj

