+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 1w4w | ||||||
|---|---|---|---|---|---|---|---|
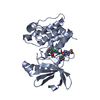
| Title | Ferric horseradish peroxidase C1A in complex with formate | ||||||
 Components Components | HORSERADISH PEROXIDASE C1A | ||||||
 Keywords Keywords | OXIDOREDUCTASE / FORMATE ION / CALCIUM / FERRIC STATE / GLYCOPROTEIN / HEME / HORSERADISH / IRON / MULTIGENE FAMILY / PEROXIDASE / PYRROLIDONE CARBOXYLIC ACID | ||||||
| Function / homology |  Function and homology information Function and homology informationlactoperoxidase activity / peroxidase / vacuole / hydrogen peroxide catabolic process / response to oxidative stress / heme binding / extracellular region / metal ion binding Similarity search - Function | ||||||
| Biological species |  ARMORACIA RUSTICANA (horseradish) ARMORACIA RUSTICANA (horseradish) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.55 Å MOLECULAR REPLACEMENT / Resolution: 1.55 Å | ||||||
 Authors Authors | Carlsson, G.H. / Nicholls, P. / Svistunenko, D. / Berglund, G.I. / Hajdu, J. | ||||||
 Citation Citation |  Journal: Biochemistry / Year: 2005 Journal: Biochemistry / Year: 2005Title: Complexes of Horseradish Peroxidase with Formate, Acetate, and Carbon Monoxide Authors: Carlsson, G.H. / Nicholls, P. / Svistunenko, D. / Berglund, G.I. / Hajdu, J. #1:  Journal: Nature / Year: 2002 Journal: Nature / Year: 2002Title: The Catalytic Pathway of Horseradish Peroxidase at High Resolution Authors: Berglund, G.I. / Carlsson, G.H. / Smith, A.T. / Szoke, H. / Henriksen, A. / Hajdu, J. #2: Journal: J.Biol.Chem. / Year: 1990 Title: Expression of a Synthetic Gene for Horseradish Peroxidase C in Escherichia Coli and Folding and Activation of the Recombinant Enzyme with Ca2 and Heme Authors: Smith, A.T. / Santama, N. / Dacey, S. / Edwards, M. / Bray, R.C. / Thorneley, R.N. / Burke, J.F. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  1w4w.cif.gz 1w4w.cif.gz | 84.8 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb1w4w.ent.gz pdb1w4w.ent.gz | 62.2 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  1w4w.json.gz 1w4w.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/w4/1w4w https://data.pdbj.org/pub/pdb/validation_reports/w4/1w4w ftp://data.pdbj.org/pub/pdb/validation_reports/w4/1w4w ftp://data.pdbj.org/pub/pdb/validation_reports/w4/1w4w | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  1w4yC  1h5aS S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| Unit cell |
|
- Components
Components
| #1: Protein | Mass: 35652.125 Da / Num. of mol.: 1 Source method: isolated from a genetically manipulated source Details: A FORMATE ION IS BOUND IN THE ACTIVE SITE / Source: (gene. exp.)  ARMORACIA RUSTICANA (horseradish) / Production host: ARMORACIA RUSTICANA (horseradish) / Production host:  | ||||||
|---|---|---|---|---|---|---|---|
| #2: Chemical | ChemComp-HEM / | ||||||
| #3: Chemical | | #4: Chemical | ChemComp-FMT / | #5: Water | ChemComp-HOH / | Has protein modification | Y | |
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 7 X-RAY DIFFRACTION / Number of used crystals: 7 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.26 Å3/Da / Density % sol: 45.6 % Description: DATA COLLECTED USING A MULTICRYSTAL STRATEGY TO DECREASE THE X-RAY INDUCED REDUCTION OF THE IRON |
|---|---|
| Crystal grow | Temperature: 277 K / Method: vapor diffusion, hanging drop / pH: 6.5 Details: 20% PEG8000, 0.2M CA-ACETATE, 0.1 M NA-CACODYLATE PH 6.5, FERULIC ACID AS ADDITIVE STREAK SEEDING, HANGING DROP, 4DEGC |
-Data collection
| Diffraction | Mean temperature: 90 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  MAX II MAX II  / Beamline: I711 / Wavelength: 1.089 / Beamline: I711 / Wavelength: 1.089 |
| Detector | Type: MARRESEARCH / Detector: CCD / Date: Sep 26, 2003 / Details: SI(III) |
| Radiation | Monochromator: MULTIPOLE WIGGLER / Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 1.089 Å / Relative weight: 1 |
| Reflection | Resolution: 1.51→50 Å / Num. obs: 49541 / % possible obs: 96 % / Observed criterion σ(I): 3 / Redundancy: 3.7 % / Biso Wilson estimate: 17.7 Å2 / Rmerge(I) obs: 0.07 / Net I/σ(I): 12.1 |
| Reflection shell | Resolution: 1.51→1.57 Å / Rmerge(I) obs: 0.24 / % possible all: 78.7 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: PDB ENTRY 1H5A Resolution: 1.55→29.87 Å / Rfactor Rfree error: 0.004 / Data cutoff high absF: 1343934.32 / Isotropic thermal model: RESTRAINED / Cross valid method: THROUGHOUT / σ(F): 0 / Stereochemistry target values: MAXIMUM LIKELIHOOD
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Solvent model: FLAT MODEL / Bsol: 40.5205 Å2 / ksol: 0.32652 e/Å3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 15 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.55→29.87 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 1.55→1.65 Å / Rfactor Rfree error: 0.015 / Total num. of bins used: 6
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Xplor file |
|
 Movie
Movie Controller
Controller

















































 PDBj
PDBj







