+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-11149 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | bovine ATP synthase Fo domain | |||||||||
 マップデータ マップデータ | Fo main map | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Mitochondrial protein import / Formation of ATP by chemiosmotic coupling / Cristae formation / : / : / Mitochondrial protein degradation / proton-transporting ATP synthase complex, coupling factor F(o) / : / proton transmembrane transporter activity / proton motive force-driven ATP synthesis ...Mitochondrial protein import / Formation of ATP by chemiosmotic coupling / Cristae formation / : / : / Mitochondrial protein degradation / proton-transporting ATP synthase complex, coupling factor F(o) / : / proton transmembrane transporter activity / proton motive force-driven ATP synthesis / proton transmembrane transport / proton motive force-driven mitochondrial ATP synthesis / lipid binding 類似検索 - 分子機能 | |||||||||
| 生物種 |   | |||||||||
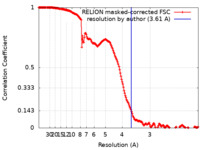
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.61 Å | |||||||||
 データ登録者 データ登録者 | Spikes T / Montgomery MG / Walker JE | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2020 ジャーナル: Proc Natl Acad Sci U S A / 年: 2020タイトル: Structure of the dimeric ATP synthase from bovine mitochondria. 著者: Tobias E Spikes / Martin G Montgomery / John E Walker /  要旨: The structure of the dimeric ATP synthase from bovine mitochondria determined in three rotational states by electron cryo-microscopy provides evidence that the proton uptake from the mitochondrial ...The structure of the dimeric ATP synthase from bovine mitochondria determined in three rotational states by electron cryo-microscopy provides evidence that the proton uptake from the mitochondrial matrix via the proton inlet half channel proceeds via a Grotthus mechanism, and a similar mechanism may operate in the exit half channel. The structure has given information about the architecture and mechanical constitution and properties of the peripheral stalk, part of the membrane extrinsic region of the stator, and how the action of the peripheral stalk damps the side-to-side rocking motions that occur in the enzyme complex during the catalytic cycle. It also describes wedge structures in the membrane domains of each monomer, where the skeleton of each wedge is provided by three α-helices in the membrane domains of the b-subunit to which the supernumerary subunits e, f, and g and the membrane domain of subunit A6L are bound. Protein voids in the wedge are filled by three specifically bound cardiolipin molecules and two other phospholipids. The external surfaces of the wedges link the monomeric complexes together into the dimeric structures and provide a pivot to allow the monomer-monomer interfaces to change during catalysis and to accommodate other changes not related directly to catalysis in the monomer-monomer interface that occur in mitochondrial cristae. The structure of the bovine dimer also demonstrates that the structures of dimeric ATP synthases in a tetrameric porcine enzyme have been seriously misinterpreted in the membrane domains. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11149.map.gz emd_11149.map.gz | 438.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11149-v30.xml emd-11149-v30.xml emd-11149.xml emd-11149.xml | 25.9 KB 25.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_11149_fsc.xml emd_11149_fsc.xml | 17.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_11149.png emd_11149.png | 46.7 KB | ||
| マスクデータ |  emd_11149_msk_1.map emd_11149_msk_1.map | 476.8 MB |  マスクマップ マスクマップ | |
| その他 |  emd_11149_half_map_1.map.gz emd_11149_half_map_1.map.gz emd_11149_half_map_2.map.gz emd_11149_half_map_2.map.gz | 382.2 MB 382.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11149 http://ftp.pdbj.org/pub/emdb/structures/EMD-11149 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11149 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11149 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11149_validation.pdf.gz emd_11149_validation.pdf.gz | 347.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11149_full_validation.pdf.gz emd_11149_full_validation.pdf.gz | 346.7 KB | 表示 | |
| XML形式データ |  emd_11149_validation.xml.gz emd_11149_validation.xml.gz | 22.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11149 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11149 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11149 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11149 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6zbbMC  6yy0C  6z1rC  6z1uC  6zg7C  6zg8C  6zikC  6ziqC  6zitC  6ziuC  6zmrC  6znaC  6zpoC  6zqmC  6zqnC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11149.map.gz / 形式: CCP4 / 大きさ: 476.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11149.map.gz / 形式: CCP4 / 大きさ: 476.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Fo main map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.048 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_11149_msk_1.map emd_11149_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
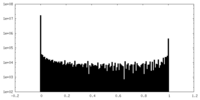
| 投影像・断面図 |
| ||||||||||||
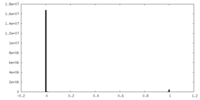
| 密度ヒストグラム |
-ハーフマップ: Fo half map 1
| ファイル | emd_11149_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Fo half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
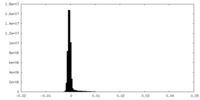
| 密度ヒストグラム |
-ハーフマップ: Fo half map 2
| ファイル | emd_11149_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Fo half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
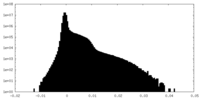
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : ATP synthase
+超分子 #1: ATP synthase
+分子 #1: ATP synthase protein 8
+分子 #2: ATP synthase F(0) complex subunit C1, mitochondrial
+分子 #3: ATP synthase subunit a
+分子 #4: ATP synthase F(0) complex subunit B1, mitochondrial
+分子 #5: ATP synthase subunit d, mitochondrial
+分子 #6: ATP synthase subunit e, mitochondrial
+分子 #7: ATP synthase subunit f, mitochondrial
+分子 #8: ATP synthase subunit g, mitochondrial
+分子 #9: ATP synthase subunit ATP5MPL, mitochondrial
+分子 #10: ATP synthase membrane subunit DAPIT, mitochondrial
+分子 #11: CARDIOLIPIN
+分子 #12: 1,2-DIPALMITOYL-PHOSPHATIDYL-GLYCEROLE
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 4.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: UltrAuFoil / 材質: GOLD |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 294 K / 装置: FEI VITROBOT MARK IV 詳細: The sample was allowed to penetrate through the holey support and to distribute to both sides of the grid surface for ca. 15 sec. Then the grids were blotted with filter paper for 8-10 sec before blotting.. |
| 詳細 | Nickel affinity purified filled by gel filtration |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: COUNTING / 平均露光時間: 12.0 sec. / 平均電子線量: 4.6 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




























 Z
Z Y
Y X
X