+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-10443 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Virion of native gene transfer agent (GTA) particle | ||||||||||||||||||||||||
 マップデータ マップデータ | virion of native GTA particle | ||||||||||||||||||||||||
 試料 試料 | Rhodobacter capsulatus DE442 != Rhodobacter capsulatus SB 1003 Rhodobacter capsulatus DE442
| ||||||||||||||||||||||||
 キーワード キーワード | "virion" / "horizontal gene transfer" / "gene delivery" / "HK97" / VIRUS | ||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報GTA TIM-barrel-like domain / : / GTA TIM-barrel-like domain / Rcc01698-like, C-terminal / Protein of unknown function DUF2460 / Conserved hypothetical protein 2217 (DUF2460) / Phage conserved hypothetical protein / Tail completion protein / Tail completion protein gp17 / Baseplate hub protein, N-terminal attachment domain ...GTA TIM-barrel-like domain / : / GTA TIM-barrel-like domain / Rcc01698-like, C-terminal / Protein of unknown function DUF2460 / Conserved hypothetical protein 2217 (DUF2460) / Phage conserved hypothetical protein / Tail completion protein / Tail completion protein gp17 / Baseplate hub protein, N-terminal attachment domain / Gene transfer agent, major tail protein / Phage portal protein, HK97 / Bacteriophage phiJL001, Gp84 / Bacteriophage phiJL001, Gp84, C-terminal / : / Phage conserved hypothetical protein BR0599 / Bacteriophage SPP1, head-tail adaptor superfamily / Bacteriophage SPP1, head-tail adaptor / Phage head completion protein / Tip attachment protein J / Putative phage tail protein / Phage major tail protein TP901-1 / Phage tail tube protein / Bacteriophage/Gene transfer agent portal protein / Phage portal protein / : / Phage capsid / Phage capsid family / Glycoside hydrolase superfamily 類似検索 - ドメイン・相同性 | ||||||||||||||||||||||||
| 生物種 |  Rhodobacter capsulatus SB 1003 (バクテリア) Rhodobacter capsulatus SB 1003 (バクテリア) | ||||||||||||||||||||||||
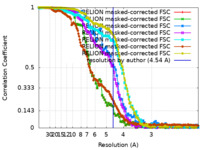
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.54 Å | ||||||||||||||||||||||||
 データ登録者 データ登録者 | Bardy P / Fuzik T | ||||||||||||||||||||||||
| 資金援助 |  チェコ, 7件 チェコ, 7件
| ||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2020 ジャーナル: Nat Commun / 年: 2020タイトル: Structure and mechanism of DNA delivery of a gene transfer agent. 著者: Pavol Bárdy / Tibor Füzik / Dominik Hrebík / Roman Pantůček / J Thomas Beatty / Pavel Plevka /   要旨: Alphaproteobacteria, which are the most abundant microorganisms of temperate oceans, produce phage-like particles called gene transfer agents (GTAs) that mediate lateral gene exchange. However, the ...Alphaproteobacteria, which are the most abundant microorganisms of temperate oceans, produce phage-like particles called gene transfer agents (GTAs) that mediate lateral gene exchange. However, the mechanism by which GTAs deliver DNA into cells is unknown. Here we present the structure of the GTA of Rhodobacter capsulatus (RcGTA) and describe the conformational changes required for its DNA ejection. The structure of RcGTA resembles that of a tailed phage, but it has an oblate head shortened in the direction of the tail axis, which limits its packaging capacity to less than 4,500 base pairs of linear double-stranded DNA. The tail channel of RcGTA contains a trimer of proteins that possess features of both tape measure proteins of long-tailed phages from the family Siphoviridae and tail needle proteins of short-tailed phages from the family Podoviridae. The opening of a constriction within the RcGTA baseplate enables the ejection of DNA into bacterial periplasm. | ||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_10443.map.gz emd_10443.map.gz | 76.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-10443-v30.xml emd-10443-v30.xml emd-10443.xml emd-10443.xml | 34.7 KB 34.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_10443_fsc.xml emd_10443_fsc.xml emd_10443_fsc_1.xml emd_10443_fsc_1.xml emd_10443_fsc_2.xml emd_10443_fsc_2.xml emd_10443_fsc_3.xml emd_10443_fsc_3.xml emd_10443_fsc_4.xml emd_10443_fsc_4.xml emd_10443_fsc_5.xml emd_10443_fsc_5.xml emd_10443_fsc_6.xml emd_10443_fsc_6.xml | 9.2 KB 9.2 KB 9.1 KB 10.7 KB 10.7 KB 18.1 KB 18.1 KB | 表示 表示 表示 表示 表示 表示 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_10443.png emd_10443.png | 87.5 KB | ||
| Filedesc metadata |  emd-10443.cif.gz emd-10443.cif.gz | 9.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-10443 http://ftp.pdbj.org/pub/emdb/structures/EMD-10443 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10443 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10443 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_10443_validation.pdf.gz emd_10443_validation.pdf.gz | 228.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_10443_full_validation.pdf.gz emd_10443_full_validation.pdf.gz | 227.3 KB | 表示 | |
| XML形式データ |  emd_10443_validation.xml.gz emd_10443_validation.xml.gz | 15.6 KB | 表示 | |
| CIF形式データ |  emd_10443_validation.cif.gz emd_10443_validation.cif.gz | 20 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10443 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10443 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10443 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10443 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6tbaMC  6tb9C  6te8C  6te9C  6teaC  6tebC  6tehC  6to8C  6toaC  6tsuC  6tsvC  6tswC  6tuiC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_10443.map.gz / 形式: CCP4 / 大きさ: 3.3 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_10443.map.gz / 形式: CCP4 / 大きさ: 3.3 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | virion of native GTA particle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.063 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Rhodobacter capsulatus DE442
+超分子 #1: Rhodobacter capsulatus SB 1003
+超分子 #2: Capsid
+超分子 #3: Head spike
+超分子 #4: Connector
+超分子 #5: Tail
+超分子 #6: Baseplate
+分子 #1: Phage major capsid protein, HK97 family
+分子 #2: Uncharacterized protein
+分子 #3: Uncharacterized protein
+分子 #4: Uncharacterized protein
+分子 #5: Portal protein Rcc01684
+分子 #6: Uncharacterized protein
+分子 #7: Uncharacterized protein
+分子 #8: Phage major tail protein, TP901-1 family
+分子 #9: Uncharacterized protein
+分子 #10: Uncharacterized protein
+分子 #11: Uncharacterized protein
+分子 #12: IRON/SULFUR CLUSTER
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 20 mg/mL | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.8 構成要素:
詳細: G-buffer, doi: 10.1016/0003-9861(77)90508-2 | ||||||||||||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 11 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 雰囲気: OTHER | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 293.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: INTEGRATING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 平均電子線量: 42.75 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): -3.0 µm / 最小 デフォーカス(公称値): -1.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-6tba: |
 ムービー
ムービー コントローラー
コントローラー
























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)