+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 5a0y | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
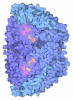
| タイトル | METHYL-COENZYME M REDUCTASE FROM METHANOTHERMOBACTER MARBURGENSIS AT 1.1 A RESOLUTION | |||||||||
 要素 要素 | (METHYL-COENZYME M REDUCTASE I SUBUNIT ...) x 3 | |||||||||
 キーワード キーワード | TRANSFERASE / POST-TRANSLATIONAL MODIFICATION / BINDING SITES / CATALYSIS / COENZYMES / DISULFIDES / HYDROGEN / HYDROGEN BONDING / LIGANDS / MESNA / METALLOPORPHYRINS / METHANE / METHANOBACTERIUM / MODELS / MOLECULAR / NICKEL / OXIDATION-REDUCTION / OXIDOREDUCTASES / PHOSPHOTHREONINE / PROTEIN CONFORMATION / PROTEIN FOLDING / PROTEIN STRUCTURE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報coenzyme-B sulfoethylthiotransferase / coenzyme-B sulfoethylthiotransferase activity / methanogenesis / metal ion binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |   METHANOTHERMOBACTER MARBURGENSIS (古細菌) METHANOTHERMOBACTER MARBURGENSIS (古細菌) | |||||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.1 Å 分子置換 / 解像度: 1.1 Å | |||||||||
 データ登録者 データ登録者 | Wagner, T. / Ermler, U. | |||||||||
 引用 引用 |  ジャーナル: Angew.Chem.Int.Ed.Engl. / 年: 2016 ジャーナル: Angew.Chem.Int.Ed.Engl. / 年: 2016タイトル: Didehydroaspartate Modification in Methyl-Coenzyme M Reductase Catalyzing Methane Formation. 著者: Wagner, T. / Kahnt, J. / Ermler, U. / Shima, S. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  5a0y.cif.gz 5a0y.cif.gz | 1.1 MB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb5a0y.ent.gz pdb5a0y.ent.gz | 904.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  5a0y.json.gz 5a0y.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  5a0y_validation.pdf.gz 5a0y_validation.pdf.gz | 1.8 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  5a0y_full_validation.pdf.gz 5a0y_full_validation.pdf.gz | 1.8 MB | 表示 | |
| XML形式データ |  5a0y_validation.xml.gz 5a0y_validation.xml.gz | 115.1 KB | 表示 | |
| CIF形式データ |  5a0y_validation.cif.gz 5a0y_validation.cif.gz | 176.7 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/a0/5a0y https://data.pdbj.org/pub/pdb/validation_reports/a0/5a0y ftp://data.pdbj.org/pub/pdb/validation_reports/a0/5a0y ftp://data.pdbj.org/pub/pdb/validation_reports/a0/5a0y | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||||||
| 単位格子 |
| ||||||||||||||||
| 非結晶学的対称性 (NCS) | NCS oper:
|
- 要素
要素
-METHYL-COENZYME M REDUCTASE I SUBUNIT ... , 3種, 6分子 ADBECF
| #1: タンパク質 | 分子量: 60637.648 Da / 分子数: 2 / 由来タイプ: 天然 / 詳細: GERMAN COLLECTION OF MICROORGANISMS (DSM) 由来: (天然)   METHANOTHERMOBACTER MARBURGENSIS (古細菌) METHANOTHERMOBACTER MARBURGENSIS (古細菌)株: MARBURG 参照: UniProt: P11558, coenzyme-B sulfoethylthiotransferase #2: タンパク質 | 分子量: 47279.676 Da / 分子数: 2 / 由来タイプ: 天然 / 詳細: GERMAN COLLECTION OF MICROORGANISMS (DSM) 由来: (天然)   METHANOTHERMOBACTER MARBURGENSIS (古細菌) METHANOTHERMOBACTER MARBURGENSIS (古細菌)株: MARBURG 参照: UniProt: P11560, coenzyme-B sulfoethylthiotransferase #3: タンパク質 | 分子量: 28797.234 Da / 分子数: 2 / 由来タイプ: 天然 / 詳細: GERMAN COLLECTION OF MICROORGANISMS (DSM) 由来: (天然)   METHANOTHERMOBACTER MARBURGENSIS (古細菌) METHANOTHERMOBACTER MARBURGENSIS (古細菌)株: MARBURG 参照: UniProt: P11562, coenzyme-B sulfoethylthiotransferase |
|---|
-非ポリマー , 8種, 2821分子 











| #4: 化合物 | ChemComp-MG / #5: 化合物 | #6: 化合物 | #7: 化合物 | #8: 化合物 | ChemComp-K / | #9: 化合物 | #10: 化合物 | #11: 水 | ChemComp-HOH / | |
|---|
-詳細
| 非ポリマーの詳細 | DIDEHYDROASPARTATE (DYA): DIDEHYDROASPARTATE IS AN ASPARTATE CONTAINING A DOUBLE BOND BETWEEN THE C ...DIDEHYDROA |
|---|---|
| 配列の詳細 | RESIDUE 450 IS A DIDEHYDROA |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.18 Å3/Da / 溶媒含有率: 43.65 % / 解説: NONE |
|---|---|
| 結晶化 | pH: 9 詳細: 27.5% (V/V) PEG 400, 100 MM HEPES PH 7.5, 250 MM MGCL2, AND 200 MM NACL |
-データ収集
| 回折 | 平均測定温度: 77 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  SOLEIL SOLEIL  / ビームライン: PROXIMA 1 / 波長: 0.85506 / ビームライン: PROXIMA 1 / 波長: 0.85506 |
| 検出器 | タイプ: MARRESEARCH / 検出器: CCD / 日付: 2014年12月11日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.85506 Å / 相対比: 1 |
| 反射 | 解像度: 1.1→48.35 Å / Num. obs: 937928 / % possible obs: 99.3 % / Observed criterion σ(I): 1.7 / 冗長度: 3.4 % / Biso Wilson estimate: 9.06 Å2 / Rmerge(I) obs: 0.06 / Net I/σ(I): 10.5 |
| 反射 シェル | 解像度: 1.1→1.16 Å / 冗長度: 3.3 % / Rmerge(I) obs: 0.7 / Mean I/σ(I) obs: 1.7 / % possible all: 97.8 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: PDB ENTRY 3POT 解像度: 1.1→48.346 Å / SU ML: 0.1 / σ(F): 1.33 / 位相誤差: 12.26 / 立体化学のターゲット値: ML 詳細: CONSIDERING THE RESOLUTION HYDROGEN REFINEMENT MODEL HAS BEEN USED WITH THE RIDING MODEL A NEW POST-TRANSLATIONAL MODIFICATION IS PRESENT IN THE CHAIN A AND D CALLED DIDEHYDROASPARTATE AT THE POSITION 450
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.11 Å / 溶媒モデル: FLAT BULK SOLVENT MODEL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 15.13 Å2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 1.1→48.346 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル |
|
 ムービー
ムービー コントローラー
コントローラー

















 PDBj
PDBj