[English] 日本語
 Yorodumi
Yorodumi- EMDB-7843: Cryo-EM structure of RAG in complex with 12-RSS and 23-RSS nicked... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: EMDB / ID: EMD-7843 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Title | Cryo-EM structure of RAG in complex with 12-RSS and 23-RSS nicked DNA intermediates | |||||||||
 Map data Map data | RAG in complex with 12-RSS and 23-RSS nicked DNA intermediates, sharpened map with B factor -91 | |||||||||
 Sample Sample |
| |||||||||
 Keywords Keywords | V(D)J recombination / synaptic RAG complex / nicked RSS intermediates / paired complex / RECOMBINATION-DNA complex | |||||||||
| Function / homology |  Function and homology information Function and homology informationsomatic diversification of immune receptors via germline recombination within a single locus / hematopoietic or lymphoid organ development / protein-DNA complex assembly / DNA recombinase complex / endodeoxyribonuclease complex / lymphocyte differentiation / pre-B cell allelic exclusion / immunoglobulin V(D)J recombination / V(D)J recombination / phosphatidylinositol-3,4-bisphosphate binding ...somatic diversification of immune receptors via germline recombination within a single locus / hematopoietic or lymphoid organ development / protein-DNA complex assembly / DNA recombinase complex / endodeoxyribonuclease complex / lymphocyte differentiation / pre-B cell allelic exclusion / immunoglobulin V(D)J recombination / V(D)J recombination / phosphatidylinositol-3,4-bisphosphate binding / histone H3K4me3 reader activity / phosphatidylinositol-3,5-bisphosphate binding / detection of maltose stimulus / maltose transport complex / phosphatidylinositol-3,4,5-trisphosphate binding / carbohydrate transport / T cell differentiation / carbohydrate transmembrane transporter activity / maltose binding / maltose transport / maltodextrin transmembrane transport / ATP-binding cassette (ABC) transporter complex, substrate-binding subunit-containing / phosphatidylinositol-4,5-bisphosphate binding / phosphatidylinositol binding / ATP-binding cassette (ABC) transporter complex / B cell differentiation / thymus development / cell chemotaxis / RING-type E3 ubiquitin transferase / ubiquitin-protein transferase activity / ubiquitin protein ligase activity / T cell differentiation in thymus / outer membrane-bounded periplasmic space / chromatin organization / endonuclease activity / histone binding / sequence-specific DNA binding / Hydrolases; Acting on ester bonds / adaptive immune response / periplasmic space / hydrolase activity / DNA damage response / chromatin binding / magnesium ion binding / protein homodimerization activity / zinc ion binding / membrane / metal ion binding / nucleus Similarity search - Function | |||||||||
| Biological species |  | |||||||||
| Method | single particle reconstruction / cryo EM / Resolution: 3.4 Å | |||||||||
 Authors Authors | Wu H / Liao M | |||||||||
| Funding support |  United States, 1 items United States, 1 items
| |||||||||
 Citation Citation |  Journal: Nat Struct Mol Biol / Year: 2018 Journal: Nat Struct Mol Biol / Year: 2018Title: DNA melting initiates the RAG catalytic pathway. Authors: Heng Ru / Wei Mi / Pengfei Zhang / Frederick W Alt / David G Schatz / Maofu Liao / Hao Wu /  Abstract: The mechanism for initiating DNA cleavage by DDE-family enzymes, including the RAG endonuclease, which initiates V(D)J recombination, is not well understood. Here we report six cryo-EM structures of ...The mechanism for initiating DNA cleavage by DDE-family enzymes, including the RAG endonuclease, which initiates V(D)J recombination, is not well understood. Here we report six cryo-EM structures of zebrafish RAG in complex with one or two intact recombination signal sequences (RSSs), at up to 3.9-Å resolution. Unexpectedly, these structures reveal DNA melting at the heptamer of the RSSs, thus resulting in a corkscrew-like rotation of coding-flank DNA and the positioning of the scissile phosphate in the active site. Substrate binding is associated with dimer opening and a piston-like movement in RAG1, first outward to accommodate unmelted DNA and then inward to wedge melted DNA. These precleavage complexes show limited base-specific contacts of RAG at the conserved terminal CAC/GTG sequence of the heptamer, thus suggesting conservation based on a propensity to unwind. CA and TG overwhelmingly dominate terminal sequences in transposons and retrotransposons, thereby implicating a universal mechanism for DNA melting during the initiation of retroviral integration and DNA transposition. | |||||||||
| History |
|
- Structure visualization
Structure visualization
| Movie |
 Movie viewer Movie viewer |
|---|---|
| Structure viewer | EM map:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| Supplemental images |
- Downloads & links
Downloads & links
-EMDB archive
| Map data |  emd_7843.map.gz emd_7843.map.gz | 59.9 MB |  EMDB map data format EMDB map data format | |
|---|---|---|---|---|
| Header (meta data) |  emd-7843-v30.xml emd-7843-v30.xml emd-7843.xml emd-7843.xml | 20.4 KB 20.4 KB | Display Display |  EMDB header EMDB header |
| Images |  emd_7843.png emd_7843.png | 68.5 KB | ||
| Filedesc metadata |  emd-7843.cif.gz emd-7843.cif.gz | 7.1 KB | ||
| Archive directory |  http://ftp.pdbj.org/pub/emdb/structures/EMD-7843 http://ftp.pdbj.org/pub/emdb/structures/EMD-7843 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7843 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7843 | HTTPS FTP |
-Related structure data
| Related structure data |  6dbiMC  7844C  7845C  7846C  7847C  7848C  7849C  7850C  7851C  7852C  7853C  6dbjC  6dblC  6dboC  6dbqC  6dbrC  6dbtC  6dbuC  6dbvC  6dbwC  6dbxC C: citing same article ( M: atomic model generated by this map |
|---|---|
| Similar structure data |
- Links
Links
| EMDB pages |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| Related items in Molecule of the Month |
- Map
Map
| File |  Download / File: emd_7843.map.gz / Format: CCP4 / Size: 64 MB / Type: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) Download / File: emd_7843.map.gz / Format: CCP4 / Size: 64 MB / Type: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Annotation | RAG in complex with 12-RSS and 23-RSS nicked DNA intermediates, sharpened map with B factor -91 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Projections & slices | Image control
Images are generated by Spider. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Voxel size | X=Y=Z: 1.06 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
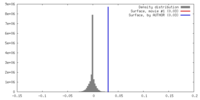
| Density |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symmetry | Space group: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Details | EMDB XML:
CCP4 map header:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-Supplemental data
- Sample components
Sample components
+Entire : RAG in complex with 12-RSS and 23-RSS nicked DNA intermediates
+Supramolecule #1: RAG in complex with 12-RSS and 23-RSS nicked DNA intermediates
+Macromolecule #1: Recombination activating gene 1 - MBP chimera
+Macromolecule #2: Recombination activating gene 2
+Macromolecule #3: Forward strand of 12-RSS signal end
+Macromolecule #4: Reverse strand of 12-RSS
+Macromolecule #5: Reverse strand of 23-RSS
+Macromolecule #6: Forward strand of 23-RSS signal end
+Macromolecule #7: Forward strand of coding flank
+Macromolecule #8: ZINC ION
+Macromolecule #9: CALCIUM ION
-Experimental details
-Structure determination
| Method | cryo EM |
|---|---|
 Processing Processing | single particle reconstruction |
| Aggregation state | particle |
- Sample preparation
Sample preparation
| Concentration | 0.38 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Buffer | pH: 7.5 Component:
Details: Solutions were made fresh from concentrated to avoid microbial contamination. | |||||||||||||||
| Vitrification | Cryogen name: ETHANE | |||||||||||||||
| Details | This sample was monodisperse. |
- Electron microscopy
Electron microscopy
| Microscope | FEI TITAN KRIOS |
|---|---|
| Image recording | Film or detector model: GATAN K2 SUMMIT (4k x 4k) / Average electron dose: 40.0 e/Å2 |
| Electron beam | Acceleration voltage: 300 kV / Electron source:  FIELD EMISSION GUN FIELD EMISSION GUN |
| Electron optics | Illumination mode: FLOOD BEAM / Imaging mode: BRIGHT FIELD |
| Experimental equipment |  Model: Titan Krios / Image courtesy: FEI Company |
- Image processing
Image processing
| Startup model | Type of model: NONE |
|---|---|
| Final reconstruction | Applied symmetry - Point group: C1 (asymmetric) / Resolution.type: BY AUTHOR / Resolution: 3.4 Å / Resolution method: FSC 0.143 CUT-OFF / Number images used: 53109 |
| Initial angle assignment | Type: PROJECTION MATCHING |
| Final angle assignment | Type: PROJECTION MATCHING |
 Movie
Movie Controller
Controller
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)