+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1mhs | ||||||
|---|---|---|---|---|---|---|---|
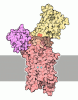
| タイトル | Model of Neurospora crassa proton ATPase | ||||||
 要素 要素 | Plasma Membrane ATPase | ||||||
 キーワード キーワード |  MEMBRANE PROTEIN (膜タンパク質) / MEMBRANE PROTEIN (膜タンパク質) /  PROTON TRANSPORT (プロトンポンプ) / PROTON TRANSPORT (プロトンポンプ) /  ion transport / ion transport /  proton pump (プロトンポンプ) / proton pump (プロトンポンプ) /  P-type ATPase / P-type ATPase /  active transport (能動輸送) active transport (能動輸送) | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報P-type H+-exporting transporter / proton export across plasma membrane / P-type proton-exporting transporter activity / proton transmembrane transport /  regulation of intracellular pH / membrane => GO:0016020 / regulation of intracellular pH / membrane => GO:0016020 /  ATP hydrolysis activity / ATP hydrolysis activity /  ATP binding / ATP binding /  metal ion binding / metal ion binding /  細胞膜 細胞膜類似検索 - 分子機能 | ||||||
| 生物種 |   Neurospora crassa (アカパンカビ) Neurospora crassa (アカパンカビ) | ||||||
| 手法 |  電子線結晶学 / 電子線結晶学 /  クライオ電子顕微鏡法 / 解像度: 8 Å クライオ電子顕微鏡法 / 解像度: 8 Å | ||||||
 データ登録者 データ登録者 | Kuhlbrandt, W. | ||||||
 引用 引用 |  ジャーナル: Science / 年: 2002 ジャーナル: Science / 年: 2002タイトル: Structure, mechanism, and regulation of the Neurospora plasma membrane H+-ATPase. 著者: Werner Kühlbrandt / Johan Zeelen / Jens Dietrich /  要旨: Proton pumps in the plasma membrane of plants and yeasts maintain the intracellular pH and membrane potential. To gain insight into the molecular mechanisms of proton pumping, we built an atomic ...Proton pumps in the plasma membrane of plants and yeasts maintain the intracellular pH and membrane potential. To gain insight into the molecular mechanisms of proton pumping, we built an atomic homology model of the proton pump based on the 2.6 angstrom x-ray structure of the related Ca2+ pump from rabbit sarcoplasmic reticulum. The model, when fitted to an 8 angstrom map of the Neurospora proton pump determined by electron microscopy, reveals the likely path of the proton through the membrane and shows that the nucleotide-binding domain rotates by approximately 70 degrees to deliver adenosine triphosphate (ATP) to the phosphorylation site. A synthetic peptide corresponding to the carboxyl-terminal regulatory domain stimulates ATPase activity, suggesting a mechanism for proton transport regulation. #1:  ジャーナル: Nature / 年: 1998 ジャーナル: Nature / 年: 1998タイトル: Three-dimensional map of the plasma membrane H+-ATPase in the open conformation 著者: AUER, M. / SCARBOROUGH, G.A. / KUHLBRANDT, W. | ||||||
| 履歴 |
| ||||||
| Remark 295 | NON-CRYSTALLOGRAPHIC SYMMETRY THE TRANSFORMATIONS PRESENTED ON THE MTRIX RECORDS BELOW DESCRIBE ... NON-CRYSTALLOGRAPHIC SYMMETRY THE TRANSFORMATIONS PRESENTED ON THE MTRIX RECORDS BELOW DESCRIBE NON-CRYSTALLOGRAPHIC RELATIONSHIPS AMONG ATOMS IN THIS ENTRY. APPLYING THE APPROPRIATE MTRIX TRANSFORMATION TO THE RESIDUES LISTED FIRST WILL YIELD APPROXIMATE COORDINATES FOR THE RESIDUES LISTED SECOND. CHAIN IDENTIFIERS GIVEN AS "?" REFER TO CHAINS FOR WHICH ATOMS ARE NOT FOUND IN THE ENTRY. APPLIED TO TRANSFORMED TO TRANSFORM CHAIN RESIDUES CHAIN RESIDUES RMSD SSS M 1 A 1 .. 920 B 1 .. 920 ? WHERE SSS -> COLUMNS 8-10 OF MTRIX RECORDS | ||||||
| Remark 300 | BIOMOLECULE: 1 THIS ENTRY CONTAINS A PORTION OF THE BIOLOGICALLY SIGNIFICANT MULTIMER. SEE REMARK ...BIOMOLECULE: 1 THIS ENTRY CONTAINS A PORTION OF THE BIOLOGICALLY SIGNIFICANT MULTIMER. SEE REMARK 350 FOR INFORMATION ON GENERATING THE BIOLOGICAL MOLECULE(S) ASSEMBLY COMPONENTS COM_ID: 1 NAME:PLASMA MEMBRANE PROTON ATPASE HEXAMERIC ASSEMBLY |
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1mhs.cif.gz 1mhs.cif.gz | 317.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1mhs.ent.gz pdb1mhs.ent.gz | 249.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1mhs.json.gz 1mhs.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/mh/1mhs https://data.pdbj.org/pub/pdb/validation_reports/mh/1mhs ftp://data.pdbj.org/pub/pdb/validation_reports/mh/1mhs ftp://data.pdbj.org/pub/pdb/validation_reports/mh/1mhs | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
| ||||||||
| 非結晶学的対称性 (NCS) | NCS oper: (Code: given / Matrix: (0.5, 0.866), : : |
- 要素
要素
| #1: タンパク質 | 分子量: 99984.359 Da / 分子数: 2 / 由来タイプ: 天然 詳細: isolated from plasma membrane of cultured Neurospora cells 由来: (天然)   Neurospora crassa (アカパンカビ) / 株: FGSC 4761 / 参照: UniProt: P07038, EC: 3.6.3.6 Neurospora crassa (アカパンカビ) / 株: FGSC 4761 / 参照: UniProt: P07038, EC: 3.6.3.6 |
|---|
-実験情報
-実験
| 実験 | 手法:  電子線結晶学 電子線結晶学 |
|---|---|
| EM実験 | 試料の集合状態: 2D ARRAY / 3次元再構成法:  電子線結晶学 電子線結晶学 |
- 試料調製
試料調製
| 構成要素 |
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | 名称: 100 mM ammonium sulphate, Tris-HCl, 30% glycerol, 10.5% PEG 4000 pH: 6.8 詳細: 100 mM ammonium sulphate, Tris-HCl, 30% glycerol, 10.5% PEG 4000 | |||||||||||||||
| 試料 | 濃度: 1 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES | |||||||||||||||
| 試料支持 | 詳細: hydrophobic carbon support film on 400 mesh gold-plated Cu EM grid | |||||||||||||||
急速凍結 | 詳細: 2D crystals were vitrified by immersion in liquid nitrogen | |||||||||||||||
結晶化 | *PLUS 手法: その他 / 詳細: MRC ELECTRON CRYSTALLOGRAPHY |
-データ収集
| 顕微鏡 | モデル: JEOL 3000SFF 詳細: Images were also recorded on JEOL 2000 EX and Philips CM200 FEG electron microscopes at 80 K at a dose of 1000 e/nm**2 |
|---|---|
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 倍率(公称値): 50000 X / 倍率(補正後): 50000 X / 最大 デフォーカス(公称値): 1200 nm / 最小 デフォーカス(公称値): 600 nm / Cs Bright-field microscopy / 倍率(公称値): 50000 X / 倍率(補正後): 50000 X / 最大 デフォーカス(公称値): 1200 nm / 最小 デフォーカス(公称値): 600 nm / Cs : 1.6 mm : 1.6 mm |
| 試料ホルダ | 温度: 4 K / 傾斜角・最大: 60 ° / 傾斜角・最小: 0 ° |
| 撮影 | 電子線照射量: 25 e/Å2 / フィルム・検出器のモデル: KODAK SO-163 FILM |
| 画像スキャン | デジタル画像の数: 60 |
| 放射 | 散乱光タイプ: electron |
| 放射波長 | 相対比: 1 |
- 解析
解析
| EMソフトウェア | 名称: MRC / カテゴリ: 3次元再構成 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | 詳細: crystallographic | ||||||||||||
3次元再構成 | 解像度: 8 Å / ピクセルサイズ(公称値): 1.4 Å / ピクセルサイズ(実測値): 1.4 Å / 倍率補正: electron diffraction of standard specimen / 対称性のタイプ: 2D CRYSTAL | ||||||||||||
| 原子モデル構築 | プロトコル: OTHER / 空間: REAL / Target criteria: best visual fit using the program o / 詳細: METHOD--manual REFINEMENT PROTOCOL--manual fit | ||||||||||||
| 原子モデル構築 | 詳細: this entry | ||||||||||||
| 精密化 | 最高解像度: 8 Å | ||||||||||||
| 精密化ステップ | サイクル: LAST / 最高解像度: 8 Å
|
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj