+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8476 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
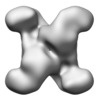
| タイトル | human CTP synthase 1 - mutant H355A | |||||||||
 マップデータ マップデータ | human CTP synthase 1 - mutant H355A | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 cytoophidium / CTP synthase (glutamine hydrolysing) / cytoophidium / CTP synthase (glutamine hydrolysing) /  CTP synthase activity / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / Interconversion of nucleotide di- and triphosphates / CTP biosynthetic process / nucleobase-containing compound metabolic process / glutamine metabolic process / B cell proliferation ... CTP synthase activity / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / Interconversion of nucleotide di- and triphosphates / CTP biosynthetic process / nucleobase-containing compound metabolic process / glutamine metabolic process / B cell proliferation ... cytoophidium / CTP synthase (glutamine hydrolysing) / cytoophidium / CTP synthase (glutamine hydrolysing) /  CTP synthase activity / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / Interconversion of nucleotide di- and triphosphates / CTP biosynthetic process / nucleobase-containing compound metabolic process / glutamine metabolic process / B cell proliferation / T cell proliferation / response to xenobiotic stimulus / CTP synthase activity / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / Interconversion of nucleotide di- and triphosphates / CTP biosynthetic process / nucleobase-containing compound metabolic process / glutamine metabolic process / B cell proliferation / T cell proliferation / response to xenobiotic stimulus /  ATP binding / ATP binding /  生体膜 / identical protein binding / 生体膜 / identical protein binding /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  ネガティブ染色法 / 解像度: 17.0 Å ネガティブ染色法 / 解像度: 17.0 Å | |||||||||
 データ登録者 データ登録者 | Lynch EM / Kollman JM | |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2017 ジャーナル: Nat Struct Mol Biol / 年: 2017タイトル: Human CTP synthase filament structure reveals the active enzyme conformation. 著者: Eric M Lynch / Derrick R Hicks / Matthew Shepherd / James A Endrizzi / Allison Maker / Jesse M Hansen / Rachael M Barry / Zemer Gitai / Enoch P Baldwin / Justin M Kollman /   要旨: The universally conserved enzyme CTP synthase (CTPS) forms filaments in bacteria and eukaryotes. In bacteria, polymerization inhibits CTPS activity and is required for nucleotide homeostasis. Here we ...The universally conserved enzyme CTP synthase (CTPS) forms filaments in bacteria and eukaryotes. In bacteria, polymerization inhibits CTPS activity and is required for nucleotide homeostasis. Here we show that for human CTPS, polymerization increases catalytic activity. The cryo-EM structures of bacterial and human CTPS filaments differ considerably in overall architecture and in the conformation of the CTPS protomer, explaining the divergent consequences of polymerization on activity. The structure of human CTPS filament, the first structure of the full-length human enzyme, reveals a novel active conformation. The filament structures elucidate allosteric mechanisms of assembly and regulation that rely on a conserved conformational equilibrium. The findings may provide a mechanism for increasing human CTPS activity in response to metabolic state and challenge the assumption that metabolic filaments are generally storage forms of inactive enzymes. Allosteric regulation of CTPS polymerization by ligands likely represents a fundamental mechanism underlying assembly of other metabolic filaments. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8476.map.gz emd_8476.map.gz | 5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8476-v30.xml emd-8476-v30.xml emd-8476.xml emd-8476.xml | 10.4 KB 10.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8476.png emd_8476.png | 55 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8476 http://ftp.pdbj.org/pub/emdb/structures/EMD-8476 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8476 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8476 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8476.map.gz / 形式: CCP4 / 大きさ: 5.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8476.map.gz / 形式: CCP4 / 大きさ: 5.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | human CTP synthase 1 - mutant H355A | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.07 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : hCTPS1-H355A tetramer
| 全体 | 名称: hCTPS1-H355A tetramer |
|---|---|
| 要素 |
|
-超分子 #1: hCTPS1-H355A tetramer
| 超分子 | 名称: hCTPS1-H355A tetramer / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:   Saccharomyces cerevisiae (パン酵母) / 組換プラスミド: pDO105-hCTPS1-H355A Saccharomyces cerevisiae (パン酵母) / 組換プラスミド: pDO105-hCTPS1-H355A |
-分子 #1: hCTPS1-H355A
| 分子 | 名称: hCTPS1-H355A / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:   Saccharomyces cerevisiae (パン酵母) Saccharomyces cerevisiae (パン酵母) |
| 配列 | 文字列: MKYILVTGGV ISGIGKGIIA SSVGTILKSC GLHVTSIKID PYINIDAGTF SPYEHGEVFV LDDGGEVDL DLGNYERFLD IRLTKDNNLT TGKIYQYVIN KERKGDYLGK TVQVVPHITD A IQEWVMRQ ALIPVDEDGL EPQVCVIELG GTVGDIESMP FIEAFRQFQF ...文字列: MKYILVTGGV ISGIGKGIIA SSVGTILKSC GLHVTSIKID PYINIDAGTF SPYEHGEVFV LDDGGEVDL DLGNYERFLD IRLTKDNNLT TGKIYQYVIN KERKGDYLGK TVQVVPHITD A IQEWVMRQ ALIPVDEDGL EPQVCVIELG GTVGDIESMP FIEAFRQFQF KVKRENFCNI HV SLVPQPS STGEQKTKPT QNSVRELRGL GLSPDLVVCR CSNPLDTSVK EKISMFCHVE PEQ VICVHD VSSIYRVPLL LEEQGVVDYF LRRLDLPIER QPRKMLMKWK EMADRYDRLL ETCS IALVG KYTKFSDSYA SVIKALEHSA LAINHKLEIK YIDSADLEPI TSQEEPVRYA EAWQK LCSA HGVLVPGGFG VRGTEGKIQA IAWARNQKKP FLGVCLGMQL AVVEFSRNVL GWQDAN STE FDPTTSHPVV VDMPEHNPGQ MGGTMRLGKR RTLFQTKNSV MRKLYGDADY LEERHRH RF EVNPVWKKCL EEQGLKFVGQ DVEGERMEIV ELEDHPFFVG VQYHPEFLSR PIKPSPPY F GLLLASVGRL SHYLQKGCRL SPRDTYSDRS GSSSPDSEIT ELKFPSINHD |
-実験情報
-構造解析
| 手法 |  ネガティブ染色法 ネガティブ染色法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.9 |
|---|---|
| 染色 | タイプ: NEGATIVE / 材質: Uranyl Formate |
| 詳細 | 20 mM Tris-HCl, pH 7.9, 2 mM UTP, 2 mM ATP, 0.2 mM GTP |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI SPIRIT |
|---|---|
| 電子線 | 加速電圧: 120 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: OTHER / 撮影モード: BRIGHT FIELD Bright-field microscopy Bright-field microscopy |
| 撮影 | フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 平均電子線量: 40.0 e/Å2 |
| 実験機器 |  モデル: Tecnai Spirit / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | ソフトウェア - 名称: CTFFIND |
|---|---|
| 初期 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: RELION |
| 最終 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: RELION |
| 最終 再構成 | 想定した対称性 - 点群: D2 (2回x2回 2面回転対称 ) )解像度のタイプ: BY AUTHOR / 解像度: 17.0 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: RELION / 使用した粒子像数: 4413 |
 ムービー
ムービー コントローラー
コントローラー