+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 9arg | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
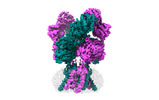
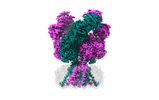
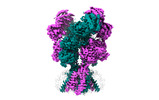
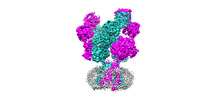
| タイトル | Rat GluN1-GluN2B NMDA receptor channel in apo conformation | |||||||||
 要素 要素 |
| |||||||||
 キーワード キーワード | MEMBRANE PROTEIN / Ligand-gated ion channel / ionotropic glutamate receptor / synaptic membrane protein | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報neurotransmitter receptor activity involved in regulation of postsynaptic membrane potential / cellular response to curcumin / cellular response to corticosterone stimulus / cellular response to magnesium starvation / regulation of postsynaptic cytosolic calcium ion concentration / sensory organ development / sensitization / pons maturation / regulation of cell communication / positive regulation of Schwann cell migration ...neurotransmitter receptor activity involved in regulation of postsynaptic membrane potential / cellular response to curcumin / cellular response to corticosterone stimulus / cellular response to magnesium starvation / regulation of postsynaptic cytosolic calcium ion concentration / sensory organ development / sensitization / pons maturation / regulation of cell communication / positive regulation of Schwann cell migration / EPHB-mediated forward signaling / neurotransmitter receptor activity involved in regulation of postsynaptic cytosolic calcium ion concentration / response to hydrogen sulfide / Assembly and cell surface presentation of NMDA receptors / olfactory learning / regulation of protein kinase A signaling / conditioned taste aversion / dendritic branch / response to other organism / regulation of respiratory gaseous exchange / protein localization to postsynaptic membrane / positive regulation of inhibitory postsynaptic potential / apical dendrite / propylene metabolic process / response to glycine / regulation of ARF protein signal transduction / fear response / response to methylmercury / positive regulation of cysteine-type endopeptidase activity / voltage-gated monoatomic cation channel activity / cellular response to dsRNA / response to carbohydrate / negative regulation of dendritic spine maintenance / regulation of monoatomic cation transmembrane transport / interleukin-1 receptor binding / cellular response to lipid / NMDA glutamate receptor activity / response to morphine / positive regulation of glutamate secretion / response to growth hormone / Synaptic adhesion-like molecules / NMDA selective glutamate receptor complex / RAF/MAP kinase cascade / parallel fiber to Purkinje cell synapse / response to manganese ion / NMDA selective glutamate receptor signaling pathway / calcium ion transmembrane import into cytosol / glutamate binding / neuromuscular process / positive regulation of reactive oxygen species biosynthetic process / protein heterotetramerization / regulation of synapse assembly / glycine binding / positive regulation of calcium ion transport into cytosol / regulation of axonogenesis / regulation of dendrite morphogenesis / male mating behavior / heterocyclic compound binding / suckling behavior / receptor clustering / startle response / behavioral response to pain / response to amine / small molecule binding / regulation of neuronal synaptic plasticity / action potential / monoatomic cation transmembrane transport / monoatomic cation transport / associative learning / positive regulation of excitatory postsynaptic potential / regulation of MAPK cascade / response to magnesium ion / social behavior / ligand-gated monoatomic ion channel activity / cellular response to organic cyclic compound / excitatory synapse / extracellularly glutamate-gated ion channel activity / cellular response to glycine / positive regulation of dendritic spine maintenance / behavioral fear response / neuron development / regulation of postsynaptic membrane potential / Unblocking of NMDA receptors, glutamate binding and activation / phosphatase binding / postsynaptic density, intracellular component / cellular response to manganese ion / glutamate receptor binding / D2 dopamine receptor binding / multicellular organismal response to stress / long-term memory / positive regulation of synaptic transmission, glutamatergic / prepulse inhibition / monoatomic cation channel activity / detection of mechanical stimulus involved in sensory perception of pain / calcium ion homeostasis / regulation of neuron apoptotic process / synaptic cleft / response to electrical stimulus / response to mechanical stimulus / glutamate-gated receptor activity 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.05 Å | |||||||||
 データ登録者 データ登録者 | Chou, T.-H. / Furukawa, H. | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2024 ジャーナル: Nature / 年: 2024タイトル: Molecular mechanism of ligand gating and opening of NMDA receptor. 著者: Tsung-Han Chou / Max Epstein / Russell G Fritzemeier / Nicholas S Akins / Srinu Paladugu / Elijah Z Ullman / Dennis C Liotta / Stephen F Traynelis / Hiro Furukawa /  要旨: Glutamate transmission and activation of ionotropic glutamate receptors are the fundamental means by which neurons control their excitability and neuroplasticity. The N-methyl-D-aspartate receptor ...Glutamate transmission and activation of ionotropic glutamate receptors are the fundamental means by which neurons control their excitability and neuroplasticity. The N-methyl-D-aspartate receptor (NMDAR) is unique among all ligand-gated channels, requiring two ligands-glutamate and glycine-for activation. These receptors function as heterotetrameric ion channels, with the channel opening dependent on the simultaneous binding of glycine and glutamate to the extracellular ligand-binding domains (LBDs) of the GluN1 and GluN2 subunits, respectively. The exact molecular mechanism for channel gating by the two ligands has been unclear, particularly without structures representing the open channel and apo states. Here we show that the channel gate opening requires tension in the linker connecting the LBD and transmembrane domain (TMD) and rotation of the extracellular domain relative to the TMD. Using electron cryomicroscopy, we captured the structure of the GluN1-GluN2B (GluN1-2B) NMDAR in its open state bound to a positive allosteric modulator. This process rotates and bends the pore-forming helices in GluN1 and GluN2B, altering the symmetry of the TMD channel from pseudofourfold to twofold. Structures of GluN1-2B NMDAR in apo and single-liganded states showed that binding of either glycine or glutamate alone leads to distinct GluN1-2B dimer arrangements but insufficient tension in the LBD-TMD linker for channel opening. This mechanistic framework identifies a key determinant for channel gating and a potential pharmacological strategy for modulating NMDAR activity. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  9arg.cif.gz 9arg.cif.gz | 514.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb9arg.ent.gz pdb9arg.ent.gz | 393 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  9arg.json.gz 9arg.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ar/9arg https://data.pdbj.org/pub/pdb/validation_reports/ar/9arg ftp://data.pdbj.org/pub/pdb/validation_reports/ar/9arg ftp://data.pdbj.org/pub/pdb/validation_reports/ar/9arg | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  43781MC  9areC  9arfC  9arhC  9ariC  9bibC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 95225.883 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  発現宿主:  参照: UniProt: P35439 #2: タンパク質 | 分子量: 98888.945 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  発現宿主:  参照: UniProt: Q00960 |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Di-heterotetrameric GluN1-GluN2B NMDA receptors / タイプ: COMPLEX / Entity ID: all / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.400 MDa / 実験値: NO |
| 由来(天然) | 生物種:  |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.5 |
| 試料 | 濃度: 4 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | グリッドのタイプ: Quantifoil R1.2/1.3 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 85 % / 凍結前の試料温度: 285 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2800 nm / 最小 デフォーカス(公称値): 1400 nm |
| 撮影 | 電子線照射量: 66.3 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) |
- 解析
解析
| EMソフトウェア |
| |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: NONE | |||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 4.05 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 60195 / 対称性のタイプ: POINT | |||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: BACKBONE TRACE | |||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 7SAA Accession code: 7SAA / Source name: PDB / タイプ: experimental model | |||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー




 PDBj
PDBj




