[English] 日本語
 Yorodumi
Yorodumi- PDB-6vhx: Klebsiella oxytoca NpsA N-terminal subdomain in complex with 3-hy... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 6vhx | ||||||
|---|---|---|---|---|---|---|---|
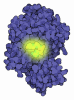
| Title | Klebsiella oxytoca NpsA N-terminal subdomain in complex with 3-hydroxyanthranilyl-AMSN | ||||||
 Components Components | NpsA Adenylation Domain | ||||||
 Keywords Keywords | BIOSYNTHETIC PROTEIN / adenylation / tilivalline / tilimycin / NRPS / nonribosomal peptide synthetase | ||||||
| Function / homology |  Function and homology information Function and homology information | ||||||
| Biological species |  Klebsiella oxytoca (bacteria) Klebsiella oxytoca (bacteria) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.7 Å MOLECULAR REPLACEMENT / Resolution: 1.7 Å | ||||||
 Authors Authors | Kreitler, D.F. / Gulick, A.M. | ||||||
| Funding support |  United States, 1items United States, 1items
| ||||||
 Citation Citation |  Journal: Acs Infect Dis. / Year: 2020 Journal: Acs Infect Dis. / Year: 2020Title: Biosynthesis, Mechanism of Action, and Inhibition of the Enterotoxin Tilimycin Produced by the Opportunistic PathogenKlebsiella oxytoca. Authors: Alexander, E.M. / Kreitler, D.F. / Guidolin, V. / Hurben, A.K. / Drake, E. / Villalta, P.W. / Balbo, S. / Gulick, A.M. / Aldrich, C.C. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  6vhx.cif.gz 6vhx.cif.gz | 354.4 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb6vhx.ent.gz pdb6vhx.ent.gz | 254.1 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  6vhx.json.gz 6vhx.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/vh/6vhx https://data.pdbj.org/pub/pdb/validation_reports/vh/6vhx ftp://data.pdbj.org/pub/pdb/validation_reports/vh/6vhx ftp://data.pdbj.org/pub/pdb/validation_reports/vh/6vhx | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  6vhtC  6vhuC  6vhvC  6vhwSC  6vhyC  6vhzC S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||||||
| 2 | 
| ||||||||||||
| 3 |
| ||||||||||||
| Unit cell |
|
- Components
Components
-Protein , 1 types, 2 molecules AB
| #1: Protein | Mass: 43960.355 Da / Num. of mol.: 2 / Mutation: E312A, E313A, Q314A Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Klebsiella oxytoca (bacteria) / Gene: NPSA / Plasmid: pET15 / Details (production host): N-term TEV tag / Production host: Klebsiella oxytoca (bacteria) / Gene: NPSA / Plasmid: pET15 / Details (production host): N-term TEV tag / Production host:  |
|---|
-Non-polymers , 6 types, 297 molecules 










| #2: Chemical | | #3: Chemical | ChemComp-BR / | #4: Chemical | ChemComp-CL / #5: Chemical | ChemComp-EPE / | #6: Chemical | ChemComp-PEG / | #7: Water | ChemComp-HOH / | |
|---|
-Details
| Has ligand of interest | Y |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.07 Å3/Da / Density % sol: 40.53 % / Description: 3D |
|---|---|
| Crystal grow | Temperature: 293 K / Method: vapor diffusion, hanging drop Details: well solution: 100 mM HEPES pH 7.5, 150 mM KBr, 30% w/v PEG3350 protein solution (15 mg/mL): 50 mM HEPES pH 8.0, 150 mM NaCl, 0.2 mM TCEP hanging drops: 1 uL protein solution, 1 uL well solution PH range: 7.5-8 |
-Data collection
| Diffraction | Mean temperature: 100 K / Serial crystal experiment: N |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  APS APS  / Beamline: 23-ID-D / Wavelength: 1.03322 Å / Beamline: 23-ID-D / Wavelength: 1.03322 Å |
| Detector | Type: DECTRIS PILATUS3 6M / Detector: PIXEL / Date: Mar 25, 2019 |
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 1.03322 Å / Relative weight: 1 |
| Reflection | Resolution: 1.7→60.79 Å / Num. obs: 73338 / % possible obs: 92.9 % / Redundancy: 6.6 % / Biso Wilson estimate: 25.07 Å2 / CC1/2: 0.999 / Rpim(I) all: 0.039 / Rrim(I) all: 0.101 / Rsym value: 0.093 / Net I/σ(I): 11.9 |
| Reflection shell | Resolution: 1.7→1.73 Å / Redundancy: 6.6 % / Mean I/σ(I) obs: 0.8 / Num. unique obs: 3912 / CC1/2: 0.366 / Rpim(I) all: 0.9 / Rrim(I) all: 2.322 / Rsym value: 2.137 / % possible all: 100 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: 6vhw Resolution: 1.7→60.79 Å / SU ML: 0.2219 / Cross valid method: FREE R-VALUE / σ(F): 1.34 / Phase error: 22.746
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 34.13 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.7→60.79 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller












 PDBj
PDBj