| Entry | Database: PDB / ID: 5elq
|
|---|
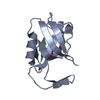
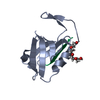
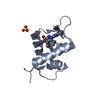
| Title | Crystal structure of the SNX27 PDZ domain bound to the C-terminal DGKzeta PDZ binding motif |
|---|
 Components Components | - GLU-ASP-GLN-GLU-THR-ALA-VAL
- Sorting nexin-27
|
|---|
 Keywords Keywords | PROTEIN TRANSPORT / Endosome / PDZ domain / sorting nexin |
|---|
| Function / homology |  Function and homology information Function and homology information
alkylglycerol kinase / alkylglycerol kinase activity / glycerolipid metabolic process / lipid phosphorylation / diacylglycerol metabolic process / postsynaptic early endosome / diacylglycerol kinase (ATP) / lipid kinase activity / ATP-dependent diacylglycerol kinase activity / establishment of protein localization to plasma membrane ...alkylglycerol kinase / alkylglycerol kinase activity / glycerolipid metabolic process / lipid phosphorylation / diacylglycerol metabolic process / postsynaptic early endosome / diacylglycerol kinase (ATP) / lipid kinase activity / ATP-dependent diacylglycerol kinase activity / establishment of protein localization to plasma membrane / phosphatidic acid biosynthetic process / positive regulation of AMPA glutamate receptor clustering / neurotransmitter receptor transport to plasma membrane / postsynaptic recycling endosome / WASH complex / Effects of PIP2 hydrolysis / retromer complex / response to methamphetamine hydrochloride / endosome to plasma membrane protein transport / phosphatidylinositol-3-phosphate binding / endocytic recycling / regulation of synapse maturation / endosomal transport / endosome to lysosome transport / immunological synapse / negative regulation of T cell receptor signaling pathway / regulation of postsynaptic membrane neurotransmitter receptor levels / mitotic G1 DNA damage checkpoint signaling / phosphatidylinositol binding / ionotropic glutamate receptor binding / cellular response to nerve growth factor stimulus / intracellular protein transport / platelet activation / Schaffer collateral - CA1 synapse / calcium-dependent protein binding / kinase activity / nervous system development / cell migration / lamellipodium / early endosome membrane / phospholipase C-activating G protein-coupled receptor signaling pathway / early endosome / endosome / nuclear speck / intracellular signal transduction / postsynapse / glutamatergic synapse / signal transduction / ATP binding / membrane / metal ion binding / nucleus / plasma membrane / cytoplasm / cytosolSimilarity search - Function : / : / Diacylglycerol kinase / Diacylglycerol kinase, accessory domain / Diacylglycerol kinase accessory domain / Diacylglycerol kinase accessory domain (presumed) / SNX27, atypical FERM-like domain / SNX27, PX domain / SNX27, RA domain / Diacylglycerol kinase, catalytic domain ...: / : / Diacylglycerol kinase / Diacylglycerol kinase, accessory domain / Diacylglycerol kinase accessory domain / Diacylglycerol kinase accessory domain (presumed) / SNX27, atypical FERM-like domain / SNX27, PX domain / SNX27, RA domain / Diacylglycerol kinase, catalytic domain / Diacylglycerol kinase catalytic domain / DAG-kinase catalytic (DAGKc) domain profile. / Diacylglycerol kinase catalytic domain (presumed) / Ras association (RalGDS/AF-6) domain / Ras-associating (RA) domain profile. / Ras-associating (RA) domain / NAD kinase/diacylglycerol kinase-like domain superfamily / Inorganic polyphosphate/ATP-NAD kinase, N-terminal / PhoX homologous domain, present in p47phox and p40phox. / PX domain profile. / PX domain / Phox homology / PX domain superfamily / Phorbol esters/diacylglycerol binding domain (C1 domain) / Protein kinase C conserved region 1 (C1) domains (Cysteine-rich domains) / Protein kinase C-like, phorbol ester/diacylglycerol-binding domain / PDZ domain / Pdz3 Domain / PDZ domain / PDZ domain profile. / Domain present in PSD-95, Dlg, and ZO-1/2. / PDZ domain / PDZ superfamily / Ankyrin repeat profile. / Ankyrin repeats (3 copies) / Ankyrin repeat region circular profile. / ankyrin repeats / Ankyrin repeat / Ankyrin repeat-containing domain superfamily / Roll / Ubiquitin-like domain superfamily / Mainly BetaSimilarity search - Domain/homology |
|---|
| Biological species |   Rattus norvegicus (Norway rat) Rattus norvegicus (Norway rat)
 Homo sapiens (human) Homo sapiens (human) |
|---|
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.1 Å MOLECULAR REPLACEMENT / Resolution: 1.1 Å |
|---|
 Authors Authors | Collins, B.M. / Clairfeuille, T. |
|---|
| Funding support |  Australia, 1items Australia, 1items | Organization | Grant number | Country |
|---|
| National Health and Medical Research Council (NHMRC, Australia) | APP1058734 |  Australia Australia |
|
|---|
 Citation Citation |  Journal: Nat.Struct.Mol.Biol. / Year: 2016 Journal: Nat.Struct.Mol.Biol. / Year: 2016
Title: A molecular code for endosomal recycling of phosphorylated cargos by the SNX27-retromer complex.
Authors: Clairfeuille, T. / Mas, C. / Chan, A.S. / Yang, Z. / Tello-Lafoz, M. / Chandra, M. / Widagdo, J. / Kerr, M.C. / Paul, B. / Merida, I. / Teasdale, R.D. / Pavlos, N.J. / Anggono, V. / Collins, B.M. |
|---|
| History | | Deposition | Nov 5, 2015 | Deposition site: RCSB / Processing site: RCSB |
|---|
| Revision 1.0 | Sep 7, 2016 | Provider: repository / Type: Initial release |
|---|
| Revision 1.1 | Sep 21, 2016 | Group: Database references |
|---|
| Revision 1.2 | Oct 19, 2016 | Group: Database references |
|---|
| Revision 1.3 | Sep 27, 2017 | Group: Author supporting evidence / Data collection / Derived calculations
Category: diffrn_source / pdbx_audit_support / pdbx_struct_oper_list
Item: _diffrn_source.pdbx_synchrotron_site / _pdbx_audit_support.funding_organization / _pdbx_struct_oper_list.symmetry_operation |
|---|
| Revision 1.4 | Jan 8, 2020 | Group: Author supporting evidence / Category: pdbx_audit_support / Item: _pdbx_audit_support.funding_organization |
|---|
| Revision 1.5 | Sep 27, 2023 | Group: Data collection / Database references / Refinement description
Category: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession |
|---|
|
|---|
 Yorodumi
Yorodumi Open data
Open data Basic information
Basic information Components
Components Keywords
Keywords Function and homology information
Function and homology information
 Homo sapiens (human)
Homo sapiens (human) X-RAY DIFFRACTION /
X-RAY DIFFRACTION /  SYNCHROTRON /
SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.1 Å
MOLECULAR REPLACEMENT / Resolution: 1.1 Å  Authors
Authors Australia, 1items
Australia, 1items  Citation
Citation Journal: Nat.Struct.Mol.Biol. / Year: 2016
Journal: Nat.Struct.Mol.Biol. / Year: 2016 Structure visualization
Structure visualization Molmil
Molmil Jmol/JSmol
Jmol/JSmol Downloads & links
Downloads & links Download
Download 5elq.cif.gz
5elq.cif.gz PDBx/mmCIF format
PDBx/mmCIF format pdb5elq.ent.gz
pdb5elq.ent.gz PDB format
PDB format 5elq.json.gz
5elq.json.gz PDBx/mmJSON format
PDBx/mmJSON format Other downloads
Other downloads https://data.pdbj.org/pub/pdb/validation_reports/el/5elq
https://data.pdbj.org/pub/pdb/validation_reports/el/5elq ftp://data.pdbj.org/pub/pdb/validation_reports/el/5elq
ftp://data.pdbj.org/pub/pdb/validation_reports/el/5elq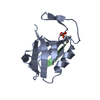


 Links
Links Assembly
Assembly

 Components
Components

 Homo sapiens (human) / References: UniProt: Q13574*PLUS
Homo sapiens (human) / References: UniProt: Q13574*PLUS X-RAY DIFFRACTION / Number of used crystals: 1
X-RAY DIFFRACTION / Number of used crystals: 1  Sample preparation
Sample preparation SYNCHROTRON / Site:
SYNCHROTRON / Site:  Australian Synchrotron
Australian Synchrotron  / Beamline: MX2 / Wavelength: 0.9537 Å
/ Beamline: MX2 / Wavelength: 0.9537 Å Processing
Processing MOLECULAR REPLACEMENT
MOLECULAR REPLACEMENT Movie
Movie Controller
Controller











 PDBj
PDBj




