+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4721 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of a truncated adenylyl cyclase bound to MANT-GTP, forskolin and an activatedstimulatory Galphas protein | |||||||||
 マップデータ マップデータ | Truncated AC9 (AC9-1250) bound to MANT-GTP, forskolin and GalphaS | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Adenylyl cyclase / G protein / MANT-GTP / forskolin / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Adenylate cyclase activating pathway / Adenylate cyclase inhibitory pathway / PKA activation / adenylate cyclase / Hedgehog 'off' state / sensory perception of chemical stimulus / mu-type opioid receptor binding / corticotropin-releasing hormone receptor 1 binding / cAMP biosynthetic process / adenylate cyclase activity ...Adenylate cyclase activating pathway / Adenylate cyclase inhibitory pathway / PKA activation / adenylate cyclase / Hedgehog 'off' state / sensory perception of chemical stimulus / mu-type opioid receptor binding / corticotropin-releasing hormone receptor 1 binding / cAMP biosynthetic process / adenylate cyclase activity / beta-2 adrenergic receptor binding / G alpha (z) signalling events / D1 dopamine receptor binding / adenylate cyclase-activating adrenergic receptor signaling pathway / insulin-like growth factor receptor binding / ionotropic glutamate receptor binding / adenylate cyclase activator activity / G-protein beta/gamma-subunit complex binding / adenylate cyclase-activating dopamine receptor signaling pathway / heterotrimeric G-protein complex / adenylate cyclase-activating G protein-coupled receptor signaling pathway / in utero embryonic development / 加水分解酵素; 酸無水物に作用; GTPに作用・細胞または細胞小器官の運動に関与 / intracellular signal transduction / ciliary basal body / GTPase activity / GTP binding / ATP binding / metal ion binding / plasma membrane / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
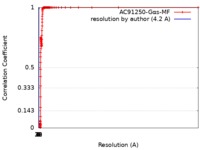
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | Qi C / Sorrentino S | |||||||||
| 資金援助 |  スイス, 1件 スイス, 1件
| |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2019 ジャーナル: Science / 年: 2019タイトル: The structure of a membrane adenylyl cyclase bound to an activated stimulatory G protein. 著者: Chao Qi / Simona Sorrentino / Ohad Medalia / Volodymyr M Korkhov /   要旨: Membrane-integral adenylyl cyclases (ACs) are key enzymes in mammalian heterotrimeric GTP-binding protein (G protein)-dependent signal transduction, which is important in many cellular processes. ...Membrane-integral adenylyl cyclases (ACs) are key enzymes in mammalian heterotrimeric GTP-binding protein (G protein)-dependent signal transduction, which is important in many cellular processes. Signals received by the G protein-coupled receptors are conveyed to ACs through G proteins to modulate the levels of cellular cyclic adenosine monophosphate (cAMP). Here, we describe the cryo-electron microscopy structure of the bovine membrane AC9 bound to an activated G protein αs subunit at 3.4-angstrom resolution. The structure reveals the organization of the membrane domain and helical domain that spans between the membrane and catalytic domains of AC9. The carboxyl-terminal extension of the catalytic domain occludes both the catalytic and the allosteric sites of AC9, inducing a conformation distinct from the substrate- and activator-bound state, suggesting a regulatory role in cAMP production. #1:  ジャーナル: To Be Published ジャーナル: To Be Publishedタイトル: The structure of a membrane adenylyl cyclase bound to an activated stimulatory G protein 著者: Qi C / Sorrentino S / Medalia O / Korkhov VM | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4721.map.gz emd_4721.map.gz | 226.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4721-v30.xml emd-4721-v30.xml emd-4721.xml emd-4721.xml | 18.1 KB 18.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_4721_fsc.xml emd_4721_fsc.xml | 6.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4721.png emd_4721.png | 67.4 KB | ||
| Filedesc metadata |  emd-4721.cif.gz emd-4721.cif.gz | 7.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4721 http://ftp.pdbj.org/pub/emdb/structures/EMD-4721 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4721 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4721 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4721.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4721.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Truncated AC9 (AC9-1250) bound to MANT-GTP, forskolin and GalphaS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.8544 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
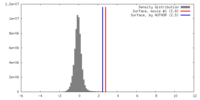
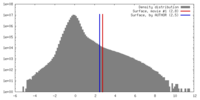
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Adenylyl cyclase AC9 (truncation, residues 1-1250) bound to MANT-...
+超分子 #1: Adenylyl cyclase AC9 (truncation, residues 1-1250) bound to MANT-...
+超分子 #2: Adenylyl cyclase AC9
+超分子 #3: GalphaS protein
+分子 #1: Adenylate cyclase 9
+分子 #2: Guanine nucleotide-binding protein G(s) subunit alpha isoforms short
+分子 #3: 3'-O-(N-METHYLANTHRANILOYL)-GUANOSINE-5'-TRIPHOSPHATE
+分子 #4: FORSKOLIN
+分子 #5: MANGANESE (II) ION
+分子 #6: 5'-GUANOSINE-DIPHOSPHATE-MONOTHIOPHOSPHATE
+分子 #7: MAGNESIUM ION
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 278 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 2 / 実像数: 10758 / 平均電子線量: 60.0 e/Å2 詳細: Two datasets were merged using two different microscopes, using pixel size of 0.831 A/pix (4453 micrographs; 60 e-/A2) and 0.8544 A/pix (6305 micrographs; 45 e-/A2). Final dataset was scaled to 0.8544 A/pix. |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL / 温度因子: 110.92 当てはまり具合の基準: Cross-correlation coefficient |
|---|---|
| 得られたモデル |  PDB-6r4o: |
 ムービー
ムービー コントローラー
コントローラー


























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)



















 Homo sapiens (ヒト)
Homo sapiens (ヒト) Trichoplusia ni (イラクサキンウワバ)
Trichoplusia ni (イラクサキンウワバ)