+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | 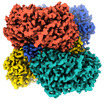 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
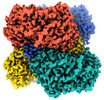
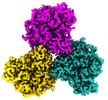
| タイトル | Aldehyde dehydrogenase 1 family member A1 from human liver | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | aldehyde dehydrogenase / human liver / OXIDOREDUCTASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報fructosamine catabolic process / 3-deoxyglucosone dehydrogenase activity / benzaldehyde dehydrogenase (NAD+) / benzaldehyde dehydrogenase (NAD+) activity / maintenance of lens transparency / gamma-aminobutyric acid biosynthetic process / retinal dehydrogenase / aminobutyraldehyde dehydrogenase / aminobutyraldehyde dehydrogenase (NAD+) activity / Fructose catabolism ...fructosamine catabolic process / 3-deoxyglucosone dehydrogenase activity / benzaldehyde dehydrogenase (NAD+) / benzaldehyde dehydrogenase (NAD+) activity / maintenance of lens transparency / gamma-aminobutyric acid biosynthetic process / retinal dehydrogenase / aminobutyraldehyde dehydrogenase / aminobutyraldehyde dehydrogenase (NAD+) activity / Fructose catabolism / Ethanol oxidation / cellular aldehyde metabolic process / RA biosynthesis pathway / glyceraldehyde-3-phosphate dehydrogenase (NAD+) (non-phosphorylating) activity / aldehyde dehydrogenase (NAD+) / cellular detoxification of aldehyde / androgen binding / aldehyde dehydrogenase (NAD+) activity / retinal dehydrogenase activity / negative regulation of cold-induced thermogenesis / retinol metabolic process / retinoid metabolic process / GTPase activator activity / NAD binding / axon / synapse / extracellular exosome / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
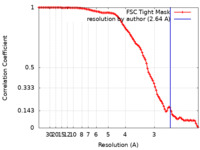
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.64 Å | |||||||||
 データ登録者 データ登録者 | Zhang Z | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell Rep / 年: 2023 ジャーナル: Cell Rep / 年: 2023タイトル: High-resolution structural-omics of human liver enzymes. 著者: Chih-Chia Su / Meinan Lyu / Zhemin Zhang / Masaru Miyagi / Wei Huang / Derek J Taylor / Edward W Yu /  要旨: We applied raw human liver microsome lysate to a holey carbon grid and used cryo-electron microscopy (cryo-EM) to define its composition. From this sample we identified and simultaneously determined ...We applied raw human liver microsome lysate to a holey carbon grid and used cryo-electron microscopy (cryo-EM) to define its composition. From this sample we identified and simultaneously determined high-resolution structural information for ten unique human liver enzymes involved in diverse cellular processes. Notably, we determined the structure of the endoplasmic bifunctional protein H6PD, where the N- and C-terminal domains independently possess glucose-6-phosphate dehydrogenase and 6-phosphogluconolactonase enzymatic activity, respectively. We also obtained the structure of heterodimeric human GANAB, an ER glycoprotein quality-control machinery that contains a catalytic α subunit and a noncatalytic β subunit. In addition, we observed a decameric peroxidase, PRDX4, which directly contacts a disulfide isomerase-related protein, ERp46. Structural data suggest that several glycosylations, bound endogenous compounds, and ions associate with these human liver enzymes. These results highlight the importance of cryo-EM in facilitating the elucidation of human organ proteomics at the atomic level. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_28271.map.gz emd_28271.map.gz | 97.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-28271-v30.xml emd-28271-v30.xml emd-28271.xml emd-28271.xml | 15.9 KB 15.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_28271_fsc.xml emd_28271_fsc.xml | 11.3 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_28271.png emd_28271.png | 224.6 KB | ||
| Filedesc metadata |  emd-28271.cif.gz emd-28271.cif.gz | 5.3 KB | ||
| その他 |  emd_28271_additional_1.map.gz emd_28271_additional_1.map.gz emd_28271_half_map_1.map.gz emd_28271_half_map_1.map.gz emd_28271_half_map_2.map.gz emd_28271_half_map_2.map.gz | 52 MB 95.3 MB 95.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-28271 http://ftp.pdbj.org/pub/emdb/structures/EMD-28271 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28271 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28271 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_28271_validation.pdf.gz emd_28271_validation.pdf.gz | 1006.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_28271_full_validation.pdf.gz emd_28271_full_validation.pdf.gz | 1006 KB | 表示 | |
| XML形式データ |  emd_28271_validation.xml.gz emd_28271_validation.xml.gz | 18.2 KB | 表示 | |
| CIF形式データ |  emd_28271_validation.cif.gz emd_28271_validation.cif.gz | 23.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28271 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28271 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28271 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28271 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8eneMC  7uzmC  8ekwC  8ekyC  8em2C  8emrC  8emsC  8emtC  8eojC  8eorC  23428 M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_28271.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_28271.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.08 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: #1
| ファイル | emd_28271_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
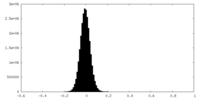
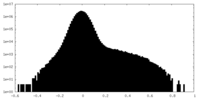
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_28271_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_28271_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Aldehyde dehydrogenase 1 family member A1
| 全体 | 名称: Aldehyde dehydrogenase 1 family member A1 |
|---|---|
| 要素 |
|
-超分子 #1: Aldehyde dehydrogenase 1 family member A1
| 超分子 | 名称: Aldehyde dehydrogenase 1 family member A1 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Retinal dehydrogenase 1
| 分子 | 名称: Retinal dehydrogenase 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO EC番号: 酸化還元酵素; アルデヒドまたはケトンに対し酸化酵素として働く; NAD又はNADPを用いる |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 54.924617 KDa |
| 配列 | 文字列: MSSSGTPDLP VLLTDLKIQY TKIFINNEWH DSVSGKKFPV FNPATEEELC QVEEGDKEDV DKAVKAARQA FQIGSPWRTM DASERGRLL YKLADLIERD RLLLATMESM NGGKLYSNAY LNDLAGCIKT LRYCAGWADK IQGRTIPIDG NFFTYTRHEP I GVCGQIIP ...文字列: MSSSGTPDLP VLLTDLKIQY TKIFINNEWH DSVSGKKFPV FNPATEEELC QVEEGDKEDV DKAVKAARQA FQIGSPWRTM DASERGRLL YKLADLIERD RLLLATMESM NGGKLYSNAY LNDLAGCIKT LRYCAGWADK IQGRTIPIDG NFFTYTRHEP I GVCGQIIP WNFPLVMLIW KIGPALSCGN TVVVKPAEQT PLTALHVASL IKEAGFPPGV VNIVPGYGPT AGAAISSHMD ID KVAFTGS TEVGKLIKEA AGKSNLKRVT LELGGKSPCI VLADADLDNA VEFAHHGVFY HQGQCCIAAS RIFVEESIYD EFV RRSVER AKKYILGNPL TPGVTQGPQI DKEQYDKILD LIESGKKEGA KLECGGGPWG NKGYFVQPTV FSNVTDEMRI AKEE IFGPV QQIMKFKSLD DVIKRANNTF YGLSAGVFTK DIDKAITISS ALQAGTVWVN CYGVVSAQCP FGGFKMSGNG RELGE YGFH EYTEVKTVTV KISQKNS UniProtKB: Aldehyde dehydrogenase 1A1 |
-分子 #2: NICOTINAMIDE-ADENINE-DINUCLEOTIDE
| 分子 | 名称: NICOTINAMIDE-ADENINE-DINUCLEOTIDE / タイプ: ligand / ID: 2 / コピー数: 4 / 式: NAD |
|---|---|
| 分子量 | 理論値: 663.425 Da |
| Chemical component information |  ChemComp-NAD: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 41.25 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 3.291 µm / 最小 デフォーカス(公称値): 0.17 µm / 倍率(公称値): 81000 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z
Z Y
Y X
X