| 登録情報 | データベース: PDB / ID: 3jyj
|
|---|
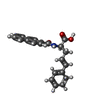
| タイトル | Structure-Based Design of Novel PIN1 Inhibitors (II) |
|---|
 要素 要素 | Peptidyl-prolyl cis-trans isomerase NIMA-interacting 1 |
|---|
 キーワード キーワード | ISOMERASE / SBDD / Small Molecule / PPIase / Cell cycle / Nucleus / Phosphoprotein / Rotamase |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
cis-trans isomerase activity / phosphothreonine residue binding / negative regulation of cell motility / negative regulation of brown fat cell differentiation / regulation of protein localization to nucleus / mitogen-activated protein kinase kinase binding / ubiquitin ligase activator activity / GTPase activating protein binding / : / protein peptidyl-prolyl isomerization ...cis-trans isomerase activity / phosphothreonine residue binding / negative regulation of cell motility / negative regulation of brown fat cell differentiation / regulation of protein localization to nucleus / mitogen-activated protein kinase kinase binding / ubiquitin ligase activator activity / GTPase activating protein binding / : / protein peptidyl-prolyl isomerization / regulation of mitotic nuclear division / negative regulation of SMAD protein signal transduction / PI5P Regulates TP53 Acetylation / negative regulation of amyloid-beta formation / cytoskeletal motor activity / phosphoserine residue binding / RHO GTPases Activate NADPH Oxidases / postsynaptic cytosol / Rho protein signal transduction / regulation of cytokinesis / peptidylprolyl isomerase / peptidyl-prolyl cis-trans isomerase activity / Negative regulators of DDX58/IFIH1 signaling / negative regulation of transforming growth factor beta receptor signaling pathway / regulation of protein stability / phosphoprotein binding / negative regulation of protein catabolic process / positive regulation of protein phosphorylation / negative regulation of ERK1 and ERK2 cascade / synapse organization / beta-catenin binding / protein destabilization / ISG15 antiviral mechanism / tau protein binding / neuron differentiation / positive regulation of canonical Wnt signaling pathway / regulation of gene expression / midbody / cellular response to hypoxia / Regulation of TP53 Activity through Phosphorylation / response to hypoxia / nuclear speck / protein stabilization / ciliary basal body / glutamatergic synapse / positive regulation of transcription by RNA polymerase II / nucleoplasm / nucleus / cytoplasm / cytosol類似検索 - 分子機能 : / Peptidyl-prolyl cis-trans isomerase, PpiC-type, conserved site / PpiC-type peptidyl-prolyl cis-trans isomerase signature. / PPIC-type PPIASE domain / PpiC-type peptidyl-prolyl cis-trans isomerase family profile. / Peptidyl-prolyl cis-trans isomerase, PpiC-type / Chitinase A; domain 3 - #40 / Chitinase A; domain 3 / WW domain / WW/rsp5/WWP domain signature. ...: / Peptidyl-prolyl cis-trans isomerase, PpiC-type, conserved site / PpiC-type peptidyl-prolyl cis-trans isomerase signature. / PPIC-type PPIASE domain / PpiC-type peptidyl-prolyl cis-trans isomerase family profile. / Peptidyl-prolyl cis-trans isomerase, PpiC-type / Chitinase A; domain 3 - #40 / Chitinase A; domain 3 / WW domain / WW/rsp5/WWP domain signature. / WW domain superfamily / WW/rsp5/WWP domain profile. / Domain with 2 conserved Trp (W) residues / WW domain / Peptidyl-prolyl cis-trans isomerase domain superfamily / Roll / Alpha Beta類似検索 - ドメイン・相同性 Chem-JZI / Peptidyl-prolyl cis-trans isomerase NIMA-interacting 1類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  フーリエ合成 / 解像度: 1.87 Å フーリエ合成 / 解像度: 1.87 Å |
|---|
 データ登録者 データ登録者 | Greasley, S.E. / Ferre, R.A. |
|---|
 引用 引用 |  ジャーナル: Bioorg.Med.Chem.Lett. / 年: 2010 ジャーナル: Bioorg.Med.Chem.Lett. / 年: 2010
タイトル: Structure-based design of novel human Pin1 inhibitors (II).
著者: Dong, L. / Marakovits, J. / Hou, X. / Guo, C. / Greasley, S. / Dagostino, E. / Ferre, R. / Johnson, M.C. / Kraynov, E. / Thomson, J. / Pathak, V. / Murray, B.W. |
|---|
| 履歴 | | 登録 | 2009年9月21日 | 登録サイト: RCSB / 処理サイト: RCSB |
|---|
| 改定 1.0 | 2010年4月7日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2011年7月13日 | Group: Version format compliance |
|---|
| 改定 1.2 | 2021年10月13日 | Group: Database references / Derived calculations / カテゴリ: database_2 / struct_ref_seq_dif / struct_site
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession ..._database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_ref_seq_dif.details / _struct_site.pdbx_auth_asym_id / _struct_site.pdbx_auth_comp_id / _struct_site.pdbx_auth_seq_id |
|---|
| 改定 1.3 | 2024年2月21日 | Group: Data collection / カテゴリ: chem_comp_atom / chem_comp_bond |
|---|
| 改定 1.4 | 2024年4月3日 | Group: Refinement description / カテゴリ: pdbx_initial_refinement_model |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  フーリエ合成 / 解像度: 1.87 Å
フーリエ合成 / 解像度: 1.87 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Bioorg.Med.Chem.Lett. / 年: 2010
ジャーナル: Bioorg.Med.Chem.Lett. / 年: 2010 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 3jyj.cif.gz
3jyj.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb3jyj.ent.gz
pdb3jyj.ent.gz PDB形式
PDB形式 3jyj.json.gz
3jyj.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード https://data.pdbj.org/pub/pdb/validation_reports/jy/3jyj
https://data.pdbj.org/pub/pdb/validation_reports/jy/3jyj ftp://data.pdbj.org/pub/pdb/validation_reports/jy/3jyj
ftp://data.pdbj.org/pub/pdb/validation_reports/jy/3jyj リンク
リンク 集合体
集合体


 要素
要素 Homo sapiens (ヒト) / 遺伝子: PIN1 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: PIN1 / 発現宿主: 
 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 回転陽極 / タイプ: RIGAKU RUH2R / 波長: 1.54 / 波長: 1.54 Å
回転陽極 / タイプ: RIGAKU RUH2R / 波長: 1.54 / 波長: 1.54 Å 解析
解析 フーリエ合成
フーリエ合成 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj