+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of human ATG9A in LMNG micelles | |||||||||
 マップデータ マップデータ | The autophagy relate transmembrane protein ATG9A, lipid scramblase | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Lipid scramblase / ATG9A / single particle cryo-EM / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報phospholipid scramblase activity / programmed necrotic cell death / protein localization to phagophore assembly site / phagophore assembly site membrane / piecemeal microautophagy of the nucleus / phagophore assembly site / bone morphogenesis / autophagy of mitochondrion / reticulophagy / Macroautophagy ...phospholipid scramblase activity / programmed necrotic cell death / protein localization to phagophore assembly site / phagophore assembly site membrane / piecemeal microautophagy of the nucleus / phagophore assembly site / bone morphogenesis / autophagy of mitochondrion / reticulophagy / Macroautophagy / autophagosome assembly / autophagosome / PINK1-PRKN Mediated Mitophagy / mitochondrial membrane / trans-Golgi network / recycling endosome / recycling endosome membrane / late endosome / late endosome membrane / endosome / Golgi membrane / intracellular membrane-bounded organelle / endoplasmic reticulum membrane / Golgi apparatus / mitochondrion / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
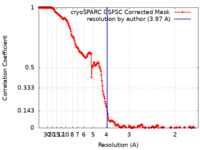
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.97 Å | |||||||||
 データ登録者 データ登録者 | Yang W / Goran S | |||||||||
| 資金援助 |  中国, 2件 中国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2024 ジャーナル: Nat Struct Mol Biol / 年: 2024タイトル: Structural basis for lipid transfer by the ATG2A-ATG9A complex. 著者: Yang Wang / Selma Dahmane / Rujuan Ti / Xinyi Mai / Lizhe Zhu / Lars-Anders Carlson / Goran Stjepanovic /   要旨: Autophagy is characterized by the formation of double-membrane vesicles called autophagosomes. Autophagy-related proteins (ATGs) 2A and 9A have an essential role in autophagy by mediating lipid ...Autophagy is characterized by the formation of double-membrane vesicles called autophagosomes. Autophagy-related proteins (ATGs) 2A and 9A have an essential role in autophagy by mediating lipid transfer and re-equilibration between membranes for autophagosome formation. Here we report the cryo-electron microscopy structures of human ATG2A in complex with WD-repeat protein interacting with phosphoinositides 4 (WIPI4) at 3.2 Å and the ATG2A-WIPI4-ATG9A complex at 7 Å global resolution. On the basis of molecular dynamics simulations, we propose a mechanism of lipid extraction from the donor membranes. Our analysis revealed 3:1 stoichiometry of the ATG9A-ATG2A complex, directly aligning the ATG9A lateral pore with ATG2A lipid transfer cavity, and an interaction of the ATG9A trimer with both the N-terminal and the C-terminal tip of rod-shaped ATG2A. Cryo-electron tomography of ATG2A liposome-binding states showed that ATG2A tethers lipid vesicles at different orientations. In summary, this study provides a molecular basis for the growth of the phagophore membrane and lends structural insights into spatially coupled lipid transport and re-equilibration during autophagosome formation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_37088.map.gz emd_37088.map.gz | 726.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-37088-v30.xml emd-37088-v30.xml emd-37088.xml emd-37088.xml | 14.2 KB 14.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_37088_fsc.xml emd_37088_fsc.xml | 20 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_37088.png emd_37088.png | 68.6 KB | ||
| Filedesc metadata |  emd-37088.cif.gz emd-37088.cif.gz | 5.8 KB | ||
| その他 |  emd_37088_half_map_1.map.gz emd_37088_half_map_1.map.gz emd_37088_half_map_2.map.gz emd_37088_half_map_2.map.gz | 764.8 MB 764.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-37088 http://ftp.pdbj.org/pub/emdb/structures/EMD-37088 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37088 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37088 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_37088_validation.pdf.gz emd_37088_validation.pdf.gz | 633.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_37088_full_validation.pdf.gz emd_37088_full_validation.pdf.gz | 633.2 KB | 表示 | |
| XML形式データ |  emd_37088_validation.xml.gz emd_37088_validation.xml.gz | 28.1 KB | 表示 | |
| CIF形式データ |  emd_37088_validation.cif.gz emd_37088_validation.cif.gz | 37.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37088 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37088 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37088 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37088 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_37088.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_37088.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | The autophagy relate transmembrane protein ATG9A, lipid scramblase | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ |
| ||||||||||||||||||||||||||||||||||||
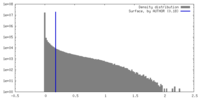
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map A of ATG9A
| ファイル | emd_37088_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A of ATG9A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
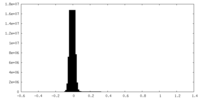
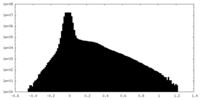
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : ATG9A trimer
| 全体 | 名称: ATG9A trimer |
|---|---|
| 要素 |
|
-超分子 #1: ATG9A trimer
| 超分子 | 名称: ATG9A trimer / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 283 KDa |
-分子 #1: Autophagy-related protein 9A
| 分子 | 名称: Autophagy-related protein 9A / タイプ: protein_or_peptide / ID: 1 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 94.551031 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MAQFDTEYQR LEASYSDSPP GEEDLLVHVA EGSKSPWHHI ENLDLFFSRV YNLHQKNGFT CMLIGEIFEL MQFLFVVAFT TFLVSCVDY DILFANKMVN HSLHPTEPVK VTLPDAFLPA QVCSARIQEN GSLITILVIA GVFWIHRLIK FIYNICCYWE I HSFYLHAL ...文字列: MAQFDTEYQR LEASYSDSPP GEEDLLVHVA EGSKSPWHHI ENLDLFFSRV YNLHQKNGFT CMLIGEIFEL MQFLFVVAFT TFLVSCVDY DILFANKMVN HSLHPTEPVK VTLPDAFLPA QVCSARIQEN GSLITILVIA GVFWIHRLIK FIYNICCYWE I HSFYLHAL RIPMSALPYC TWQEVQARIV QTQKEHQICI HKRELTELDI YHRILRFQNY MVALVNKSLL PLRFRLPGLG EA VFFTRGL KYNFELILFW GPGSLFLNEW SLKAEYKRGG QRLELAQRLS NRILWIGIAN FLLCPLILIW QILYAFFSYA EVL KREPGA LGARCWSLYG RCYLRHFNEL EHELQSRLNR GYKPASKYMN CFLSPLLTLL AKNGAFFAGS ILAVLIALTI YDED VLAVE HVLTTVTLLG VTVTVCRSFI PDQHMVFCPE QLLRVILAHI HYMPDHWQGN AHRSQTRDEF AQLFQYKAVF ILEEL LSPI VTPLILIFCL RPRALEIIDF FRNFTVEVVG VGDTCSFAQM DVRQHGHPQW LSAGQTEASV YQQAEDGKTE LSLMHF AIT NPGWQPPRES TAFLGFLKEQ VQRDGAAASL AQGGLLPENA LFTSIQSLQS ESEPLSLIAN VVAGSSCRGP PLPRDLQ GS RHRAEVASAL RSFSPLQPGQ APTGRAHSTM TGSGVDARTA SSGSSVWEGQ LQSLVLSEYA STEMSLHALY MHQLHKQQ A QAEPERHVWH RRESDESGES APDEGGEGAR APQSIPRSAS YPCAAPRPGA PETTALHGGF QRRYGGITDP GTVPRVPSH FSRLPLGGWA EDGQSASRHP EPVPEEGSED ELPPQVHKV UniProtKB: Autophagy-related protein 9A |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 65.17 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD 最大 デフォーカス(公称値): 1.9000000000000001 µm 最小 デフォーカス(公称値): 1.4000000000000001 µm 倍率(公称値): 105000 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)