+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-11777 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | RET/GDF15/GFRAL extracellular complex negative stain envelope | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 26.0 Å | |||||||||
 データ登録者 データ登録者 | Adams SE / Earl CP / McDonald NQ | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2021 ジャーナル: Structure / 年: 2021タイトル: A two-site flexible clamp mechanism for RET-GDNF-GFRα1 assembly reveals both conformational adaptation and strict geometric spacing. 著者: Sarah E Adams / Andrew G Purkiss / Phillip P Knowles / Andrea Nans / David C Briggs / Annabel Borg / Christopher P Earl / Kerry M Goodman / Agata Nawrotek / Aaron J Borg / Pauline B McIntosh ...著者: Sarah E Adams / Andrew G Purkiss / Phillip P Knowles / Andrea Nans / David C Briggs / Annabel Borg / Christopher P Earl / Kerry M Goodman / Agata Nawrotek / Aaron J Borg / Pauline B McIntosh / Francesca M Houghton / Svend Kjær / Neil Q McDonald /  要旨: RET receptor tyrosine kinase plays vital developmental and neuroprotective roles in metazoans. GDNF family ligands (GFLs) when bound to cognate GFRα co-receptors recognize and activate RET ...RET receptor tyrosine kinase plays vital developmental and neuroprotective roles in metazoans. GDNF family ligands (GFLs) when bound to cognate GFRα co-receptors recognize and activate RET stimulating its cytoplasmic kinase function. The principles for RET ligand-co-receptor recognition are incompletely understood. Here, we report a crystal structure of the cadherin-like module (CLD1-4) from zebrafish RET revealing interdomain flexibility between CLD2 and CLD3. Comparison with a cryo-electron microscopy structure of a ligand-engaged zebrafish RET-GDNF-GFRα1a complex indicates conformational changes within a clade-specific CLD3 loop adjacent to the co-receptor. Our observations indicate that RET is a molecular clamp with a flexible calcium-dependent arm that adapts to different GFRα co-receptors, while its rigid arm recognizes a GFL dimer to align both membrane-proximal cysteine-rich domains. We also visualize linear arrays of RET-GDNF-GFRα1a suggesting that a conserved contact stabilizes higher-order species. Our study reveals that ligand-co-receptor recognition by RET involves both receptor plasticity and strict spacing of receptor dimers by GFL ligands. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11777.map.gz emd_11777.map.gz | 4.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11777-v30.xml emd-11777-v30.xml emd-11777.xml emd-11777.xml | 16.4 KB 16.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_11777.png emd_11777.png | 65.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11777 http://ftp.pdbj.org/pub/emdb/structures/EMD-11777 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11777 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11777 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11777_validation.pdf.gz emd_11777_validation.pdf.gz | 200.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11777_full_validation.pdf.gz emd_11777_full_validation.pdf.gz | 199.3 KB | 表示 | |
| XML形式データ |  emd_11777_validation.xml.gz emd_11777_validation.xml.gz | 5.4 KB | 表示 | |
| CIF形式データ |  emd_11777_validation.cif.gz emd_11777_validation.cif.gz | 5.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11777 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11777 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11777 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11777 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11777.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11777.map.gz / 形式: CCP4 / 大きさ: 6.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
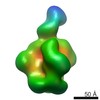
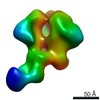
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.438 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
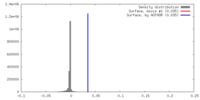
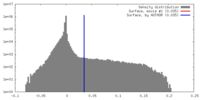
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Ternary complex of the human RET extracellular domain with the GD...
| 全体 | 名称: Ternary complex of the human RET extracellular domain with the GDF15/GFRAL ligand-co-receptor pair |
|---|---|
| 要素 |
|
-超分子 #1: Ternary complex of the human RET extracellular domain with the GD...
| 超分子 | 名称: Ternary complex of the human RET extracellular domain with the GDF15/GFRAL ligand-co-receptor pair タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  Homo sapiens (ヒト) / 組換細胞: Freestyle 293-F / 組換プラスミド: pCEP Homo sapiens (ヒト) / 組換細胞: Freestyle 293-F / 組換プラスミド: pCEP |
| 分子量 | 理論値: 240 KDa |
-分子 #1: Proto-oncogene tyrosine-protein kinase receptor Ret
| 分子 | 名称: Proto-oncogene tyrosine-protein kinase receptor Ret / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: LYFSRDAYWE KLYVDQAAGT PLLYVHALRD APEEVPSFRL GQHLYGTYRT RLHENNWIRI QEDTGLLYLQ RSLDHSSWEK LSVRNRGFPL LTVYLKVFLS PTSLREGECQ WPGCARVYFS FFNTSFPACS SLKPRELCFP ETRPSFRIRE NRPPGTFHQF RLLPVQFLCP ...文字列: LYFSRDAYWE KLYVDQAAGT PLLYVHALRD APEEVPSFRL GQHLYGTYRT RLHENNWIRI QEDTGLLYLQ RSLDHSSWEK LSVRNRGFPL LTVYLKVFLS PTSLREGECQ WPGCARVYFS FFNTSFPACS SLKPRELCFP ETRPSFRIRE NRPPGTFHQF RLLPVQFLCP QISVAYRLLE GEGLPFRSAP DSLEVSTRWA LDREQREKYE LVAVCTVHAG AREEVVMVPF PVTVYDEDDS APTFPAGVDT ASAVVEFKRK EDTVVATLRV FDADVVPASG ELVRRYTSTL LPGDTWAQQT FRVEHWPNET SVQANGSFVR ATVHDYRLVL NRNLSISENR TMQLAVLVND SDFQGPGAGV LLLHFNVSVL PVSLHLPSTY SLSVSRRARR FAQIGKVCVE NCQAFSGINV QYKLHSSGAN CSTLGVVTSA EDTSGILFVN DTKALRRPKC AELHYMVVAT DQQTSRQAQA QLLVTVEGSY VAEEAGCPLS CAVSKRRLEC EECGGLGSPT GRCEWRQGDG KGITRNFSTC SPSTKTCPDG HCDVVETQDI NICPQDCLRG SIVGGHEPGE PRGIKAGYGT CNCFPEEEKC FCEPEDIQDP LCDELCRTGE NLYF |
-分子 #2: GDNF family receptor alpha-like
| 分子 | 名称: GDNF family receptor alpha-like / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: APLANNCTYL REQCLRDANG CKHAWRVMED ACNDSDPGDP CKMRNSSYCN LSIQYLVESN FQFKECLCTD DFYCTVNKLL GKKCINKSDN VKEDKFKWNL TTRSHHGFKG MWSCLEVAEA CVGDVVCNAQ LASYLKACSA NGNPCDLKQC QAAIRFFYQN IPFNIAQMLA ...文字列: APLANNCTYL REQCLRDANG CKHAWRVMED ACNDSDPGDP CKMRNSSYCN LSIQYLVESN FQFKECLCTD DFYCTVNKLL GKKCINKSDN VKEDKFKWNL TTRSHHGFKG MWSCLEVAEA CVGDVVCNAQ LASYLKACSA NGNPCDLKQC QAAIRFFYQN IPFNIAQMLA FCDCAQSDIP CQQSKEALHS KTCAVNMVPP PTCLSVIRSC QNDELCRRHY RTFQSKCWQR VTRKCHEDEN CISTLSKQDL TCSGSDDCKA AYIDILGTVL QVQCTCRTIT QSEESLCKIF QHMLHRKSCF NYPTLSNVKG MALYTRKHAN KITLTGFHSP FNGEAAAHHH HHH |
-分子 #3: Growth/differentiation factor 15
| 分子 | 名称: Growth/differentiation factor 15 / タイプ: protein_or_peptide / ID: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: APLARARNGD HCPLGPGRCC RLHTVRASLE DLGWADWVLS PREVQVTMCI GACPS QFRA ANMHAQIKTS LHRLKPDTVP APCCVPASYN PMVLIQKTDT GVSLQTYDDL LAKDCH CI |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7 構成要素:
詳細: Protein crosslinked by GraFIX method with sucrose/gluteraldehyde gradient | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 染色 | タイプ: NEGATIVE / 材質: uranyl acetate | ||||||||||||||||||
| グリッド | モデル: Homemade / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR / 詳細: 45 mA |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI SPIRIT |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN ULTRASCAN 1000 (2k x 2k) 撮影したグリッド数: 1 / 実像数: 299 / 平均露光時間: 1.0 sec. / 平均電子線量: 20.0 e/Å2 |
| 電子線 | 加速電圧: 120 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 42000 |
| 実験機器 |  モデル: Tecnai Spirit / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| 精密化 | プロトコル: RIGID BODY FIT |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)