+検索条件
-Structure paper
| タイトル | Cooperativity in E. coli aspartate transcarbamoylase is tuned by allosteric breathing. |
|---|---|
| ジャーナル・号・ページ | Nat Commun, Year 2026 |
| 掲載日 | 2026年3月20日 |
 著者 著者 | Robert C Miller / Michael G Patterson / Neti Bhatt / Xiaokun Pei / Nozomi Ando /  |
| PubMed 要旨 | Aspartate transcarbamoylase (ATCase) from Escherichia coli catalyzes a key step in pyrimidine nucleotide biosynthesis and has long served as a model for allosteric regulation. Despite decades of ...Aspartate transcarbamoylase (ATCase) from Escherichia coli catalyzes a key step in pyrimidine nucleotide biosynthesis and has long served as a model for allosteric regulation. Despite decades of study, how nucleotide binding at distant regulatory sites controls cooperativity between active sites remained unresolved. Here we show that ATCase does not simply interconvert between two conformations, as traditionally depicted, but instead samples a continuum of conformations that tune enzyme cooperativity. Using complementary cryo-electron microscopy, small-angle X-ray scattering, and crystallography under conditions that ensure full assembly of the allosteric sites, we show that ATCase behaves like a flexible balloon whose global "breathing" motions directly regulate activity: compression enforces high cooperativity, inhibiting the enzyme, whereas expansion relieves this cooperativity and activates the enzyme. We further show that all four ribonucleoside triphosphates act in symmetric pairs to tune this motion, with the pyrimidines CTP and UTP compressing the enzyme to limit further pyrimidine production, and the purines ATP and GTP expanding it to balance pyrimidine and purine pools. Together, these findings uncover a dynamic breathing mechanism for long-range allosteric communication in ATCase. |
 リンク リンク |  Nat Commun / Nat Commun /  PubMed:41862478 PubMed:41862478 |
| 手法 | EM (単粒子) / X線回折 |
| 解像度 | 2.19 - 3.85 Å |
| 構造データ | EMDB-47956, PDB-9eek: EMDB-47957, PDB-9eel: EMDB-47958, PDB-9eem: EMDB-47959, PDB-9een: EMDB-47960, PDB-9eeo: EMDB-47961, PDB-9eep: EMDB-47963, PDB-9eeq: EMDB-47964, PDB-9eer: EMDB-47965, PDB-9ees: EMDB-47966, PDB-9eeu:  PDB-9eeh:  PDB-9eej: |
| 化合物 | 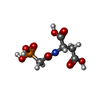 ChemComp-PAL:  ChemComp-ZN:  ChemComp-ATP:  ChemComp-MG:  ChemComp-GTP:  ChemComp-HOH:  ChemComp-CP: 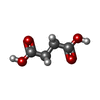 ChemComp-SIN: 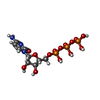 ChemComp-CTP: 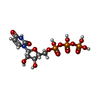 ChemComp-UTP: |
| 由来 |
|
 キーワード キーワード | CYTOSOLIC PROTEIN / Complex / Allostery / ATCase / R-state / ATP / GTP / PALA / CP / succinate / T-state / CTP / UTP / MWC / Expanded |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について
























