+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5aea | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
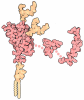
| Title | Crystal structure of human NCAM domain 1 | |||||||||
 Components Components | NEURAL CELL ADHESION MOLECULE 1 Neural cell adhesion molecule Neural cell adhesion molecule | |||||||||
 Keywords Keywords |  CELL ADHESION / CELL ADHESION /  NCAM NCAM | |||||||||
| Function / homology |  Function and homology information Function and homology informationregulation of semaphorin-plexin signaling pathway / commissural neuron axon guidance / NCAM1 interactions / ECM proteoglycans /  epithelial to mesenchymal transition / NCAM signaling for neurite out-growth / Signal transduction by L1 / Interferon gamma signaling / virus receptor activity / RAF/MAP kinase cascade ...regulation of semaphorin-plexin signaling pathway / commissural neuron axon guidance / NCAM1 interactions / ECM proteoglycans / epithelial to mesenchymal transition / NCAM signaling for neurite out-growth / Signal transduction by L1 / Interferon gamma signaling / virus receptor activity / RAF/MAP kinase cascade ...regulation of semaphorin-plexin signaling pathway / commissural neuron axon guidance / NCAM1 interactions / ECM proteoglycans /  epithelial to mesenchymal transition / NCAM signaling for neurite out-growth / Signal transduction by L1 / Interferon gamma signaling / virus receptor activity / RAF/MAP kinase cascade / collagen-containing extracellular matrix / epithelial to mesenchymal transition / NCAM signaling for neurite out-growth / Signal transduction by L1 / Interferon gamma signaling / virus receptor activity / RAF/MAP kinase cascade / collagen-containing extracellular matrix /  cell adhesion / external side of plasma membrane / cell adhesion / external side of plasma membrane /  Golgi membrane / Golgi membrane /  cell surface / extracellular region / cell surface / extracellular region /  membrane / membrane /  plasma membrane / plasma membrane /  cytosol cytosolSimilarity search - Function | |||||||||
| Biological species |   HOMO SAPIENS (human) HOMO SAPIENS (human) | |||||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.9 Å MOLECULAR REPLACEMENT / Resolution: 1.9 Å | |||||||||
 Authors Authors | Kvansakul, M. / Griffiths, K. / Foley, M. | |||||||||
 Citation Citation |  Journal: J.Biol.Chem. / Year: 2016 Journal: J.Biol.Chem. / Year: 2016Title: I-Bodies, Human Single Domain Antibodies that Antagonize Chemokine Receptor Cxcr4. Authors: Griffiths, K. / Dolezal, O. / Cao, B. / Nilsson, S.K. / See, H.B. / Pfleger, K.D.G. / Roche, M. / Gorry, P.R. / Pow, A. / Viduka, K. / Lim, K. / Lu, B.G.C. / Chang, D.H.C. / Murray-Rust, T. ...Authors: Griffiths, K. / Dolezal, O. / Cao, B. / Nilsson, S.K. / See, H.B. / Pfleger, K.D.G. / Roche, M. / Gorry, P.R. / Pow, A. / Viduka, K. / Lim, K. / Lu, B.G.C. / Chang, D.H.C. / Murray-Rust, T. / Kvansakul, M. / Perugini, M.A. / Dogovski, C. / Doerflinger, M. / Zhang, Y. / Parisi, K. / Casey, J.L. / Nuttall, S.D. / Foley, M. | |||||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5aea.cif.gz 5aea.cif.gz | 124.4 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5aea.ent.gz pdb5aea.ent.gz | 100.2 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5aea.json.gz 5aea.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/ae/5aea https://data.pdbj.org/pub/pdb/validation_reports/ae/5aea ftp://data.pdbj.org/pub/pdb/validation_reports/ae/5aea ftp://data.pdbj.org/pub/pdb/validation_reports/ae/5aea | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  1qz1S S: Starting model for refinement |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| Unit cell |
|
- Components
Components
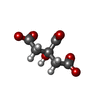
| #1: Protein |  Neural cell adhesion molecule / N-CAM-1 / NCAM-1 / NCAM DOMAIN 1 Neural cell adhesion molecule / N-CAM-1 / NCAM-1 / NCAM DOMAIN 1Mass: 12915.902 Da / Num. of mol.: 2 / Fragment: UNP RESIDUES 20-116 Source method: isolated from a genetically manipulated source Source: (gene. exp.)   HOMO SAPIENS (human) / Production host: HOMO SAPIENS (human) / Production host:   ESCHERICHIA COLI (E. coli) / Strain (production host): TG1 / References: UniProt: P13591 ESCHERICHIA COLI (E. coli) / Strain (production host): TG1 / References: UniProt: P13591#2: Chemical | ChemComp-FLC / |  Citric acid Citric acid#3: Water | ChemComp-HOH / |  Water Water |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.05 Å3/Da / Density % sol: 40 % / Description: NONE |
|---|---|
Crystal grow | pH: 6.88 / Details: 1.45 M TRI-SODIUM CITRATE PH 6.88 |
-Data collection
| Diffraction | Mean temperature: 100 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  Australian Synchrotron Australian Synchrotron  / Beamline: MX2 / Wavelength: 0.9537 / Beamline: MX2 / Wavelength: 0.9537 |
| Detector | Type: ADSC QUANTUM 315 / Detector: CCD / Date: Oct 20, 2012 |
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength : 0.9537 Å / Relative weight: 1 : 0.9537 Å / Relative weight: 1 |
| Reflection | Resolution: 1.9→38.44 Å / Num. obs: 16311 / % possible obs: 99.9 % / Observed criterion σ(I): 2 / Redundancy: 6.4 % / Biso Wilson estimate: 21.69 Å2 / Rmerge(I) obs: 0.1 / Net I/σ(I): 14.4 |
| Reflection shell | Resolution: 1.9→2 Å / Redundancy: 6.4 % / Rmerge(I) obs: 0.79 / Mean I/σ(I) obs: 2.7 / % possible all: 100 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure : :  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: PDB ENTRY 1QZ1 Resolution: 1.9→38.436 Å / SU ML: 0.21 / σ(F): 1.35 / Phase error: 24.33 / Stereochemistry target values: ML
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å / Solvent model: FLAT BULK SOLVENT MODEL | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.9→38.436 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller













 PDBj
PDBj