+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6ehl | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
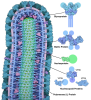
| タイトル | Model of the Ebola virus nucleoprotein in recombinant nucleocapsid-like assemblies | ||||||||||||
 要素 要素 | Nucleoprotein | ||||||||||||
 キーワード キーワード | VIRUS LIKE PARTICLE / nucleocapsid | ||||||||||||
| 機能・相同性 | Ebola nucleoprotein / Ebola nucleoprotein / viral RNA genome packaging / helical viral capsid / viral nucleocapsid / host cell cytoplasm / ribonucleoprotein complex / RNA binding / Nucleoprotein 機能・相同性情報 機能・相同性情報 | ||||||||||||
| 生物種 |  | ||||||||||||
| 手法 | 電子顕微鏡法 / サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 6.6 Å | ||||||||||||
 データ登録者 データ登録者 | Wan, W. / Kolesnikova, L. / Clarke, M. / Koehler, A. / Noda, T. / Becker, S. / Briggs, J.A.G. | ||||||||||||
| 資金援助 |  ドイツ, 3件 ドイツ, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2017 ジャーナル: Nature / 年: 2017タイトル: Structure and assembly of the Ebola virus nucleocapsid. 著者: William Wan / Larissa Kolesnikova / Mairi Clarke / Alexander Koehler / Takeshi Noda / Stephan Becker / John A G Briggs /    要旨: Ebola and Marburg viruses are filoviruses: filamentous, enveloped viruses that cause haemorrhagic fever. Filoviruses are within the order Mononegavirales, which also includes rabies virus, measles ...Ebola and Marburg viruses are filoviruses: filamentous, enveloped viruses that cause haemorrhagic fever. Filoviruses are within the order Mononegavirales, which also includes rabies virus, measles virus, and respiratory syncytial virus. Mononegaviruses have non-segmented, single-stranded negative-sense RNA genomes that are encapsidated by nucleoprotein and other viral proteins to form a helical nucleocapsid. The nucleocapsid acts as a scaffold for virus assembly and as a template for genome transcription and replication. Insights into nucleoprotein-nucleoprotein interactions have been derived from structural studies of oligomerized, RNA-encapsidating nucleoprotein, and cryo-electron microscopy of nucleocapsid or nucleocapsid-like structures. There have been no high-resolution reconstructions of complete mononegavirus nucleocapsids. Here we apply cryo-electron tomography and subtomogram averaging to determine the structure of Ebola virus nucleocapsid within intact viruses and recombinant nucleocapsid-like assemblies. These structures reveal the identity and arrangement of the nucleocapsid components, and suggest that the formation of an extended α-helix from the disordered carboxy-terminal region of nucleoprotein-core links nucleoprotein oligomerization, nucleocapsid condensation, RNA encapsidation, and accessory protein recruitment. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6ehl.cif.gz 6ehl.cif.gz | 32.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6ehl.ent.gz pdb6ehl.ent.gz | 12.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6ehl.json.gz 6ehl.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  6ehl_validation.pdf.gz 6ehl_validation.pdf.gz | 766.5 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  6ehl_full_validation.pdf.gz 6ehl_full_validation.pdf.gz | 766.1 KB | 表示 | |
| XML形式データ |  6ehl_validation.xml.gz 6ehl_validation.xml.gz | 11.8 KB | 表示 | |
| CIF形式データ |  6ehl_validation.cif.gz 6ehl_validation.cif.gz | 16 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/eh/6ehl https://data.pdbj.org/pub/pdb/validation_reports/eh/6ehl ftp://data.pdbj.org/pub/pdb/validation_reports/eh/6ehl ftp://data.pdbj.org/pub/pdb/validation_reports/eh/6ehl | HTTPS FTP |
-関連構造データ
| 関連構造データ |  3869MC  3870C  3871C  3872C  3873C  3874C  3875C  3876C  6ehmC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 83387.500 Da / 分子数: 1 / 変異: Truncation mutant (residues 1-450) / 由来タイプ: 組換発現 由来: (組換発現)  株: Mayinga-76 / 遺伝子: NP / 細胞株 (発現宿主): HEK-293T / 発現宿主:  Homo sapiens (ヒト) / 参照: UniProt: P18272 Homo sapiens (ヒト) / 参照: UniProt: P18272 |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: HELICAL ARRAY / 3次元再構成法: サブトモグラム平均法 |
- 試料調製
試料調製
| 構成要素 | 名称: Ebola virus - Mayinga, Zaire, 1976 / タイプ: VIRUS / Entity ID: all / 由来: RECOMBINANT | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 由来(天然) | 生物種:  | |||||||||||||||||||||||||
| 由来(組換発現) | 生物種:  Homo sapiens (ヒト) / 細胞: HEK 293T Homo sapiens (ヒト) / 細胞: HEK 293T | |||||||||||||||||||||||||
| ウイルスについての詳細 | 中空か: NO / エンベロープを持つか: NO / 単離: STRAIN / タイプ: VIRUS-LIKE PARTICLE | |||||||||||||||||||||||||
| ウイルス殻 | 名称: Nucleocapsid / 直径: 280 nm | |||||||||||||||||||||||||
| 緩衝液 | pH: 7.4 | |||||||||||||||||||||||||
| 緩衝液成分 |
| |||||||||||||||||||||||||
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | |||||||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: C-flat 2/1 3C | |||||||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK II / 凍結剤: ETHANE / 湿度: 95 % |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 81000 X / 最大 デフォーカス(公称値): 4500 nm / 最小 デフォーカス(公称値): 2000 nm / Cs: 2.7 mm / C2レンズ絞り径: 50 µm / アライメント法: ZEMLIN TABLEAU |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 1 sec. / 電子線照射量: 2.4 e/Å2 / 検出モード: SUPER-RESOLUTION フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 撮影したグリッド数: 1 |
| 電子光学装置 | エネルギーフィルター名称: GIF Quantum LS / エネルギーフィルター 上限: 10 eV / エネルギーフィルター 下限: -10 eV |
| 画像スキャン | 横: 3708 / 縦: 3708 / 動画フレーム数/画像: 5 / 利用したフレーム数/画像: 1-5 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 画像処理 | 詳細: Frames were aligned using K2Align software, based off the MotionCorr algorithm. Tomograms were reconstructed with IMOD, using stripwise CTF-correction and weighted back projection. ...詳細: Frames were aligned using K2Align software, based off the MotionCorr algorithm. Tomograms were reconstructed with IMOD, using stripwise CTF-correction and weighted back projection. Subtomogram averaging was performed using scripts derived from TOM, AV3, and DYNAMO. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CTF補正 | 詳細: CTF amplitude correction was performed during the wedge-weighted subtomogram averaging step. タイプ: PHASE FLIPPING ONLY | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 6.6 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 1 / アルゴリズム: BACK PROJECTION 詳細: Local resolution was estimated using moving window FSC calculations. クラス平均像の数: 1 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EM volume selection | 詳細: Points along the helical axis were manually placed to define a spline. A cylindrical grid as defined at a given radius from the spline; grid spacing was chosen to provide ~4x oversampling. Num. of tomograms: 63 / Num. of volumes extracted: 488916 / Reference model: None | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: FLEXIBLE FIT 詳細: Crystal structure was rigid-body fitted into density using Chimera. Missing regions of the structure was built using ideal secondary structures in coot. These were then flexibly fit using MDFF and NAMD. |
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj