+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8354 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of Polycystic Kidney Disease protein 2 (PKD2), residues 198-703 | |||||||||
 マップデータ マップデータ | B-factor sharpened, masked map generated from relion auto-refinement and postprocessing | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報detection of nodal flow / metanephric smooth muscle tissue development / metanephric cortex development / metanephric cortical collecting duct development / metanephric distal tubule development /  polycystin complex / mesonephric tubule development / mesonephric duct development / : / metanephric part of ureteric bud development ...detection of nodal flow / metanephric smooth muscle tissue development / metanephric cortex development / metanephric cortical collecting duct development / metanephric distal tubule development / polycystin complex / mesonephric tubule development / mesonephric duct development / : / metanephric part of ureteric bud development ...detection of nodal flow / metanephric smooth muscle tissue development / metanephric cortex development / metanephric cortical collecting duct development / metanephric distal tubule development /  polycystin complex / mesonephric tubule development / mesonephric duct development / : / metanephric part of ureteric bud development / determination of liver left/right asymmetry / renal tubule morphogenesis / metanephric ascending thin limb development / HLH domain binding / basal cortex / metanephric mesenchyme development / metanephric S-shaped body morphogenesis / renal artery morphogenesis / positive regulation of inositol 1,4,5-trisphosphate-sensitive calcium-release channel activity / migrasome / cilium organization / VxPx cargo-targeting to cilium / detection of mechanical stimulus / regulation of calcium ion import / polycystin complex / mesonephric tubule development / mesonephric duct development / : / metanephric part of ureteric bud development / determination of liver left/right asymmetry / renal tubule morphogenesis / metanephric ascending thin limb development / HLH domain binding / basal cortex / metanephric mesenchyme development / metanephric S-shaped body morphogenesis / renal artery morphogenesis / positive regulation of inositol 1,4,5-trisphosphate-sensitive calcium-release channel activity / migrasome / cilium organization / VxPx cargo-targeting to cilium / detection of mechanical stimulus / regulation of calcium ion import /  cation channel complex / cation channel complex /  calcium-induced calcium release activity / muscle alpha-actinin binding / placenta blood vessel development / voltage-gated monoatomic ion channel activity / cellular response to hydrostatic pressure / outward rectifier potassium channel activity / voltage-gated monoatomic cation channel activity / non-motile cilium / cellular response to fluid shear stress / cellular response to osmotic stress / calcium-induced calcium release activity / muscle alpha-actinin binding / placenta blood vessel development / voltage-gated monoatomic ion channel activity / cellular response to hydrostatic pressure / outward rectifier potassium channel activity / voltage-gated monoatomic cation channel activity / non-motile cilium / cellular response to fluid shear stress / cellular response to osmotic stress /  voltage-gated sodium channel activity / voltage-gated sodium channel activity /  actinin binding / actinin binding /  繊毛 / inorganic cation transmembrane transport / transcription regulator inhibitor activity / determination of left/right symmetry / neural tube development / aorta development / protein heterotetramerization / ciliary membrane / branching involved in ureteric bud morphogenesis / negative regulation of G1/S transition of mitotic cell cycle / spinal cord development / heart looping / cytoplasmic side of endoplasmic reticulum membrane / 繊毛 / inorganic cation transmembrane transport / transcription regulator inhibitor activity / determination of left/right symmetry / neural tube development / aorta development / protein heterotetramerization / ciliary membrane / branching involved in ureteric bud morphogenesis / negative regulation of G1/S transition of mitotic cell cycle / spinal cord development / heart looping / cytoplasmic side of endoplasmic reticulum membrane /  voltage-gated potassium channel activity / cell surface receptor signaling pathway via JAK-STAT / voltage-gated potassium channel activity / cell surface receptor signaling pathway via JAK-STAT /  potassium channel activity / centrosome duplication / sodium ion transmembrane transport / negative regulation of ryanodine-sensitive calcium-release channel activity / potassium channel activity / centrosome duplication / sodium ion transmembrane transport / negative regulation of ryanodine-sensitive calcium-release channel activity /  voltage-gated calcium channel activity / embryonic placenta development / monoatomic cation channel activity / cellular response to cAMP / release of sequestered calcium ion into cytosol / potassium ion transmembrane transport / cellular response to calcium ion / voltage-gated calcium channel activity / embryonic placenta development / monoatomic cation channel activity / cellular response to cAMP / release of sequestered calcium ion into cytosol / potassium ion transmembrane transport / cellular response to calcium ion /  cytoskeletal protein binding / basal plasma membrane / ciliary basal body / liver development / establishment of localization in cell / lumenal side of endoplasmic reticulum membrane / calcium ion transmembrane transport / protein tetramerization / cytoskeletal protein binding / basal plasma membrane / ciliary basal body / liver development / establishment of localization in cell / lumenal side of endoplasmic reticulum membrane / calcium ion transmembrane transport / protein tetramerization /  phosphoprotein binding / cytoplasmic vesicle membrane / phosphoprotein binding / cytoplasmic vesicle membrane /  繊毛 / intracellular calcium ion homeostasis / 繊毛 / intracellular calcium ion homeostasis /  紡錘体 / 紡錘体 /  Wntシグナル経路 / cellular response to reactive oxygen species / positive regulation of nitric oxide biosynthetic process / calcium ion transport / cell-cell junction / Wntシグナル経路 / cellular response to reactive oxygen species / positive regulation of nitric oxide biosynthetic process / calcium ion transport / cell-cell junction /  lamellipodium / regulation of cell population proliferation / lamellipodium / regulation of cell population proliferation /  heart development / heart development /  ATPase binding / positive regulation of cytosolic calcium ion concentration / protein homotetramerization / basolateral plasma membrane / transmembrane transporter binding / ATPase binding / positive regulation of cytosolic calcium ion concentration / protein homotetramerization / basolateral plasma membrane / transmembrane transporter binding /  regulation of cell cycle / negative regulation of cell population proliferation / regulation of cell cycle / negative regulation of cell population proliferation /  signaling receptor binding / signaling receptor binding /  calcium ion binding / endoplasmic reticulum membrane / positive regulation of gene expression / calcium ion binding / endoplasmic reticulum membrane / positive regulation of gene expression /  ゴルジ体 / ゴルジ体 /  小胞体 / protein homodimerization activity / positive regulation of transcription by RNA polymerase II / extracellular exosome 小胞体 / protein homodimerization activity / positive regulation of transcription by RNA polymerase II / extracellular exosome類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
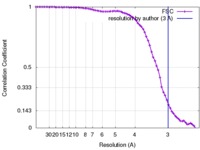
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.0 Å クライオ電子顕微鏡法 / 解像度: 3.0 Å | |||||||||
 データ登録者 データ登録者 | Shen PS / Yang X / DeCaen PG / Liu X / Bulkley D / Clapham DE / Cao E | |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2016 ジャーナル: Cell / 年: 2016タイトル: The Structure of the Polycystic Kidney Disease Channel PKD2 in Lipid Nanodiscs. 著者: Peter S Shen / Xiaoyong Yang / Paul G DeCaen / Xiaowen Liu / David Bulkley / David E Clapham / Erhu Cao /  要旨: The Polycystic Kidney Disease 2 (Pkd2) gene is mutated in autosomal dominant polycystic kidney disease (ADPKD), one of the most common human monogenic disorders. Here, we present the cryo-EM ...The Polycystic Kidney Disease 2 (Pkd2) gene is mutated in autosomal dominant polycystic kidney disease (ADPKD), one of the most common human monogenic disorders. Here, we present the cryo-EM structure of PKD2 in lipid bilayers at 3.0 Å resolution, which establishes PKD2 as a homotetrameric ion channel and provides insight into potential mechanisms for its activation. The PKD2 voltage-sensor domain retains two of four gating charges commonly found in those of voltage-gated ion channels. The PKD2 ion permeation pathway is constricted at the selectivity filter and near the cytoplasmic end of S6, suggesting that two gates regulate ion conduction. The extracellular domain of PKD2, a hotspot for ADPKD pathogenic mutations, contributes to channel assembly and strategically interacts with the transmembrane core, likely serving as a physical substrate for extracellular stimuli to allosterically gate the channel. Finally, our structure establishes the molecular basis for the majority of pathogenic mutations in Pkd2-related ADPKD. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8354.map.gz emd_8354.map.gz | 3.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8354-v30.xml emd-8354-v30.xml emd-8354.xml emd-8354.xml | 18.6 KB 18.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_8354_fsc.xml emd_8354_fsc.xml | 8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_8354_1.png emd_8354_1.png emd_8354_2.png emd_8354_2.png | 178 KB 244.4 KB | ||
| マスクデータ |  emd_8354_msk_1.map emd_8354_msk_1.map | 27 MB |  マスクマップ マスクマップ | |
| その他 |  emd_8354_half_map_1.map.gz emd_8354_half_map_1.map.gz emd_8354_half_map_2.map.gz emd_8354_half_map_2.map.gz | 17.9 MB 17.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8354 http://ftp.pdbj.org/pub/emdb/structures/EMD-8354 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8354 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8354 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8354.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8354.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | B-factor sharpened, masked map generated from relion auto-refinement and postprocessing | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.2156 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_8354_msk_1.map emd_8354_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: RELION half map 2 (relion refine)
| ファイル | emd_8354_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | RELION half map 2 (relion_refine) | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: RELION half map 1 (relion refine)
| ファイル | emd_8354_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | RELION half map 1 (relion_refine) | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : hPKD:198-703
| 全体 | 名称: hPKD:198-703 |
|---|---|
| 要素 |
|
-超分子 #1: hPKD:198-703
| 超分子 | 名称: hPKD:198-703 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:   Homo sapiens (ヒト) / 組換細胞: HEK293S GnTI-/- / 組換プラスミド: pFastbac1 Homo sapiens (ヒト) / 組換細胞: HEK293S GnTI-/- / 組換プラスミド: pFastbac1 |
-分子 #1: hPKD:198-703, Polycystin-2
| 分子 | 名称: hPKD:198-703, Polycystin-2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 59.429145 KDa |
| 組換発現 | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: GAMGSRGLWG TRLMEESSTN REKYLKSVLR ELVTYLLFLI VLCILTYGMM SSNVYYYTRM MSQLFLDTPV SKTEKTNFKT LSSMEDFWK FTEGSLLDGL YWKMQPSNQT EADNRSFIFY ENLLLGVPRI RQLRVRNGSC SIPQDLRDEI KECYDVYSVS S EDRAPFGP ...文字列: GAMGSRGLWG TRLMEESSTN REKYLKSVLR ELVTYLLFLI VLCILTYGMM SSNVYYYTRM MSQLFLDTPV SKTEKTNFKT LSSMEDFWK FTEGSLLDGL YWKMQPSNQT EADNRSFIFY ENLLLGVPRI RQLRVRNGSC SIPQDLRDEI KECYDVYSVS S EDRAPFGP RNGTAWIYTS EKDLNGSSHW GIIATYSGAG YYLDLSRTRE ETAAQVASLK KNVWLDRGTR ATFIDFSVYN AN INLFCVV RLLVEFPATG GVIPSWQFQP LKLIRYVTTF DFFLAACEII FCFFIFYYVV EEILEIRIHK LHYFRSFWNC LDV VIVVLS VVAIGINIYR TSNVEVLLQF LEDQNTFPNF EHLAYWQIQF NNIAAVTVFF VWIKLFKFIN FNRTMSQLST TMSR CAKDL FGFAIMFFII FLAYAQLAYL VFGTQVDDFS TFQECIFTQF RIILGDINFA EIEEANRVLG PIYFTTFVFF MFFIL LNMF LAIINDTYSE VKSDLAQQKA EMELSD |
-分子 #2: 2-acetamido-2-deoxy-beta-D-glucopyranose
| 分子 | 名称: 2-acetamido-2-deoxy-beta-D-glucopyranose / タイプ: ligand / ID: 2 / コピー数: 12 / 式: NAG |
|---|---|
| 分子量 | 理論値: 221.208 Da |
| Chemical component information |  ChemComp-NAG: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
| |||||||||
| グリッド | モデル: Quantifoil / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 80 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK II / 詳細: blot for 7 seconds, -1 mm offset before plunging. | |||||||||
| 詳細 | Single particles embedded in lipid nanodiscs. This sample was monodisperse. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 41132 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 0.6 µm / 倍率(公称値): 31000 Bright-field microscopy / Cs: 2.0 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 0.6 µm / 倍率(公称値): 31000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / 撮影したグリッド数: 1 / 実像数: 1500 / 平均露光時間: 0.2 sec. / 平均電子線量: 1.35 e/Å2 |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z
Z Y
Y X
X