登録情報 データベース : EMDB / ID : EMD-11215タイトル Cryo-EM structure of DNA-PKcs:Ku80ct194 細胞器官・細胞要素 : DNA-PKcs in complex with Ku80 C-terminal domain細胞器官・細胞要素 : DNA-dependent protein kinase catalytic subunit,DNA-PKcsタンパク質・ペプチド : DNA-dependent protein kinase catalytic subunit,DNA-PKcs細胞器官・細胞要素 : X-ray repair cross-complementing protein 5タンパク質・ペプチド : X-ray repair cross-complementing protein 5 / / / / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
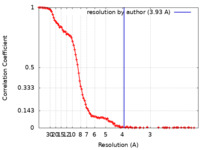
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト)手法 / / 解像度 : 3.93 Å Chaplin AK / Hardwick SW 資金援助 Organization Grant number 国 Wellcome Trust 200814/Z/16/Z
ジャーナル : Nat Struct Mol Biol / 年 : 2021タイトル : Dimers of DNA-PK create a stage for DNA double-strand break repair.
著者 :
Amanda K Chaplin / Steven W Hardwick / Shikang Liang / Antonia Kefala Stavridi / Ales Hnizda / Lee R Cooper / Taiana Maia De Oliveira / Dimitri Y Chirgadze / Tom L Blundell / 要旨 :
DNA double-strand breaks are the most dangerous type of DNA damage and, if not repaired correctly, can lead to cancer. In humans, Ku70/80 recognizes DNA broken ends and recruits the DNA-dependent ... DNA double-strand breaks are the most dangerous type of DNA damage and, if not repaired correctly, can lead to cancer. In humans, Ku70/80 recognizes DNA broken ends and recruits the DNA-dependent protein kinase catalytic subunit (DNA-PKcs) to form DNA-dependent protein kinase holoenzyme (DNA-PK) in the process of non-homologous end joining (NHEJ). We present a 2.8-Å-resolution cryo-EM structure of DNA-PKcs, allowing precise amino acid sequence registration in regions uninterpreted in previous 4.3-Å X-ray maps. We also report a cryo-EM structure of DNA-PK at 3.5-Å resolution and reveal a dimer mediated by the Ku80 C terminus. Central to dimer formation is a domain swap of the conserved C-terminal helix of Ku80. Our results suggest a new mechanism for NHEJ utilizing a DNA-PK dimer to bring broken DNA ends together. Furthermore, drug inhibition of NHEJ in combination with chemo- and radiotherapy has proved successful, making these models central to structure-based drug targeting efforts. 履歴 登録 2020年6月21日 - ヘッダ(付随情報) 公開 2020年10月21日 - マップ公開 2020年10月21日 - 更新 2024年5月1日 - 現状 2024年5月1日 処理サイト : PDBe / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード Kinase (キナーゼ) /
Kinase (キナーゼ) /  DNA-PKcs (DNA依存性プロテインキナーゼ触媒サブユニット) /
DNA-PKcs (DNA依存性プロテインキナーゼ触媒サブユニット) /  NHEJ (非相同末端結合) / DNA-repair / DNA-PK /
NHEJ (非相同末端結合) / DNA-repair / DNA-PK /  DNA BINDING PROTEIN (DNA結合タンパク質) /
DNA BINDING PROTEIN (DNA結合タンパク質) /  Ku80 (Ku80)
Ku80 (Ku80) 機能・相同性情報
機能・相同性情報 DNA end binding / T cell receptor V(D)J recombination / pro-B cell differentiation / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase activity / histone H2AXS139 kinase activity ...Ku70:Ku80 complex / negative regulation of t-circle formation / positive regulation of platelet formation /
DNA end binding / T cell receptor V(D)J recombination / pro-B cell differentiation / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase activity / histone H2AXS139 kinase activity ...Ku70:Ku80 complex / negative regulation of t-circle formation / positive regulation of platelet formation /  DNA end binding / T cell receptor V(D)J recombination / pro-B cell differentiation / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase activity / histone H2AXS139 kinase activity / DNA-dependent protein kinase complex / immature B cell differentiation / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray / immunoglobulin V(D)J recombination /
DNA end binding / T cell receptor V(D)J recombination / pro-B cell differentiation / small-subunit processome assembly / positive regulation of lymphocyte differentiation / DNA-dependent protein kinase activity / histone H2AXS139 kinase activity / DNA-dependent protein kinase complex / immature B cell differentiation / DNA-dependent protein kinase-DNA ligase 4 complex / cellular response to X-ray / immunoglobulin V(D)J recombination /  nonhomologous end joining complex / nuclear telomere cap complex / regulation of smooth muscle cell proliferation / double-strand break repair via alternative nonhomologous end joining / Cytosolic sensors of pathogen-associated DNA / regulation of epithelial cell proliferation / IRF3-mediated induction of type I IFN / telomere capping /
nonhomologous end joining complex / nuclear telomere cap complex / regulation of smooth muscle cell proliferation / double-strand break repair via alternative nonhomologous end joining / Cytosolic sensors of pathogen-associated DNA / regulation of epithelial cell proliferation / IRF3-mediated induction of type I IFN / telomere capping /  相同組換え /
相同組換え /  regulation of telomere maintenance / U3 snoRNA binding / regulation of hematopoietic stem cell differentiation / positive regulation of neurogenesis / protein localization to chromosome, telomeric region / cellular response to fatty acid / hematopoietic stem cell proliferation / cellular hyperosmotic salinity response / maturation of 5.8S rRNA / T cell lineage commitment / negative regulation of cGAS/STING signaling pathway / telomeric DNA binding / positive regulation of catalytic activity / B cell lineage commitment / 2-LTR circle formation / positive regulation of double-strand break repair via nonhomologous end joining / site of DNA damage /
regulation of telomere maintenance / U3 snoRNA binding / regulation of hematopoietic stem cell differentiation / positive regulation of neurogenesis / protein localization to chromosome, telomeric region / cellular response to fatty acid / hematopoietic stem cell proliferation / cellular hyperosmotic salinity response / maturation of 5.8S rRNA / T cell lineage commitment / negative regulation of cGAS/STING signaling pathway / telomeric DNA binding / positive regulation of catalytic activity / B cell lineage commitment / 2-LTR circle formation / positive regulation of double-strand break repair via nonhomologous end joining / site of DNA damage /  enzyme activator activity / hematopoietic stem cell differentiation / positive regulation of protein kinase activity / ectopic germ cell programmed cell death / ATP-dependent activity, acting on DNA /
enzyme activator activity / hematopoietic stem cell differentiation / positive regulation of protein kinase activity / ectopic germ cell programmed cell death / ATP-dependent activity, acting on DNA /  somitogenesis / positive regulation of telomerase activity / mitotic G1 DNA damage checkpoint signaling / positive regulation of telomere maintenance via telomerase /
somitogenesis / positive regulation of telomerase activity / mitotic G1 DNA damage checkpoint signaling / positive regulation of telomere maintenance via telomerase /  DNA helicase activity / activation of innate immune response /
DNA helicase activity / activation of innate immune response /  telomere maintenance / cellular response to leukemia inhibitory factor /
telomere maintenance / cellular response to leukemia inhibitory factor /  神経発生 / small-subunit processome / positive regulation of translation / positive regulation of erythrocyte differentiation / negative regulation of protein phosphorylation /
神経発生 / small-subunit processome / positive regulation of translation / positive regulation of erythrocyte differentiation / negative regulation of protein phosphorylation /  デオキシリボ核酸 / response to gamma radiation / Nonhomologous End-Joining (NHEJ) /
デオキシリボ核酸 / response to gamma radiation / Nonhomologous End-Joining (NHEJ) /  加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 /
加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 /  brain development / peptidyl-threonine phosphorylation / protein destabilization / protein modification process / cellular response to gamma radiation /
brain development / peptidyl-threonine phosphorylation / protein destabilization / protein modification process / cellular response to gamma radiation /  regulation of circadian rhythm / double-strand break repair via nonhomologous end joining / cellular response to insulin stimulus / rhythmic process / intrinsic apoptotic signaling pathway in response to DNA damage / double-strand break repair / E3 ubiquitin ligases ubiquitinate target proteins / T cell differentiation in thymus /
regulation of circadian rhythm / double-strand break repair via nonhomologous end joining / cellular response to insulin stimulus / rhythmic process / intrinsic apoptotic signaling pathway in response to DNA damage / double-strand break repair / E3 ubiquitin ligases ubiquitinate target proteins / T cell differentiation in thymus /  heart development /
heart development /  double-stranded DNA binding / peptidyl-serine phosphorylation / secretory granule lumen / DNA recombination /
double-stranded DNA binding / peptidyl-serine phosphorylation / secretory granule lumen / DNA recombination /  transcription regulator complex / RNA polymerase II-specific DNA-binding transcription factor binding /
transcription regulator complex / RNA polymerase II-specific DNA-binding transcription factor binding /  chromosome, telomeric region / damaged DNA binding / transcription cis-regulatory region binding /
chromosome, telomeric region / damaged DNA binding / transcription cis-regulatory region binding /  non-specific serine/threonine protein kinase /
non-specific serine/threonine protein kinase /  protein kinase activity / response to xenobiotic stimulus /
protein kinase activity / response to xenobiotic stimulus /  ribonucleoprotein complex / positive regulation of apoptotic process / protein domain specific binding /
ribonucleoprotein complex / positive regulation of apoptotic process / protein domain specific binding /  protein phosphorylation / protein serine kinase activity /
protein phosphorylation / protein serine kinase activity /  自然免疫系 / protein serine/threonine kinase activity / negative regulation of DNA-templated transcription / DNA damage response /
自然免疫系 / protein serine/threonine kinase activity / negative regulation of DNA-templated transcription / DNA damage response /  ubiquitin protein ligase binding /
ubiquitin protein ligase binding /  クロマチン
クロマチン
 Homo sapiens (ヒト)
Homo sapiens (ヒト) 単粒子再構成法 /
単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.93 Å
クライオ電子顕微鏡法 / 解像度: 3.93 Å  データ登録者
データ登録者 英国, 1件
英国, 1件  引用
引用 ジャーナル: Nat Struct Mol Biol / 年: 2021
ジャーナル: Nat Struct Mol Biol / 年: 2021
 ジャーナル: Nat.Struct.Mol.Biol. / 年: 2020
ジャーナル: Nat.Struct.Mol.Biol. / 年: 2020 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_11215.map.gz
emd_11215.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-11215-v30.xml
emd-11215-v30.xml emd-11215.xml
emd-11215.xml EMDBヘッダ
EMDBヘッダ emd_11215_fsc.xml
emd_11215_fsc.xml FSCデータファイル
FSCデータファイル emd_11215.png
emd_11215.png emd-11215.cif.gz
emd-11215.cif.gz emd_11215_additional_1.map.gz
emd_11215_additional_1.map.gz emd_11215_half_map_1.map.gz
emd_11215_half_map_1.map.gz emd_11215_half_map_2.map.gz
emd_11215_half_map_2.map.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-11215
http://ftp.pdbj.org/pub/emdb/structures/EMD-11215 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11215
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11215 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_11215.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_11215.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) 試料の構成要素
試料の構成要素 DNA依存性プロテインキナーゼ触媒サブユニット
DNA依存性プロテインキナーゼ触媒サブユニット
 Homo sapiens (ヒト)
Homo sapiens (ヒト)
 Homo sapiens (ヒト)
Homo sapiens (ヒト) non-specific serine/threonine protein kinase
non-specific serine/threonine protein kinase
 Homo sapiens (ヒト)
Homo sapiens (ヒト) 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与
加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与
 Homo sapiens (ヒト)
Homo sapiens (ヒト)
 Escherichia coli (大腸菌)
Escherichia coli (大腸菌) クライオ電子顕微鏡法
クライオ電子顕微鏡法 解析
解析 単粒子再構成法
単粒子再構成法 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN Bright-field microscopy
Bright-field microscopy
 ムービー
ムービー コントローラー
コントローラー


































 Z
Z Y
Y X
X