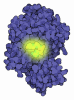
登録情報 データベース : PDB / ID : 5dp2タイトル CurF ER cyclopropanase from curacin A biosynthetic pathway CurF キーワード / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Lyngbya majuscula (バクテリア)手法 / / / 解像度 : 0.96 Å データ登録者 Khare, D. / Smith, J.L. 資金援助 組織 認可番号 国 National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS)
ジャーナル : Structure / 年 : 2015タイトル : Structural Basis for Cyclopropanation by a Unique Enoyl-Acyl Carrier Protein Reductase.著者 : Khare, D. / Hale, W.A. / Tripathi, A. / Gu, L. / Sherman, D.H. / Gerwick, W.H. / Hakansson, K. / Smith, J.L. 履歴 登録 2015年9月12日 登録サイト / 処理サイト 改定 1.0 2015年11月18日 Provider / タイプ 改定 1.1 2015年12月16日 Group 改定 1.2 2017年9月27日 Group / Database references / Derived calculationsカテゴリ / pdbx_audit_support / pdbx_struct_oper_listItem / _pdbx_audit_support.funding_organization / _pdbx_struct_oper_list.symmetry_operation改定 1.3 2019年12月25日 Group / カテゴリ / Item 改定 1.4 2023年9月27日 Group / Database references / Refinement descriptionカテゴリ chem_comp_atom / chem_comp_bond ... chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model Item / _database_2.pdbx_database_accession
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Lyngbya majuscula (バクテリア)
Lyngbya majuscula (バクテリア) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 0.96 Å
分子置換 / 解像度: 0.96 Å  データ登録者
データ登録者 米国, 1件
米国, 1件  引用
引用 ジャーナル: Structure / 年: 2015
ジャーナル: Structure / 年: 2015 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 5dp2.cif.gz
5dp2.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb5dp2.ent.gz
pdb5dp2.ent.gz PDB形式
PDB形式 5dp2.json.gz
5dp2.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード https://data.pdbj.org/pub/pdb/validation_reports/dp/5dp2
https://data.pdbj.org/pub/pdb/validation_reports/dp/5dp2 ftp://data.pdbj.org/pub/pdb/validation_reports/dp/5dp2
ftp://data.pdbj.org/pub/pdb/validation_reports/dp/5dp2 リンク
リンク 集合体
集合体
 要素
要素 Lyngbya majuscula (バクテリア) / 遺伝子: curF / 発現宿主:
Lyngbya majuscula (バクテリア) / 遺伝子: curF / 発現宿主: 
 X線回折
X線回折 試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  APS
APS  / ビームライン: 23-ID-D / 波長: 0.72932 Å
/ ビームライン: 23-ID-D / 波長: 0.72932 Å 解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー
















 PDBj
PDBj