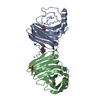
Entry Database : PDB / ID : 5dorTitle P2 Integrase catalytic domain in space group P21 Integrase Keywords / / Function / homology Function Domain/homology Component
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / Biological species Method / / / Resolution : 2.5 Å Authors Skaar, K. / Claesson, M. / Odegrip, R. / Haggard-Ljungquist, E. / Hogbom, M. Funding support Organization Grant number Country Swedish Research Council 2010-5200, 2014-5667 Wenner-Gren Foundation Carl Tryggers Foundation
Journal : Febs Lett. / Year : 2015Title : Crystal structure of the bacteriophage P2 integrase catalytic domain.Authors : Skaar, K. / Claesson, M. / Odegrip, R. / Hogbom, M. / Haggard-Ljungquist, E. / Stenmark, P. History Deposition Sep 11, 2015 Deposition site / Processing site Revision 1.0 Dec 2, 2015 Provider / Type Revision 1.1 Jan 10, 2024 Group / Database references / Refinement descriptionCategory chem_comp_atom / chem_comp_bond ... chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model / struct_ncs_dom_lim Item _database_2.pdbx_DOI / _database_2.pdbx_database_accession ... _database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_ncs_dom_lim.beg_auth_comp_id / _struct_ncs_dom_lim.beg_label_asym_id / _struct_ncs_dom_lim.beg_label_comp_id / _struct_ncs_dom_lim.beg_label_seq_id / _struct_ncs_dom_lim.end_auth_comp_id / _struct_ncs_dom_lim.end_label_asym_id / _struct_ncs_dom_lim.end_label_comp_id / _struct_ncs_dom_lim.end_label_seq_id
Show all Show less
 Open data
Open data Basic information
Basic information Components
Components Keywords
Keywords Function and homology information
Function and homology information Enterobacteria phage P2 (virus)
Enterobacteria phage P2 (virus) X-RAY DIFFRACTION /
X-RAY DIFFRACTION /  SYNCHROTRON /
SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 2.5 Å
MOLECULAR REPLACEMENT / Resolution: 2.5 Å  Authors
Authors Sweden, 3items
Sweden, 3items  Citation
Citation Journal: Febs Lett. / Year: 2015
Journal: Febs Lett. / Year: 2015 Structure visualization
Structure visualization Molmil
Molmil Jmol/JSmol
Jmol/JSmol Downloads & links
Downloads & links Download
Download 5dor.cif.gz
5dor.cif.gz PDBx/mmCIF format
PDBx/mmCIF format pdb5dor.ent.gz
pdb5dor.ent.gz PDB format
PDB format 5dor.json.gz
5dor.json.gz PDBx/mmJSON format
PDBx/mmJSON format Other downloads
Other downloads https://data.pdbj.org/pub/pdb/validation_reports/do/5dor
https://data.pdbj.org/pub/pdb/validation_reports/do/5dor ftp://data.pdbj.org/pub/pdb/validation_reports/do/5dor
ftp://data.pdbj.org/pub/pdb/validation_reports/do/5dor
 Links
Links Assembly
Assembly


 Components
Components Enterobacteria phage P2 (virus) / Gene: int / Production host:
Enterobacteria phage P2 (virus) / Gene: int / Production host: 
 X-RAY DIFFRACTION
X-RAY DIFFRACTION Sample preparation
Sample preparation SYNCHROTRON / Site:
SYNCHROTRON / Site:  BESSY
BESSY  / Beamline: 14.1 / Wavelength: 1.2782 Å
/ Beamline: 14.1 / Wavelength: 1.2782 Å Processing
Processing MOLECULAR REPLACEMENT
MOLECULAR REPLACEMENT Movie
Movie Controller
Controller












 PDBj
PDBj







