[English] 日本語
 Yorodumi
Yorodumi- PDB-4nhf: Crystal structure of the soluble domain of TrwG Type IV secretion... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 4nhf | ||||||
|---|---|---|---|---|---|---|---|
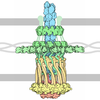
| Title | Crystal structure of the soluble domain of TrwG Type IV secretion machinery from Bartonella grahamii | ||||||
 Components Components | TrwG protein | ||||||
 Keywords Keywords | PROTEIN TRANSPORT / Structural Genomics / NIAID / National Institute of Allergy and Infectious Diseases / Seattle Structural Genomics Center for Infectious Disease / SSGCID / host-specific interaction / outer membrane protein / pathogenesis / type IV secretion system / VirB8 | ||||||
| Function / homology |  Function and homology information Function and homology informationprotein secretion by the type IV secretion system / endomembrane system / metal ion binding / membrane Similarity search - Function | ||||||
| Biological species |  Bartonella grahamii (bacteria) Bartonella grahamii (bacteria) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / MOLECULAR REPLACEMENT /  molecular replacement / Resolution: 2 Å molecular replacement / Resolution: 2 Å | ||||||
 Authors Authors | Seattle Structural Genomics Center for Infectious Disease (SSGCID) | ||||||
 Citation Citation |  Journal: MBio / Year: 2015 Journal: MBio / Year: 2015Title: Structural Insight into How Bacteria Prevent Interference between Multiple Divergent Type IV Secretion Systems. Authors: Gillespie, J.J. / Phan, I.Q. / Scheib, H. / Subramanian, S. / Edwards, T.E. / Lehman, S.S. / Piitulainen, H. / Rahman, M.S. / Rennoll-Bankert, K.E. / Staker, B.L. / Taira, S. / Stacy, R. / ...Authors: Gillespie, J.J. / Phan, I.Q. / Scheib, H. / Subramanian, S. / Edwards, T.E. / Lehman, S.S. / Piitulainen, H. / Rahman, M.S. / Rennoll-Bankert, K.E. / Staker, B.L. / Taira, S. / Stacy, R. / Myler, P.J. / Azad, A.F. / Pulliainen, A.T. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  4nhf.cif.gz 4nhf.cif.gz | 356.4 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb4nhf.ent.gz pdb4nhf.ent.gz | 291.3 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  4nhf.json.gz 4nhf.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Summary document |  4nhf_validation.pdf.gz 4nhf_validation.pdf.gz | 472.8 KB | Display |  wwPDB validaton report wwPDB validaton report |
|---|---|---|---|---|
| Full document |  4nhf_full_validation.pdf.gz 4nhf_full_validation.pdf.gz | 476.2 KB | Display | |
| Data in XML |  4nhf_validation.xml.gz 4nhf_validation.xml.gz | 37.5 KB | Display | |
| Data in CIF |  4nhf_validation.cif.gz 4nhf_validation.cif.gz | 54.8 KB | Display | |
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/nh/4nhf https://data.pdbj.org/pub/pdb/validation_reports/nh/4nhf ftp://data.pdbj.org/pub/pdb/validation_reports/nh/4nhf ftp://data.pdbj.org/pub/pdb/validation_reports/nh/4nhf | HTTPS FTP |
-Related structure data
| Related structure data |  4jf8SC  4kz1C  4lsoC  4meiC  4o3vC S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data | |
| Other databases |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 3 | 
| ||||||||
| Unit cell |
|
- Components
Components
| #1: Protein | Mass: 20379.705 Da / Num. of mol.: 6 / Fragment: soluble domain (UNP residues 63-233) Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Bartonella grahamii (bacteria) / Strain: as4aup / Gene: Bgr_19310, trwG / Production host: Bartonella grahamii (bacteria) / Strain: as4aup / Gene: Bgr_19310, trwG / Production host:  #2: Chemical | ChemComp-CA / #3: Water | ChemComp-HOH / | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.16 Å3/Da / Density % sol: 43.16 % |
|---|---|
| Crystal grow | Temperature: 289 K / Method: vapor diffusion, sitting drop / pH: 6 Details: BagrA.18388.b.B2.PW37127 at 19.5 mg/mL against PACT condition B11, 0.2 M CaCl2, 0.1 M MES pH 6.0, 20% PEG 6000 supplemented with 20% glycerol as cryo-protectant, crystal tracking ID ...Details: BagrA.18388.b.B2.PW37127 at 19.5 mg/mL against PACT condition B11, 0.2 M CaCl2, 0.1 M MES pH 6.0, 20% PEG 6000 supplemented with 20% glycerol as cryo-protectant, crystal tracking ID 248166b11, unique puck ID ngo7-6, VAPOR DIFFUSION, SITTING DROP, temperature 289K |
-Data collection
| Diffraction | Mean temperature: 100 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  APS APS  / Beamline: 21-ID-F / Wavelength: 0.97856 Å / Beamline: 21-ID-F / Wavelength: 0.97856 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: RAYONIX MX-300 / Detector: CCD / Date: Oct 3, 2013 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength | Wavelength: 0.97856 Å / Relative weight: 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 2→50 Å / Num. obs: 71950 / % possible obs: 99.1 % / Observed criterion σ(I): -3 / Biso Wilson estimate: 30.553 Å2 / Rmerge(I) obs: 0.08 / Net I/σ(I): 15.35 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell | Diffraction-ID: 1
|
-Phasing
| Phasing | Method:  molecular replacement molecular replacement |
|---|
- Processing
Processing
| Software |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: 4JF8 Resolution: 2→50 Å / Cor.coef. Fo:Fc: 0.955 / Cor.coef. Fo:Fc free: 0.931 / WRfactor Rfree: 0.2269 / WRfactor Rwork: 0.182 / Occupancy max: 1 / Occupancy min: 0.3 / FOM work R set: 0.7856 / SU B: 8.673 / SU ML: 0.126 / SU R Cruickshank DPI: 0.1729 / SU Rfree: 0.1608 / Cross valid method: THROUGHOUT / σ(F): 0 / ESU R: 0.173 / ESU R Free: 0.161 / Stereochemistry target values: MAXIMUM LIKELIHOOD Details: U VALUES : WITH TLS ADDED HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Ion probe radii: 0.8 Å / Shrinkage radii: 0.8 Å / VDW probe radii: 1.2 Å / Solvent model: MASK | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 90.51 Å2 / Biso mean: 31.9757 Å2 / Biso min: 11.14 Å2
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 2→50 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 2→2.052 Å / Total num. of bins used: 20
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller












 PDBj
PDBj