+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 3lo2 | ||||||
|---|---|---|---|---|---|---|---|
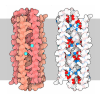
| Title | Crystal structure of human alpha-defensin 1 (Y21A mutant) | ||||||
 Components Components | Neutrophil defensin 1 | ||||||
 Keywords Keywords | ANTIMICROBIAL PROTEIN / ANTIMICROBIAL PEPTIDE / HUMAN ALPHA DEFENSIN 1 / HUMAN NEUTROPHIL PEPTIDE 1 / HNP1 / ANTIBIOTIC / ANTIMICROBIAL / Antiviral defense / Defensin / Disulfide bond / Fungicide / Phosphoprotein / Secreted | ||||||
| Function / homology |  Function and homology information Function and homology informationdisruption of plasma membrane integrity in another organism / Defensins / pore-forming activity / : / T cell chemotaxis / Alpha-defensins / defense response to protozoan / defense response to fungus / estrogen receptor signaling pathway / innate immune response in mucosa ...disruption of plasma membrane integrity in another organism / Defensins / pore-forming activity / : / T cell chemotaxis / Alpha-defensins / defense response to protozoan / defense response to fungus / estrogen receptor signaling pathway / innate immune response in mucosa / Golgi lumen / chemotaxis / azurophil granule lumen / antimicrobial humoral immune response mediated by antimicrobial peptide / antibacterial humoral response / killing of cells of another organism / defense response to virus / defense response to Gram-negative bacterium / defense response to Gram-positive bacterium / immune response / innate immune response / Neutrophil degranulation / : / extracellular exosome / extracellular region Similarity search - Function | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  MOLECULAR REPLACEMENT / Resolution: 1.56 Å MOLECULAR REPLACEMENT / Resolution: 1.56 Å | ||||||
 Authors Authors | Pazgier, M. / Lu, W. | ||||||
 Citation Citation |  Journal: J.Biol.Chem. / Year: 2010 Journal: J.Biol.Chem. / Year: 2010Title: Trp-26 imparts functional versatility to human alpha-defensin HNP1. Authors: Wei, G. / Pazgier, M. / de Leeuw, E. / Rajabi, M. / Li, J. / Zou, G. / Jung, G. / Yuan, W. / Lu, W.Y. / Lehrer, R.I. / Lu, W. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  3lo2.cif.gz 3lo2.cif.gz | 27.1 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb3lo2.ent.gz pdb3lo2.ent.gz | 17.1 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  3lo2.json.gz 3lo2.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/lo/3lo2 https://data.pdbj.org/pub/pdb/validation_reports/lo/3lo2 ftp://data.pdbj.org/pub/pdb/validation_reports/lo/3lo2 ftp://data.pdbj.org/pub/pdb/validation_reports/lo/3lo2 | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  3h6cC  3lo1C  3lo4C  3lo6C  3lo9C  3loeC  3lvxC  3gnyS S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||||||||||||
| 2 | 
| ||||||||||||||||||
| 3 |
| ||||||||||||||||||
| Unit cell |
| ||||||||||||||||||
| Components on special symmetry positions |
| ||||||||||||||||||
| Noncrystallographic symmetry (NCS) | NCS domain:
NCS domain segments: Component-ID: 1 / Ens-ID: 1 / Beg auth comp-ID: ALA / Beg label comp-ID: ALA / End auth comp-ID: CYS / End label comp-ID: CYS / Refine code: 6 / Auth seq-ID: 1 - 30 / Label seq-ID: 1 - 30
| ||||||||||||||||||
| Details | biological unit is half of asymmetric unit |
- Components
Components
| #1: Protein/peptide | Mass: 3360.015 Da / Num. of mol.: 2 / Fragment: UNP residues 65-94 / Mutation: Y21A / Source method: obtained synthetically / Details: Protein is naturally found in HUMAN / References: UniProt: P59665 #2: Chemical | #3: Chemical | ChemComp-TFA / | #4: Chemical | ChemComp-SO4 / | #5: Water | ChemComp-HOH / | Has protein modification | Y | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.02 Å3/Da / Density % sol: 39.03 % |
|---|---|
| Crystal grow | Temperature: 298 K / Method: vapor diffusion, hanging drop Details: 30% PEG 8,000; 0.2 M ammonium sulfate, pH pH 8, VAPOR DIFFUSION, HANGING DROP, temperature 298K PH range: pH 8 |
-Data collection
| Diffraction | Mean temperature: 100 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  ROTATING ANODE / Type: RIGAKU MICROMAX-007 / Wavelength: 1.54 Å ROTATING ANODE / Type: RIGAKU MICROMAX-007 / Wavelength: 1.54 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: RIGAKU RAXIS IV++ / Detector: IMAGE PLATE / Date: Mar 18, 2008 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength | Wavelength: 1.54 Å / Relative weight: 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Redundancy: 3.1 % / Number: 23252 / Rmerge(I) obs: 0.107 / Χ2: 1.2 / D res high: 1.56 Å / D res low: 50 Å / Num. obs: 7547 / % possible obs: 92 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diffraction reflection shell |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 1.56→41.552 Å / Num. all: 8139 / Num. obs: 7534 / % possible obs: 93 % / Observed criterion σ(I): 2 / Redundancy: 3.1 % / Rmerge(I) obs: 0.107 / Rsym value: 0.157 / Net I/σ(I): 10.3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell | Resolution: 1.56→1.59 Å / Redundancy: 2.9 % / Rmerge(I) obs: 0.106 / Mean I/σ(I) obs: 2.9 / Rsym value: 0.11 / % possible all: 80.3 |
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: PDB ENTRY 3GNY Resolution: 1.56→20 Å / Cor.coef. Fo:Fc: 0.961 / Cor.coef. Fo:Fc free: 0.96 / Occupancy max: 1 / Occupancy min: 0.5 / SU B: 2.754 / SU ML: 0.048 / Cross valid method: THROUGHOUT / ESU R: 0.095 / ESU R Free: 0.091 / Stereochemistry target values: MAXIMUM LIKELIHOOD / Details: U VALUES : RESIDUAL ONLY
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Ion probe radii: 0.8 Å / Shrinkage radii: 0.8 Å / VDW probe radii: 1.4 Å / Solvent model: BABINET MODEL WITH MASK | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 13.388 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.56→20 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints NCS | Dom-ID: 1 / Auth asym-ID: A / Ens-ID: 1 / Number: 231 / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 1.562→1.602 Å / Total num. of bins used: 20
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller









 PDBj
PDBj