+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2ppz | ||||||
|---|---|---|---|---|---|---|---|
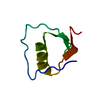
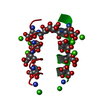
| タイトル | NMR solution Structure of the Villin Headpiece Mutant G34L | ||||||
 要素 要素 | Villin-1 | ||||||
 キーワード キーワード | STRUCTURAL PROTEIN / small stable core / alpha helical / thermostable / in silico sequence optimization | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報regulation of actin nucleation / lysophosphatidic acid binding / cytoplasmic actin-based contraction involved in cell motility / regulation of lamellipodium morphogenesis / filopodium tip / positive regulation of actin filament bundle assembly / actin filament severing / regulation of wound healing / barbed-end actin filament capping / actin filament capping ...regulation of actin nucleation / lysophosphatidic acid binding / cytoplasmic actin-based contraction involved in cell motility / regulation of lamellipodium morphogenesis / filopodium tip / positive regulation of actin filament bundle assembly / actin filament severing / regulation of wound healing / barbed-end actin filament capping / actin filament capping / actin filament depolymerization / actin polymerization or depolymerization / cysteine-type endopeptidase inhibitor activity involved in apoptotic process / cellular response to hepatocyte growth factor stimulus / actin filament bundle / microvillus / positive regulation of epithelial cell migration / ruffle / phosphatidylinositol-4,5-bisphosphate binding / actin filament polymerization / cellular response to epidermal growth factor stimulus / filopodium / response to bacterium / epidermal growth factor receptor signaling pathway / actin filament binding / actin cytoskeleton / lamellipodium / regulation of cell shape / positive regulation of cell migration / calcium ion binding / protein homodimerization activity / cytoplasm 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 溶液NMR / simulated annealing | ||||||
 データ登録者 データ登録者 | Gronwald, W. / Hohm, T. / Hoffmann, D. | ||||||
 引用 引用 |  ジャーナル: Bmc Bioinformatics / 年: 2008 ジャーナル: Bmc Bioinformatics / 年: 2008タイトル: Evolutionary Pareto-optimization of stably folding peptides 著者: Gronwald, W. / Hohm, T. / Hoffmann, D. | ||||||
| 履歴 |
| ||||||
| Remark 999 | SEQUENCE The authors state that residue Met1 of the peptide is not from villin but was included to ...SEQUENCE The authors state that residue Met1 of the peptide is not from villin but was included to compare their fragment with the corresponding structure in PDB entry 1VII where Met1 is also included. |
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2ppz.cif.gz 2ppz.cif.gz | 141.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2ppz.ent.gz pdb2ppz.ent.gz | 117.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2ppz.json.gz 2ppz.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  2ppz_validation.pdf.gz 2ppz_validation.pdf.gz | 337.6 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  2ppz_full_validation.pdf.gz 2ppz_full_validation.pdf.gz | 387.7 KB | 表示 | |
| XML形式データ |  2ppz_validation.xml.gz 2ppz_validation.xml.gz | 6 KB | 表示 | |
| CIF形式データ |  2ppz_validation.cif.gz 2ppz_validation.cif.gz | 9.2 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/pp/2ppz https://data.pdbj.org/pub/pdb/validation_reports/pp/2ppz ftp://data.pdbj.org/pub/pdb/validation_reports/pp/2ppz ftp://data.pdbj.org/pub/pdb/validation_reports/pp/2ppz | HTTPS FTP |
-関連構造データ
| 類似構造データ | |
|---|---|
| その他のデータベース |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||
| NMR アンサンブル |
|
- 要素
要素
| #1: タンパク質・ペプチド | 分子量: 4252.007 Da / 分子数: 1 断片: C-terminal residues of headpiece domain, sequence database residues 792-826 変異: G34L / 由来タイプ: 合成 詳細: Synthesized on a peptide synthesizer using the FMOC/But strategy. 由来: (合成)  |
|---|
-実験情報
-実験
| 実験 | 手法: 溶液NMR | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| NMR実験 |
|
- 試料調製
試料調製
| 詳細 | 内容: 4.3 mg peptide dissolved in 0.5 ml 90% H2O, 10% D2O (v/v) and 0.1 mM 2,2-dimethyl-2-silapentane sulfonic acid (DSS) for internal referencing 溶媒系: 90% H2O/10% D2O |
|---|---|
| 試料状態 | pH: 5 / 圧: ambient / 温度: 298 K |
-NMR測定
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M |
|---|---|
| 放射波長 | 相対比: 1 |
| NMRスペクトロメーター | タイプ: Bruker DRX / 製造業者: Bruker / モデル: DRX / 磁場強度: 500 MHz |
- 解析
解析
| NMR software |
| ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 手法: simulated annealing / ソフトェア番号: 1 / 詳細: torsion angle dynamics | ||||||||||||||||
| 代表構造 | 選択基準: lowest energy | ||||||||||||||||
| NMRアンサンブル | コンフォーマー選択の基準: structures with favorable non-bond energy 計算したコンフォーマーの数: 200 / 登録したコンフォーマーの数: 10 |
 ムービー
ムービー コントローラー
コントローラー









 PDBj
PDBj
 CYANA
CYANA