+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2cyu | ||||||
|---|---|---|---|---|---|---|---|
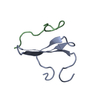
| タイトル | NMR structure of a downhill folding protein | ||||||
 要素 要素 | 2-OXOGLUTARATE DEHYDROGENASE MULTIENZYME COMPLEX | ||||||
 キーワード キーワード | TRANSFERASE / helix bundle / downhill folding protein | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報L-lysine catabolic process to acetyl-CoA via saccharopine / dihydrolipoyllysine-residue succinyltransferase / dihydrolipoyllysine-residue succinyltransferase activity / oxoglutarate dehydrogenase complex / tricarboxylic acid cycle / cytosol 類似検索 - 分子機能 | ||||||
| 手法 | 溶液NMR / simulated annealing | ||||||
 データ登録者 データ登録者 | Munoz, V. / Sadqi, M. | ||||||
 引用 引用 |  ジャーナル: Nature / 年: 2006 ジャーナル: Nature / 年: 2006タイトル: Atom-by-atom analysis of global downhill protein folding. 著者: Sadqi, M. / Fushman, D. / Munoz, V. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2cyu.cif.gz 2cyu.cif.gz | 238.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2cyu.ent.gz pdb2cyu.ent.gz | 196.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2cyu.json.gz 2cyu.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  2cyu_validation.pdf.gz 2cyu_validation.pdf.gz | 339.1 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  2cyu_full_validation.pdf.gz 2cyu_full_validation.pdf.gz | 465.5 KB | 表示 | |
| XML形式データ |  2cyu_validation.xml.gz 2cyu_validation.xml.gz | 14 KB | 表示 | |
| CIF形式データ |  2cyu_validation.cif.gz 2cyu_validation.cif.gz | 23.2 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/cy/2cyu https://data.pdbj.org/pub/pdb/validation_reports/cy/2cyu ftp://data.pdbj.org/pub/pdb/validation_reports/cy/2cyu ftp://data.pdbj.org/pub/pdb/validation_reports/cy/2cyu | HTTPS FTP |
-関連構造データ
| 関連構造データ | |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||
| NMR アンサンブル |
|
- 要素
要素
| #1: タンパク質・ペプチド | 分子量: 4400.073 Da / 分子数: 1 / 断片: E3-BINDING DOMAIN / 由来タイプ: 合成 詳細: The peptide was chemically synthesized. The sequence of the peptide is naturally found in E coli. 参照: UniProt: P0AFG7, dihydrolipoyllysine-residue succinyltransferase |
|---|
-実験情報
-実験
| 実験 | 手法: 溶液NMR | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| NMR実験 |
| ||||||||||||||||
| NMR実験の詳細 | Text: This structure was determined using standard 2D homonuclear techniques. |
- 試料調製
試料調製
| 詳細 | 内容: 90% H2O, 10% D2O, trace amounts of DSS for NMR calibration 溶媒系: 90% H2O/10% D2O |
|---|---|
| 試料状態 | イオン強度: 0 / pH: 5.3 / 圧: ambient / 温度: 278 K |
-NMR測定
| NMRスペクトロメーター | タイプ: Bruker DRX / 製造業者: Bruker / モデル: DRX / 磁場強度: 500 MHz |
|---|
- 解析
解析
| NMR software |
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 手法: simulated annealing / ソフトェア番号: 1 詳細: THE FIRST THREE RESIDUES OF OUR PROTEIN VARIANT ARE NOT STRUCTURED (NO DISTANCE RESTRAINTS). ACCORDINGLY, THE COORDINATES FOR THE N-TERMINAL NAPHTHYLALANINE ARE NOT SHOWN | ||||||||||||||||||||
| 代表構造 | 選択基準: lowest energy | ||||||||||||||||||||
| NMRアンサンブル | コンフォーマー選択の基準: structures with the lowest energy 計算したコンフォーマーの数: 300 / 登録したコンフォーマーの数: 20 |
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj

 NMRPipe
NMRPipe