+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-6609 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-electron microscopy structure of influenza H5 hemagglutinin expressed on the viral surface | |||||||||
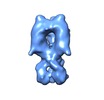
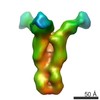
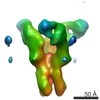
 マップデータ マップデータ | Tomographic subvolume average of virus-bound influenza H5 HA | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Influenza / HA | |||||||||
| 生物種 |   unidentified influenza virus (インフルエンザウイルス) unidentified influenza virus (インフルエンザウイルス) | |||||||||
| 手法 | サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 25.0 Å | |||||||||
 データ登録者 データ登録者 | Tran EEH / Podolsky KA / Bartesaghi A / Kuybeda O / Grandinetti G / Wohlbold TJ / Tan GS / Nachbagauer R / Palese P / Krammer F / Subramaniam S | |||||||||
 引用 引用 |  ジャーナル: mBio / 年: 2016 ジャーナル: mBio / 年: 2016タイトル: Cryo-electron Microscopy Structures of Chimeric Hemagglutinin Displayed on a Universal Influenza Vaccine Candidate. 著者: Erin E H Tran / Kira A Podolsky / Alberto Bartesaghi / Oleg Kuybeda / Giovanna Grandinetti / Teddy John Wohlbold / Gene S Tan / Raffael Nachbagauer / Peter Palese / Florian Krammer / Sriram Subramaniam /   要旨: Influenza viruses expressing chimeric hemagglutinins (HAs) are important tools in the quest for a universal vaccine. Using cryo-electron tomography, we have determined the structures of a chimeric HA ...Influenza viruses expressing chimeric hemagglutinins (HAs) are important tools in the quest for a universal vaccine. Using cryo-electron tomography, we have determined the structures of a chimeric HA variant that comprises an H1 stalk and an H5 globular head domain (cH5/1 HA) in native and antibody-bound states. We show that cH5/1 HA is structurally different from native HA, displaying a 60° rotation between the stalk and head groups, leading to a novel and unexpected "open" arrangement of HA trimers. cH5/1N1 viruses also display higher glycoprotein density than pH1N1 or H5N1 viruses, but despite these differences, antibodies that target either the stalk or head domains of hemagglutinins still bind to cH5/1 HA with the same consequences as those observed with native H1 or H5 HA. Our results show that a large range of structural plasticity can be tolerated in the chimeric spike scaffold without disrupting structural and geometric aspects of antibody binding. IMPORTANCE: Chimeric hemagglutinin proteins are set to undergo human clinical trials as a universal influenza vaccine candidate, yet no structural information for these proteins is available. Using ...IMPORTANCE: Chimeric hemagglutinin proteins are set to undergo human clinical trials as a universal influenza vaccine candidate, yet no structural information for these proteins is available. Using cryo-electron tomography, we report the first three-dimensional (3D) visualization of chimeric hemagglutinin proteins displayed on the surface of the influenza virus. We show that, unexpectedly, the chimeric hemagglutinin structure differs from those of naturally occurring hemagglutinins by displaying a more open head domain and a dramatically twisted head/stalk arrangement. Despite this unusual spatial relationship between head and stalk regions, virus preparations expressing the chimeric hemagglutinin are fully infectious and display a high glycoprotein density, which likely helps induction of a broadly protective immune response. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_6609.map.gz emd_6609.map.gz | 513.3 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-6609-v30.xml emd-6609-v30.xml emd-6609.xml emd-6609.xml | 11.2 KB 11.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_6609.png emd_6609.png | 364.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-6609 http://ftp.pdbj.org/pub/emdb/structures/EMD-6609 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6609 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6609 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_6609.map.gz / 形式: CCP4 / 大きさ: 908.2 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_6609.map.gz / 形式: CCP4 / 大きさ: 908.2 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Tomographic subvolume average of virus-bound influenza H5 HA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 これらの図は立方格子座標系で作成されたものです | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 4.1 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
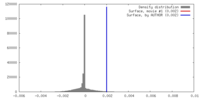
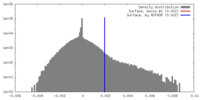
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Tomographic subvolume average of virus-bound influenza H5 HA
| 全体 | 名称: Tomographic subvolume average of virus-bound influenza H5 HA |
|---|---|
| 要素 |
|
-超分子 #1000: Tomographic subvolume average of virus-bound influenza H5 HA
| 超分子 | 名称: Tomographic subvolume average of virus-bound influenza H5 HA タイプ: sample / ID: 1000 / Number unique components: 1 |
|---|
-分子 #1: H5 hemagglutinin
| 分子 | 名称: H5 hemagglutinin / タイプ: protein_or_peptide / ID: 1 / 集合状態: trimer / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種:   unidentified influenza virus (インフルエンザウイルス) unidentified influenza virus (インフルエンザウイルス)株: H5N1 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 / 詳細: 25 mM Tris, 100 mM NaCl |
|---|---|
| グリッド | 詳細: Quantifoil Multi-A 200 mesh carbon grids |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 90 K / 装置: LEICA EM GP / 手法: Blot for 6 seconds before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: Gatan, Inc. エネルギーフィルター - エネルギー下限: 0.0 eV エネルギーフィルター - エネルギー上限: 20.0 eV |
| 日付 | 2015年7月22日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 実像数: 10 / 平均電子線量: 120 e/Å2 詳細: Every image is the average of two frames recorded by the direct electron detector. |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 23000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 64000 |
| 試料ステージ | 試料ホルダー: Liquid nitrogen-cooled 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER Tilt series - Axis1 - Min angle: -60 ° / Tilt series - Axis1 - Max angle: 60 ° |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 詳細 | Subtomograms were selected manually. |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 25.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称:  IMOD / 使用したサブトモグラム数: 129 IMOD / 使用したサブトモグラム数: 129 |
 ムービー
ムービー コントローラー
コントローラー














 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)