+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4414 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | beta-galactosidase (integrating mode) | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
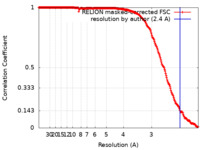
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.4 Å | |||||||||
 データ登録者 データ登録者 | Song B / Flegler V | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Ultramicroscopy / 年: 2019 ジャーナル: Ultramicroscopy / 年: 2019タイトル: Capabilities of the Falcon III detector for single-particle structure determination. 著者: Boyuan Song / Julian Lenhart / Vanessa Judith Flegler / Cihan Makbul / Tim Rasmussen / Bettina Böttcher /  要旨: Direct electron detectors are an essential asset for the resolution revolution in electron cryo microscopy of biological objects. The direct detectors provide two modes of data acquisition; the ...Direct electron detectors are an essential asset for the resolution revolution in electron cryo microscopy of biological objects. The direct detectors provide two modes of data acquisition; the counting mode in which single electrons are counted, and the integrating mode in which the signal that arises from the incident electrons is integrated. While counting mode leads to far higher detective quantum efficiency at all spatial frequencies, the integrating mode enables faster data acquisition at higher exposure rates. For optimal throughput at best possible resolution it is important to understand when the better performance in counting mode becomes essential for solving a structure and when the lower detective quantum efficiency in integrating mode can be compensated by increasing the number of particles in the data set. Here, we provide a case study of the Falcon III camera, which has counting mode capability at exposure rates of <0.9 e/Px² and integrating mode capability at exposure rates above 10 e/Px². We found that counting mode gives better resolution for medium sized complexes such as the β-galactosidase (465 kDa) (2.2 Å, 97% of Nyquist vs. 2.4 Å, 89% of Nyquist) with data sets of similar size. However, for larger particles such as Hepatitis B virus capsid like particles (4.8 MDa) we did not find any resolution gain in counting mode. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4414.map.gz emd_4414.map.gz | 767.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4414-v30.xml emd-4414-v30.xml emd-4414.xml emd-4414.xml | 19.2 KB 19.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_4414_fsc.xml emd_4414_fsc.xml | 21 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4414.png emd_4414.png | 102.7 KB | ||
| その他 |  emd_4414_half_map_1.map.gz emd_4414_half_map_1.map.gz emd_4414_half_map_2.map.gz emd_4414_half_map_2.map.gz | 666.9 MB 666.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4414 http://ftp.pdbj.org/pub/emdb/structures/EMD-4414 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4414 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4414 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_4414_validation.pdf.gz emd_4414_validation.pdf.gz | 277.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_4414_full_validation.pdf.gz emd_4414_full_validation.pdf.gz | 276.4 KB | 表示 | |
| XML形式データ |  emd_4414_validation.xml.gz emd_4414_validation.xml.gz | 27 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4414 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4414 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4414 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4414 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4414.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4414.map.gz / 形式: CCP4 / 大きさ: 824 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.0635 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
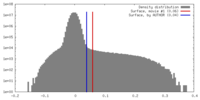
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-ハーフマップ: #2
| ファイル | emd_4414_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
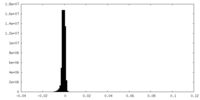
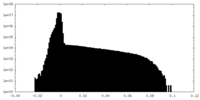
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_4414_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
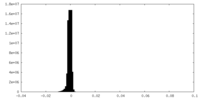
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : beta-galactosidase
| 全体 | 名称: beta-galactosidase |
|---|---|
| 要素 |
|
-超分子 #1: beta-galactosidase
| 超分子 | 名称: beta-galactosidase / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: sample was purchased from Sigma G5635 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 465 KDa |
-分子 #1: beta-galactosidase
| 分子 | 名称: beta-galactosidase / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO / EC番号: beta-galactosidase |
|---|---|
| 配列 | 文字列: MTMITDSLAV VLQRRDWENP GVTQLNRLAA HPPFASWRNS EEARTDRPSQ QLRSLNGEWR FAWFPAPEA VPESWLECDL PEADTVVVPS NWQMHGYDAP IYTNVTYPIT VNPPFVPTEN P TGCYSLTF NVDESWLQEG QTRIIFDGVN SAFHLWCNGR WVGYGQDSRL ...文字列: MTMITDSLAV VLQRRDWENP GVTQLNRLAA HPPFASWRNS EEARTDRPSQ QLRSLNGEWR FAWFPAPEA VPESWLECDL PEADTVVVPS NWQMHGYDAP IYTNVTYPIT VNPPFVPTEN P TGCYSLTF NVDESWLQEG QTRIIFDGVN SAFHLWCNGR WVGYGQDSRL PSEFDLSAFL RA GENRLAV MVLRWSDGSY LEDQDMWRMS GIFRDVSLLH KPTTQISDFH VATRFNDDFS RAV LEAEVQ MCGELRDYLR VTVSLWQGET QVASGTAPFG GEIIDERGGY ADRVTLRLNV ENPK LWSAE IPNLYRAVVE LHTADGTLIE AEACDVGFRE VRIENGLLLL NGKPLLIRGV NRHEH HPLH GQVMDEQTMV QDILLMKQNN FNAVRCSHYP NHPLWYTLCD RYGLYVVDEA NIETHG MVP MNRLTDDPRW LPAMSERVTR MVQRDRNHPS VIIWSLGNES GHGANHDALY RWIKSVD PS RPVQYEGGGA DTTATDIICP MYARVDEDQP FPAVPKWSIK KWLSLPGETR PLILCEYA H AMGNSLGGFA KYWQAFRQYP RLQGGFVWDW VDQSLIKYDE NGNPWSAYGG DFGDTPNDR QFCMNGLVFA DRTPHPALTE AKHQQQFFQF RLSGQTIEVT SEYLFRHSDN ELLHWMVALD GKPLASGEV PLDVAPQGKQ LIELPELPQP ESAGQLWLTV RVVQPNATAW SEAGHISAWQ Q WRLAENLS VTLPAASHAI PHLTTSEMDF CIELGNKRWQ FNRQSGFLSQ MWIGDKKQLL TP LRDQFTR APLDNDIGVS EATRIDPNAW VERWKAAGHY QAEAALLQCT ADTLADAVLI TTA HAWQHQ GKTLFISRKT YRIDGSGQMA ITVDVEVASD TPHPARIGLN CQLAQVAERV NWLG LGPQE NYPDRLTAAC FDRWDLPLSD MYTPYVFPSE NGLRCGTREL NYGPHQWRGD FQFNI SRYS QQQLMETSHR HLLHAEEGTW LNIDGFHMGI GGDDSWSPSV SAEFQLSAGR YHYQLV WCQ K |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2.6 mg/mL |
|---|---|
| 緩衝液 | pH: 7.9 詳細: The lyophilized protein powder was reconstituted into a 5 mg/ml solution with 50 mM Tris-HCl (pH 7.9), 50 mM NaCl, 2 mM MgCl2 and 2mM Mercaptoethanol. 300 ul of this solution were loaded onto ...詳細: The lyophilized protein powder was reconstituted into a 5 mg/ml solution with 50 mM Tris-HCl (pH 7.9), 50 mM NaCl, 2 mM MgCl2 and 2mM Mercaptoethanol. 300 ul of this solution were loaded onto a Superdex 200 10/300 GL (GE LifeSciences) size-exclusion chromatography column and eluted with 50 mM Tris-HCl (pH 7.9), 50 mM NaCl, 2 mM MgCl2 and 2 mM TCEP. Peak fractions corresponding to the tetrameric complex were pooled and concentrated to 2.6 mg/ml with a 50 kDa MWCO spin concentrator (Amicon, Millipore Co.). The sample were checked by SDS-PAGE with silver staining (Pierce silver staining kit, ThermoFischer Scientific). |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV 詳細: Quantifoil 400 mesh copper grids R 1.2/1.3 were used (Quantifoil Micro Tools GmbH, Jena, Germany). Grids were glow discharged in air at a pressure of 2.2x10-2 Torr for 2 min at medium power ...詳細: Quantifoil 400 mesh copper grids R 1.2/1.3 were used (Quantifoil Micro Tools GmbH, Jena, Germany). Grids were glow discharged in air at a pressure of 2.2x10-2 Torr for 2 min at medium power with a Harrick Plasma cleaner (PDC-002). Subsequently, 3-4 ul of the sample was pipetted onto the glow discharged grids and plunge frozen in liquid Ethane with a Vitrobot IV (FEI). The sample chamber of the Vitrobot was maintained at 4C and 100% humidity. Wait time between sample application and blotting was 45 s, the drain time 0 s, the blot time 3 s and the blot force 0.. |
| 詳細 | beta-Galactosidase from E. coli was purchased from SIGMA-ALDRICH (G5635). |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 79.0 K / 最高: 80.0 K |
| 詳細 | data has been recorded in integrating mode 25 frames per movie |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: INTEGRATING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 実像数: 1389 / 平均露光時間: 4.3 sec. / 平均電子線量: 52.0 e/Å2 詳細: images were collected in movie mode (25 frames in total) |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 2.77 µm / 最小 デフォーカス(補正後): 1.12 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.5 µm / 倍率(公称値): 75000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: RECIPROCAL / プロトコル: AB INITIO MODEL / 温度因子: 34 |
|---|
 ムービー
ムービー コントローラー
コントローラー





























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)