+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3933 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | In situ subtomogram average of the Chlamydomonas single-capped 26S proteasome | |||||||||
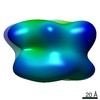
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
| 手法 | サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 23.81 Å | |||||||||
 データ登録者 データ登録者 | Albert S / Schaffer M / Beck F / Mosalaganti S / Asano S / Thomas HF / Plitzko J / Beck M / Baumeister W / Engel BD | |||||||||
| 資金援助 |  ドイツ, 2件 ドイツ, 2件
| |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2017 ジャーナル: Proc Natl Acad Sci U S A / 年: 2017タイトル: Proteasomes tether to two distinct sites at the nuclear pore complex. 著者: Sahradha Albert / Miroslava Schaffer / Florian Beck / Shyamal Mosalaganti / Shoh Asano / Henry F Thomas / Jürgen M Plitzko / Martin Beck / Wolfgang Baumeister / Benjamin D Engel /  要旨: The partitioning of cellular components between the nucleus and cytoplasm is the defining feature of eukaryotic life. The nuclear pore complex (NPC) selectively gates the transport of macromolecules ...The partitioning of cellular components between the nucleus and cytoplasm is the defining feature of eukaryotic life. The nuclear pore complex (NPC) selectively gates the transport of macromolecules between these compartments, but it is unknown whether surveillance mechanisms exist to reinforce this function. By leveraging in situ cryo-electron tomography to image the native cellular environment of , we observed that nuclear 26S proteasomes crowd around NPCs. Through a combination of subtomogram averaging and nanometer-precision localization, we identified two classes of proteasomes tethered via their Rpn9 subunits to two specific NPC locations: binding sites on the NPC basket that reflect its eightfold symmetry and more abundant binding sites at the inner nuclear membrane that encircle the NPC. These basket-tethered and membrane-tethered proteasomes, which have similar substrate-processing state frequencies as proteasomes elsewhere in the cell, are ideally positioned to regulate transcription and perform quality control of both soluble and membrane proteins transiting the NPC. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3933.map.gz emd_3933.map.gz | 9.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3933-v30.xml emd-3933-v30.xml emd-3933.xml emd-3933.xml | 14.4 KB 14.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_3933.png emd_3933.png | 20 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3933 http://ftp.pdbj.org/pub/emdb/structures/EMD-3933 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3933 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3933 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3933_validation.pdf.gz emd_3933_validation.pdf.gz | 208.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3933_full_validation.pdf.gz emd_3933_full_validation.pdf.gz | 207.7 KB | 表示 | |
| XML形式データ |  emd_3933_validation.xml.gz emd_3933_validation.xml.gz | 5.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3933 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3933 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3933 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3933 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3933.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3933.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.42 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : In situ single-capped 26S proteasome
| 全体 | 名称: In situ single-capped 26S proteasome |
|---|---|
| 要素 |
|
-超分子 #1: In situ single-capped 26S proteasome
| 超分子 | 名称: In situ single-capped 26S proteasome / タイプ: complex / ID: 1 / 親要素: 0 詳細: In situ subtomogram average generated from single-capped 26S proteasomes imaged within the native Chlamydomonas cell. Cells were thinned by focused ion beam milling. |
|---|---|
| 由来(天然) | 生物種:  株: mat3-4 / Organelle: nucleus, cytoplasm / 細胞中の位置: nucleus, cytoplasm |
| 分子量 | 理論値: 2 MDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | cell |
- 試料調製
試料調製
| 緩衝液 | pH: 7 |
|---|---|
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE-PROPANE / チャンバー内湿度: 90 % / チャンバー内温度: 293 K / 装置: FEI VITROBOT MARK IV 詳細: Blotted for 10 seconds with 10 blot force before plunging.. |
| 詳細 | Single-capped 26S proteasome within the cytoplasm and nucleus of the native Chlamydomonas cell. Whole cells were plunge-frozen onto EM grids and then thinned with a cryo-focused ion beam instrument. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS エネルギーフィルター - エネルギー下限: 0 eV エネルギーフィルター - エネルギー上限: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3838 pixel / デジタル化 - サイズ - 縦: 3710 pixel / 平均露光時間: 1.5 sec. / 平均電子線量: 1.5 e/Å2 詳細: Images were collected in movie mode at 12 frames per second |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 6.0 µm / 最小 デフォーカス(公称値): 4.0 µm / 倍率(公称値): 42000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー



















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





















