+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of Methylococcus capsulatus (Bath) pMMO in a native lipid nanodisc at 2.26 Angstrom resolution | |||||||||
 マップデータ マップデータ | CryoEM structure of Methylococcus capsulatus (Bath) pMMO in a POPC lipid nanodisc at 2.26 angstrom resolution | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Complex / OXIDOREDUCTASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報methane monooxygenase (particulate) / methane monooxygenase (soluble) / : / : / monooxygenase activity / membrane / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Methylococcus capsulatus (strain ATCC 33009 / NCIMB 11132 / Bath) (バクテリア) / Methylococcus capsulatus (strain ATCC 33009 / NCIMB 11132 / Bath) (バクテリア) /  Methylococcus capsulatus str. Bath (バクテリア) Methylococcus capsulatus str. Bath (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.26 Å | |||||||||
 データ登録者 データ登録者 | Koo CW / Rosenzweig AC | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2022 ジャーナル: Science / 年: 2022タイトル: Recovery of particulate methane monooxygenase structure and activity in a lipid bilayer. 著者: Christopher W Koo / Frank J Tucci / Yuan He / Amy C Rosenzweig /  要旨: Bacterial methane oxidation using the enzyme particulate methane monooxygenase (pMMO) contributes to the removal of environmental methane, a potent greenhouse gas. Crystal structures determined using ...Bacterial methane oxidation using the enzyme particulate methane monooxygenase (pMMO) contributes to the removal of environmental methane, a potent greenhouse gas. Crystal structures determined using inactive, detergent-solubilized pMMO lack several conserved regions neighboring the proposed active site. We show that reconstituting pMMO in nanodiscs with lipids extracted from the native organism restores methane oxidation activity. Multiple nanodisc-embedded pMMO structures determined by cryo-electron microscopy to 2.14- to 2.46-angstrom resolution reveal the structure of pMMO in a lipid environment. The resulting model includes stabilizing lipids, regions of the PmoA and PmoC subunits not observed in prior structures, and a previously undetected copper-binding site in the PmoC subunit with an adjacent hydrophobic cavity. These structures provide a revised framework for understanding and engineering pMMO function. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_24827.map.gz emd_24827.map.gz | 278.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-24827-v30.xml emd-24827-v30.xml emd-24827.xml emd-24827.xml | 14.9 KB 14.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
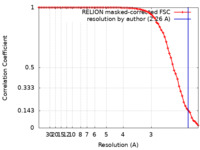
| FSC (解像度算出) |  emd_24827_fsc.xml emd_24827_fsc.xml | 7.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_24827.png emd_24827.png | 118.2 KB | ||
| Filedesc metadata |  emd-24827.cif.gz emd-24827.cif.gz | 5.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-24827 http://ftp.pdbj.org/pub/emdb/structures/EMD-24827 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-24827 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-24827 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_24827_validation.pdf.gz emd_24827_validation.pdf.gz | 613.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_24827_full_validation.pdf.gz emd_24827_full_validation.pdf.gz | 613.4 KB | 表示 | |
| XML形式データ |  emd_24827_validation.xml.gz emd_24827_validation.xml.gz | 11.2 KB | 表示 | |
| CIF形式データ |  emd_24827_validation.cif.gz emd_24827_validation.cif.gz | 14.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-24827 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-24827 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-24827 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-24827 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7s4iMC  7s4hC  7s4jC  7s4kC  7s4lC  7s4mC  7t4oC  7t4pC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_24827.map.gz / 形式: CCP4 / 大きさ: 307.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_24827.map.gz / 形式: CCP4 / 大きさ: 307.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | CryoEM structure of Methylococcus capsulatus (Bath) pMMO in a POPC lipid nanodisc at 2.26 angstrom resolution | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.47222 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : pMMO complex in a native lipid nanodisc
+超分子 #1: pMMO complex in a native lipid nanodisc
+分子 #1: Particulate methane monooxygenase alpha subunit
+分子 #2: Ammonia monooxygenase/methane monooxygenase, subunit C family protein
+分子 #3: Particulate methane monooxygenase beta subunit
+分子 #4: COPPER (II) ION
+分子 #5: DECANE
+分子 #6: DIUNDECYL PHOSPHATIDYL CHOLINE
+分子 #7: 1,2-dihexanoyl-sn-glycero-3-phosphocholine
+分子 #8: 1,2-DIDECANOYL-SN-GLYCERO-3-PHOSPHOCHOLINE
+分子 #9: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.3 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 52.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー