+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-21009 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Lon Protease from Yersinia pestis | ||||||||||||||||||
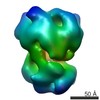
 マップデータ マップデータ | Final reconstruction used for model building and refinement | ||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||
 キーワード キーワード | AAA+ ATPase / Quality Control / Protease / HYDROLASE | ||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報endopeptidase La / ATP-dependent peptidase activity / protein quality control for misfolded or incompletely synthesized proteins / cellular response to heat / sequence-specific DNA binding / serine-type endopeptidase activity / ATP hydrolysis activity / ATP binding / cytoplasm 類似検索 - 分子機能 | ||||||||||||||||||
| 生物種 |  | ||||||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.8 Å | ||||||||||||||||||
 データ登録者 データ登録者 | Shin M / Puchades C | ||||||||||||||||||
| 資金援助 |  米国, 5件 米国, 5件
| ||||||||||||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2020 ジャーナル: Sci Adv / 年: 2020タイトル: Structural basis for distinct operational modes and protease activation in AAA+ protease Lon. 著者: Mia Shin / Cristina Puchades / Ananya Asmita / Neha Puri / Eric Adjei / R Luke Wiseman / A Wali Karzai / Gabriel C Lander /  要旨: Substrate-bound structures of AAA+ protein translocases reveal a conserved asymmetric spiral staircase architecture wherein a sequential ATP hydrolysis cycle drives hand-over-hand substrate ...Substrate-bound structures of AAA+ protein translocases reveal a conserved asymmetric spiral staircase architecture wherein a sequential ATP hydrolysis cycle drives hand-over-hand substrate translocation. However, this configuration is unlikely to represent the full conformational landscape of these enzymes, as biochemical studies suggest distinct conformational states depending on the presence or absence of substrate. Here, we used cryo-electron microscopy to determine structures of the Lon AAA+ protease in the absence and presence of substrate, uncovering the mechanistic basis for two distinct operational modes. In the absence of substrate, Lon adopts a left-handed, "open" spiral organization with autoinhibited proteolytic active sites. Upon the addition of substrate, Lon undergoes a reorganization to assemble an enzymatically active, right-handed "closed" conformer with active protease sites. These findings define the mechanistic principles underlying the operational plasticity required for processing diverse protein substrates. | ||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_21009.map.gz emd_21009.map.gz | 59.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-21009-v30.xml emd-21009-v30.xml emd-21009.xml emd-21009.xml | 23.1 KB 23.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
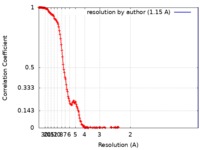
| FSC (解像度算出) |  emd_21009_fsc.xml emd_21009_fsc.xml | 11.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_21009.png emd_21009.png | 83.9 KB | ||
| Filedesc metadata |  emd-21009.cif.gz emd-21009.cif.gz | 7.2 KB | ||
| その他 |  emd_21009_half_map_1.map.gz emd_21009_half_map_1.map.gz emd_21009_half_map_2.map.gz emd_21009_half_map_2.map.gz | 59.4 MB 59.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-21009 http://ftp.pdbj.org/pub/emdb/structures/EMD-21009 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21009 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21009 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_21009_validation.pdf.gz emd_21009_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_21009_full_validation.pdf.gz emd_21009_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_21009_validation.xml.gz emd_21009_validation.xml.gz | 16 KB | 表示 | |
| CIF形式データ |  emd_21009_validation.cif.gz emd_21009_validation.cif.gz | 21.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21009 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21009 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21009 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21009 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_21009.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_21009.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Final reconstruction used for model building and refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.15 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-ハーフマップ: Half-map B from final reconstruction used to calculate FSC
| ファイル | emd_21009_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map B from final reconstruction used to calculate FSC | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half-map A from final reconstruction used to calculate FSC
| ファイル | emd_21009_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half-map A from final reconstruction used to calculate FSC | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Lon Protease from Yersinia pestis
| 全体 | 名称: Lon Protease from Yersinia pestis |
|---|---|
| 要素 |
|
-超分子 #1: Lon Protease from Yersinia pestis
| 超分子 | 名称: Lon Protease from Yersinia pestis / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 詳細: Complexes consisting of homohexameric Lon protease from Yersinia pestis were isolated using size-exclusion chromatography |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Lon protease
| 分子 | 名称: Lon protease / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO / EC番号: endopeptidase La |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 57.780863 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: ALKRKIEAAK MPKDAREKTE AELQKLKMMS PMSAEATVVR GYIDWMLQVP WNSRSKVKKD LVKAQEVLDT DHYGLERVKD RILEYLAVQ SRVSKIKGPI LCLVGPPGVG KTSLGQSIAK ATGRQYVRMA LGGVRDEAEI RGHRRTYIGS MPGKLIQKMA K VGVKNPLF ...文字列: ALKRKIEAAK MPKDAREKTE AELQKLKMMS PMSAEATVVR GYIDWMLQVP WNSRSKVKKD LVKAQEVLDT DHYGLERVKD RILEYLAVQ SRVSKIKGPI LCLVGPPGVG KTSLGQSIAK ATGRQYVRMA LGGVRDEAEI RGHRRTYIGS MPGKLIQKMA K VGVKNPLF LLDEIDKMAS DMRGDPASAL LEVLDPEQNV AFNDHYLEVD YDLSDVMFVA TSNSMNIPAP LLDRMEVIRL SG YTEDEKL NIAKQHLLPK QFERNAIKKG ELTIDDSAIM SIIRYYTREA GVRSLEREIS KLCRKAVKNL LMDKTVKHIE ING DNLKDF LGVQKVDYGR ADTENRVGQV TGLAWTEVGG DLLTIETACV PGKGKLTYTG SLGEVMQESI QAALTVVRAR ADKL GINPD FYEKRDIHVH VPEGATPKDG PSAGIAMCTA LVSCLTGNPV RADVAMTGEI TLRGLVLPIG GLKEKLLAAH RGGIK VVLI PDDNKRDLEE IPDNVIADLE IHPVKRIDDV LAIALEHPA UniProtKB: Lon protease |
-分子 #2: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 5 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 17 mg/mL | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
詳細: Solutions were made fresh from concentrated and filtered using a 0.1 um syringe filter to avoid microbial contamination. Buffers were stored on ice and used within 15 minutes of mixing in ...詳細: Solutions were made fresh from concentrated and filtered using a 0.1 um syringe filter to avoid microbial contamination. Buffers were stored on ice and used within 15 minutes of mixing in order to avoid excess ATP hydrolysis. | ||||||||||||||||||
| グリッド | モデル: UltrAuFoil / 材質: GOLD / メッシュ: 400 | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277 K / 装置: HOMEMADE PLUNGER 詳細: 4 uL of sample was applied per grid and manually blotted for 4 seconds followed by immediately plunge-freezing in liquid ethane cooled by liquid nitrogen.. | ||||||||||||||||||
| 詳細 | This sample was monodisperse |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 温度 | 最低: 80.0 K / 最高: 90.0 K |
| アライメント法 | Coma free - Residual tilt: 0.14 mrad |
| 詳細 | Coma-free alignment procedure from Herzik & Wu, Nature Methods (2017). Preliminary grid screening was performed manually prior to data collection. |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3710 pixel / デジタル化 - サイズ - 縦: 3838 pixel / デジタル化 - 画像ごとのフレーム数: 0-57 / 撮影したグリッド数: 1 / 実像数: 1864 / 平均露光時間: 11.6 sec. / 平均電子線量: 50.0 e/Å2 詳細: Images were collected in counting mode at 5 frames per second |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 1.5 µm / 最小 デフォーカス(補正後): 0.5 µm / 倍率(補正後): 43478 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.2 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 36000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A / Chain - Residue range: 253-775 / Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | Initial rigid body docking was done using UCSF Chimera |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 115 / 当てはまり具合の基準: Correlation coefficient |
| 得られたモデル |  PDB-6v11: |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)