+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1372 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Architecture of the Dam1 kinetochore ring complex and implications for microtubule-driven assembly and force-coupling mechanisms. | |||||||||
 マップデータ マップデータ | This is the single particle reconstruction of the wild-type Dam1 complex in its dimeric form. | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 28.0 Å | |||||||||
 データ登録者 データ登録者 | Wang H-W / Ramey VH / Westermann S / Leschziner AE / Welburn JPI / Nakajima Y / Drubin DG / Barnes G / Nogales E | |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2007 ジャーナル: Nat Struct Mol Biol / 年: 2007タイトル: Architecture of the Dam1 kinetochore ring complex and implications for microtubule-driven assembly and force-coupling mechanisms. 著者: Hong-Wei Wang / Vincent H Ramey / Stefan Westermann / Andres E Leschziner / Julie P I Welburn / Yuko Nakajima / David G Drubin / Georjana Barnes / Eva Nogales /  要旨: The Dam1 kinetochore complex is essential for chromosome segregation in budding yeast. This ten-protein complex self-assembles around microtubules, forming ring-like structures that move with ...The Dam1 kinetochore complex is essential for chromosome segregation in budding yeast. This ten-protein complex self-assembles around microtubules, forming ring-like structures that move with depolymerizing microtubule ends, a mechanism with implications for cellular function. Here we used EM-based single-particle and helical analyses to define the architecture of the Dam1 complex at 30-A resolution and the self-assembly mechanism. Ring oligomerization seems to be facilitated by a conformational change upon binding to microtubules, suggesting that the Dam1 ring is not preformed, but self-assembles around kinetochore microtubules. The C terminus of the Dam1p protein, where most of the Aurora kinase Ipl1 phosphorylation sites reside, is in a strategic location to affect oligomerization and interactions with the microtubule. One of Ipl1's roles might be to fine-tune the coupling of the microtubule interaction with the conformational change required for oligomerization, with phosphorylation resulting in ring breakdown. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1372.map.gz emd_1372.map.gz | 7.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1372-v30.xml emd-1372-v30.xml emd-1372.xml emd-1372.xml | 9.7 KB 9.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1372.gif 1372.gif | 36.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1372 http://ftp.pdbj.org/pub/emdb/structures/EMD-1372 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1372 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1372 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1372_validation.pdf.gz emd_1372_validation.pdf.gz | 205.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1372_full_validation.pdf.gz emd_1372_full_validation.pdf.gz | 204.7 KB | 表示 | |
| XML形式データ |  emd_1372_validation.xml.gz emd_1372_validation.xml.gz | 5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1372 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1372 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1372 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1372 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1372.map.gz / 形式: CCP4 / 大きさ: 8.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1372.map.gz / 形式: CCP4 / 大きさ: 8.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | This is the single particle reconstruction of the wild-type Dam1 complex in its dimeric form. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 4 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
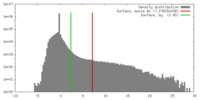
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Dam1 complex
| 全体 | 名称: Dam1 complex |
|---|---|
| 要素 |
|
-超分子 #1000: Dam1 complex
| 超分子 | 名称: Dam1 complex / タイプ: sample / ID: 1000 詳細: The sample is mainly dimeric with some in monomeric and trimeric forms. 集合状態: dimer of decamer / Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 200 KDa / 理論値: 200 KDa |
-分子 #1: Dam1 complex
| 分子 | 名称: Dam1 complex / タイプ: protein_or_peptide / ID: 1 / Name.synonym: DASH / コピー数: 2 / 集合状態: dimer of decamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 200 KDa / 理論値: 200 KDa |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.02 mg/mL |
|---|---|
| 緩衝液 | pH: 6.8 詳細: 500 mM NaCl, 20 mM sodium phosphate pH 6.8, 1 mM EDTA |
| 染色 | タイプ: NEGATIVE 詳細: The complexes were negatively stained with 2% uranyl formate with the sandwich method between two layers of thin carbon film |
| グリッド | 詳細: 400 mesh copper grid |
| 凍結 | 凍結剤: NONE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI 12 |
|---|---|
| アライメント法 | Legacy - 非点収差: objective lens astigmatism was corrected at 120,000 magnification |
| 詳細 | Low dose mode was used in data collection |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: OTHER / デジタル化 - サンプリング間隔: 12.7 µm / 実像数: 200 詳細: The films were digitized on a Nikon Super Coolscan 8000 scanner Od range: 1.4 / ビット/ピクセル: 14 |
| Tilt angle min | 0 |
| 電子線 | 加速電圧: 120 kV / 電子線源: LAB6 |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 6.6 mm / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 49000 |
| 試料ステージ | 試料ホルダー: Eucentric / 試料ホルダーモデル: OTHER / Tilt angle max: 65 |
- 画像解析
画像解析
| 詳細 | The particles were picked by hand in WEB |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 28.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: IMAGIC, SPIDER / 使用した粒子像数: 4468 |
| 最終 2次元分類 | クラス数: 50 |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)