登録情報 データベース : EMDB / ID : EMD-13393タイトル The structure of human neurofibromin isoform 2 in closed conformation DeepEMhancer sharpened map. Main map. 複合体 : Homo-dimer of human Neurofibromin Isoform 2タンパク質・ペプチド : Neurofibrominリガンド : ZINC ION / / / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
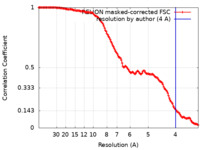
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト)手法 / / 解像度 : 4.0 Å Naschberger A / Baradaran R 資金援助 Organization Grant number 国 Knut and Alice Wallenberg Foundation 431042 Austrian Science Fund P28395 Austrian Science Fund I5152
ジャーナル : Nature / 年 : 2021タイトル : The structure of neurofibromin isoform 2 reveals different functional states.著者 : Andreas Naschberger / Rozbeh Baradaran / Bernhard Rupp / Marta Carroni / 要旨 : The autosomal dominant monogenetic disease neurofibromatosis type 1 (NF1) affects approximately one in 3,000 individuals and is caused by mutations in the NF1 tumour suppressor gene, leading to ... The autosomal dominant monogenetic disease neurofibromatosis type 1 (NF1) affects approximately one in 3,000 individuals and is caused by mutations in the NF1 tumour suppressor gene, leading to dysfunction in the protein neurofibromin (Nf1). As a GTPase-activating protein, a key function of Nf1 is repression of the Ras oncogene signalling cascade. We determined the human Nf1 dimer structure at an overall resolution of 3.3 Å. The cryo-electron microscopy structure reveals domain organization and structural details of the Nf1 exon 23a splicing isoform 2 in a closed, self-inhibited, Zn-stabilized state and an open state. In the closed conformation, HEAT/ARM core domains shield the GTPase-activating protein-related domain (GRD) so that Ras binding is sterically inhibited. In a distinctly different, open conformation of one protomer, a large-scale movement of the GRD occurs, which is necessary to access Ras, whereas Sec14-PH reorients to allow interaction with the cellular membrane. Zn incubation of Nf1 leads to reduced Ras-GAP activity with both protomers in the self-inhibited, closed conformation stabilized by a Zn binding site between the N-HEAT/ARM domain and the GRD-Sec14-PH linker. The transition between closed, self-inhibited states of Nf1 and open states provides guidance for targeted studies deciphering the complex molecular mechanism behind the widespread neurofibromatosis syndrome and Nf1 dysfunction in carcinogenesis. 履歴 登録 2021年8月15日 - ヘッダ(付随情報) 公開 2021年11月17日 - マップ公開 2021年11月17日 - 更新 2024年7月17日 - 現状 2024年7月17日 処理サイト : PDBe / 状態 : 公開
すべて表示 表示を減らす
 万見
万見 データを開く
データを開く 基本情報
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) データ登録者
データ登録者 オーストリア, 3件
オーストリア, 3件  引用
引用 ジャーナル: Nature / 年: 2021
ジャーナル: Nature / 年: 2021


 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_13393.map.gz
emd_13393.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-13393-v30.xml
emd-13393-v30.xml emd-13393.xml
emd-13393.xml EMDBヘッダ
EMDBヘッダ emd_13393_fsc.xml
emd_13393_fsc.xml FSCデータファイル
FSCデータファイル emd_13393.png
emd_13393.png emd_13393_msk_1.map
emd_13393_msk_1.map マスクマップ
マスクマップ emd-13393.cif.gz
emd-13393.cif.gz emd_13393_additional_1.map.gz
emd_13393_additional_1.map.gz emd_13393_half_map_1.map.gz
emd_13393_half_map_1.map.gz emd_13393_half_map_2.map.gz
emd_13393_half_map_2.map.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-13393
http://ftp.pdbj.org/pub/emdb/structures/EMD-13393 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13393
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13393 emd_13393_validation.pdf.gz
emd_13393_validation.pdf.gz EMDB検証レポート
EMDB検証レポート emd_13393_full_validation.pdf.gz
emd_13393_full_validation.pdf.gz emd_13393_validation.xml.gz
emd_13393_validation.xml.gz emd_13393_validation.cif.gz
emd_13393_validation.cif.gz https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13393
https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13393 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13393
ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13393 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_13393.map.gz / 形式: CCP4 / 大きさ: 396.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_13393.map.gz / 形式: CCP4 / 大きさ: 396.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) emd_13393_msk_1.map
emd_13393_msk_1.map 試料の構成要素
試料の構成要素 Homo sapiens (ヒト)
Homo sapiens (ヒト) Homo sapiens (ヒト)
Homo sapiens (ヒト)
 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 ムービー
ムービー コントローラー
コントローラー
























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)