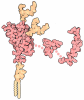
登録情報 データベース : EMDB / ID : EMD-10204タイトル Abeta fibril (Morphology I) ABeta(1-40) Morphology I 組織 : meningesタンパク質・ペプチド : Amyloid-beta precursor protein / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト)手法 / / 解像度 : 4.4 Å Kollmer M / Fandrich M 資金援助 Organization Grant number 国 German Research Foundation FA456/12-1 German Research Foundation FA456/24-1
ジャーナル : Nat Commun / 年 : 2019タイトル : Cryo-EM structure and polymorphism of Aβ amyloid fibrils purified from Alzheimer's brain tissue.著者 : Marius Kollmer / William Close / Leonie Funk / Jay Rasmussen / Aref Bsoul / Angelika Schierhorn / Matthias Schmidt / Christina J Sigurdson / Mathias Jucker / Marcus Fändrich / 要旨 : The formation of Aβ amyloid fibrils is a neuropathological hallmark of Alzheimer's disease and cerebral amyloid angiopathy. However, the structure of Aβ amyloid fibrils from brain tissue is poorly ... The formation of Aβ amyloid fibrils is a neuropathological hallmark of Alzheimer's disease and cerebral amyloid angiopathy. However, the structure of Aβ amyloid fibrils from brain tissue is poorly understood. Here we report the purification of Aβ amyloid fibrils from meningeal Alzheimer's brain tissue and their structural analysis with cryo-electron microscopy. We show that these fibrils are polymorphic but consist of similarly structured protofilaments. Brain derived Aβ amyloid fibrils are right-hand twisted and their peptide fold differs sharply from previously analyzed Aβ fibrils that were formed in vitro. These data underscore the importance to use patient-derived amyloid fibrils when investigating the structural basis of the disease. 履歴 登録 2019年8月8日 - ヘッダ(付随情報) 公開 2019年11月6日 - マップ公開 2019年11月6日 - 更新 2024年5月22日 - 現状 2024年5月22日 処理サイト : PDBe / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) データ登録者
データ登録者 ドイツ, 2件
ドイツ, 2件  引用
引用 ジャーナル: Nat Commun / 年: 2019
ジャーナル: Nat Commun / 年: 2019


 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_10204.map.gz
emd_10204.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-10204-v30.xml
emd-10204-v30.xml emd-10204.xml
emd-10204.xml EMDBヘッダ
EMDBヘッダ emd_10204_fsc.xml
emd_10204_fsc.xml FSCデータファイル
FSCデータファイル emd_10204.png
emd_10204.png emd-10204.cif.gz
emd-10204.cif.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-10204
http://ftp.pdbj.org/pub/emdb/structures/EMD-10204 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10204
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10204 emd_10204_validation.pdf.gz
emd_10204_validation.pdf.gz EMDB検証レポート
EMDB検証レポート emd_10204_full_validation.pdf.gz
emd_10204_full_validation.pdf.gz emd_10204_validation.xml.gz
emd_10204_validation.xml.gz emd_10204_validation.cif.gz
emd_10204_validation.cif.gz https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10204
https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10204 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10204
ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10204 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_10204.map.gz / 形式: CCP4 / 大きさ: 12.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_10204.map.gz / 形式: CCP4 / 大きさ: 12.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) 試料の構成要素
試料の構成要素 Homo sapiens (ヒト) / 器官: brain / 組織: meninges
Homo sapiens (ヒト) / 器官: brain / 組織: meninges Homo sapiens (ヒト) / 器官: BRAIN / 組織: meninges
Homo sapiens (ヒト) / 器官: BRAIN / 組織: meninges 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 画像解析
画像解析
 ムービー
ムービー コントローラー
コントローラー






























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















