+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6zcf | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
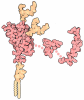
| タイトル | Amyloid fibril morphology i (in vitro) from murine SAA1.1 protein | |||||||||||||||||||||
 要素 要素 | Serum amyloid A-2 protein | |||||||||||||||||||||
 キーワード キーワード | PROTEIN FIBRIL / systemic amyloidosis / misfolding disease / inflammation / prion | |||||||||||||||||||||
| 機能・相同性 | Serum amyloid A protein / Serum amyloid A protein / Serum amyloid A proteins signature. / Serum amyloid A proteins / response to stilbenoid / high-density lipoprotein particle / acute-phase response / Serum amyloid A-2 protein 機能・相同性情報 機能・相同性情報 | |||||||||||||||||||||
| 生物種 |  | |||||||||||||||||||||
| 手法 | 電子顕微鏡法 / らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 2.73 Å | |||||||||||||||||||||
 データ登録者 データ登録者 | Bansal, A. / Schmidt, M. / Faendrich, M. | |||||||||||||||||||||
| 資金援助 |  ドイツ, 6件 ドイツ, 6件
| |||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2021 ジャーナル: Nat Commun / 年: 2021タイトル: AA amyloid fibrils from diseased tissue are structurally different from in vitro formed SAA fibrils. 著者: Akanksha Bansal / Matthias Schmidt / Matthies Rennegarbe / Christian Haupt / Falk Liberta / Sabrina Stecher / Ioana Puscalau-Girtu / Alexander Biedermann / Marcus Fändrich /  要旨: Systemic AA amyloidosis is a world-wide occurring protein misfolding disease of humans and animals. It arises from the formation of amyloid fibrils from serum amyloid A (SAA) protein. Using cryo ...Systemic AA amyloidosis is a world-wide occurring protein misfolding disease of humans and animals. It arises from the formation of amyloid fibrils from serum amyloid A (SAA) protein. Using cryo electron microscopy we here show that amyloid fibrils which were purified from AA amyloidotic mice are structurally different from fibrils formed from recombinant SAA protein in vitro. Ex vivo amyloid fibrils consist of fibril proteins that contain more residues within their ordered parts and possess a higher β-sheet content than in vitro fibril proteins. They are also more resistant to proteolysis than their in vitro formed counterparts. These data suggest that pathogenic amyloid fibrils may originate from proteolytic selection, allowing specific fibril morphologies to proliferate and to cause damage to the surrounding tissue. | |||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6zcf.cif.gz 6zcf.cif.gz | 92.9 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6zcf.ent.gz pdb6zcf.ent.gz | 69.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6zcf.json.gz 6zcf.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  6zcf_validation.pdf.gz 6zcf_validation.pdf.gz | 1 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  6zcf_full_validation.pdf.gz 6zcf_full_validation.pdf.gz | 1 MB | 表示 | |
| XML形式データ |  6zcf_validation.xml.gz 6zcf_validation.xml.gz | 21.8 KB | 表示 | |
| CIF形式データ |  6zcf_validation.cif.gz 6zcf_validation.cif.gz | 29.9 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/zc/6zcf https://data.pdbj.org/pub/pdb/validation_reports/zc/6zcf ftp://data.pdbj.org/pub/pdb/validation_reports/zc/6zcf ftp://data.pdbj.org/pub/pdb/validation_reports/zc/6zcf | HTTPS FTP |
-関連構造データ
| 関連構造データ |  11162MC  6zcgC  6zchC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-11027 (タイトル: Cryo electron microscopy of in vitro recombinant SAA1.1 amyloid fibrils EMPIAR-11027 (タイトル: Cryo electron microscopy of in vitro recombinant SAA1.1 amyloid fibrilsData size: 525.4 Data #1: Unaligned multiframe micrographs of ex-vivo murine SAA1 [micrographs - multiframe] Data #2: Thumbnails for micrographs of ex-vivo murine SAA1 [micrographs - single frame]) |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 11622.629 Da / 分子数: 12 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: HELICAL ARRAY / 3次元再構成法: らせん対称体再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Serum amyloid A1 (SAA1) amyloid fibril / タイプ: COMPLEX / 詳細: in vitro murine SAA amyloid fibril morphology i / Entity ID: all / 由来: RECOMBINANT |
|---|---|
| 分子量 | 単位: KILODALTONS/NANOMETER |
| 由来(天然) | 生物種:  |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 8.5 / 詳細: 10mM Tris(hydroxymethyl)aminomethane (Tris) |
| 緩衝液成分 | 濃度: 10 mM / 名称: Tris(hydroxymethyl)aminomethane / 式: (HOCH2)3CNH2 |
| 試料 | 濃度: 0.2 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 急速凍結 | 装置: FEI VITROBOT MARK III / 凍結剤: ETHANE / 湿度: 96 % |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / Cs: 2.7 mm |
| 試料ホルダ | 凍結剤: NITROGEN |
| 撮影 | 平均露光時間: 12 sec. / 電子線照射量: 40 e/Å2 / 検出モード: COUNTING フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) |
| 画像スキャン | 動画フレーム数/画像: 40 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||
| らせん対称 | 回転角度/サブユニット: 178.93 ° / 軸方向距離/サブユニット: 2.3719 Å / らせん対称軸の対称性: C1 | ||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 94220 | ||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.73 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 93347 / 対称性のタイプ: HELICAL | ||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: BACKBONE TRACE / 空間: REAL / Target criteria: correlation coefficient |
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj