+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0425 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | T.elongatus NDH (data-set 2) | ||||||||||||
 マップデータ マップデータ | pixel spacing resized to match EMD-415 | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | photosynthesis / bioenergetics / membrane protein complex / OXIDOREDUCTASE | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報トランスロカーゼ; ヒドロンの輸送の触媒; 酸化還元酵素反応を伴う / NADH dehydrogenase complex / transmembrane transporter complex / photosynthetic electron transport chain / oxidoreductase activity, acting on NAD(P)H, quinone or similar compound as acceptor / plasma membrane-derived thylakoid membrane / photosynthesis, light reaction / ubiquinone binding / electron transport coupled proton transport / NADH dehydrogenase activity ...トランスロカーゼ; ヒドロンの輸送の触媒; 酸化還元酵素反応を伴う / NADH dehydrogenase complex / transmembrane transporter complex / photosynthetic electron transport chain / oxidoreductase activity, acting on NAD(P)H, quinone or similar compound as acceptor / plasma membrane-derived thylakoid membrane / photosynthesis, light reaction / ubiquinone binding / electron transport coupled proton transport / NADH dehydrogenase activity / respiratory chain complex I / NADH dehydrogenase (ubiquinone) activity / quinone binding / ATP synthesis coupled electron transport / endomembrane system / aerobic respiration / NAD binding / 4 iron, 4 sulfur cluster binding / iron ion binding / membrane / plasma membrane 類似検索 - 分子機能 | ||||||||||||
| 生物種 |   Thermosynechococcus elongatus BP-1 (バクテリア) / Thermosynechococcus elongatus BP-1 (バクテリア) /   Thermosynechococcus elongatus (strain BP-1) (バクテリア) Thermosynechococcus elongatus (strain BP-1) (バクテリア) | ||||||||||||
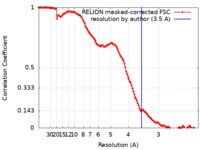
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.5 Å | ||||||||||||
 データ登録者 データ登録者 | Laughlin TG / Bayne A | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2019 ジャーナル: Nature / 年: 2019タイトル: Structure of the complex I-like molecule NDH of oxygenic photosynthesis. 著者: Thomas G Laughlin / Andrew N Bayne / Jean-François Trempe / David F Savage / Karen M Davies /   要旨: Cyclic electron flow around photosystem I (PSI) is a mechanism by which photosynthetic organisms balance the levels of ATP and NADPH necessary for efficient photosynthesis. NAD(P)H dehydrogenase-like ...Cyclic electron flow around photosystem I (PSI) is a mechanism by which photosynthetic organisms balance the levels of ATP and NADPH necessary for efficient photosynthesis. NAD(P)H dehydrogenase-like complex (NDH) is a key component of this pathway in most oxygenic photosynthetic organisms and is the last large photosynthetic membrane-protein complex for which the structure remains unknown. Related to the respiratory NADH dehydrogenase complex (complex I), NDH transfers electrons originating from PSI to the plastoquinone pool while pumping protons across the thylakoid membrane, thereby increasing the amount of ATP produced per NADP molecule reduced. NDH possesses 11 of the 14 core complex I subunits, as well as several oxygenic-photosynthesis-specific (OPS) subunits that are conserved from cyanobacteria to plants. However, the three core complex I subunits that are involved in accepting electrons from NAD(P)H are notably absent in NDH, and it is therefore not clear how NDH acquires and transfers electrons to plastoquinone. It is proposed that the OPS subunits-specifically NdhS-enable NDH to accept electrons from its electron donor, ferredoxin. Here we report a 3.1 Å structure of the 0.42-MDa NDH complex from the thermophilic cyanobacterium Thermosynechococcus elongatus BP-1, obtained by single-particle cryo-electron microscopy. Our maps reveal the structure and arrangement of the principal OPS subunits in the NDH complex, as well as an unexpected cofactor close to the plastoquinone-binding site in the peripheral arm. The location of the OPS subunits supports a role in electron transfer and defines two potential ferredoxin-binding sites at the apex of the peripheral arm. These results suggest that NDH could possess several electron transfer routes, which would serve to maximize plastoquinone reduction and avoid deleterious off-target chemistry of the semi-plastoquinone radical. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0425.map.gz emd_0425.map.gz | 148.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0425-v30.xml emd-0425-v30.xml emd-0425.xml emd-0425.xml | 40.2 KB 40.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_0425_fsc.xml emd_0425_fsc.xml | 12.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_0425.png emd_0425.png | 138.9 KB | ||
| マスクデータ |  emd_0425_msk_1.map emd_0425_msk_1.map | 178 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-0425.cif.gz emd-0425.cif.gz | 9.8 KB | ||
| その他 |  emd_0425_half_map_1.map.gz emd_0425_half_map_1.map.gz emd_0425_half_map_2.map.gz emd_0425_half_map_2.map.gz | 141.2 MB 141.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0425 http://ftp.pdbj.org/pub/emdb/structures/EMD-0425 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0425 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0425 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0425_validation.pdf.gz emd_0425_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0425_full_validation.pdf.gz emd_0425_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_0425_validation.xml.gz emd_0425_validation.xml.gz | 21.4 KB | 表示 | |
| CIF形式データ |  emd_0425_validation.cif.gz emd_0425_validation.cif.gz | 27 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0425 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0425 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0425 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0425 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6nbxMC  0415C  0416C  0417C  0418C  0419C  0420C  6nbqC  6nbyC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10257 (タイトル: Structure of NDH the complex I-like molecule of photosynthesis EMPIAR-10257 (タイトル: Structure of NDH the complex I-like molecule of photosynthesisData size: 1.8 TB Data #1: Unaligned multiframe micrographs for NDH dataset1 [micrographs - multiframe] Data #2: Unaligned multiframe micrographs for NDH dataset2 [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0425.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0425.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | pixel spacing resized to match EMD-415 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.068 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
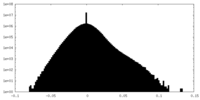
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_0425_msk_1.map emd_0425_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
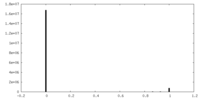
| 投影像・断面図 |
| ||||||||||||
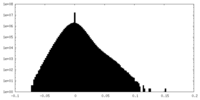
| 密度ヒストグラム |
-ハーフマップ: binned relative to original particle images
| ファイル | emd_0425_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | binned relative to original particle images | ||||||||||||
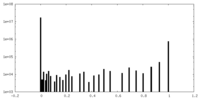
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: em-half-volume P2
| ファイル | emd_0425_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | em-half-volume_P2 | ||||||||||||
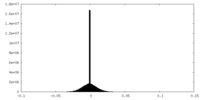
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : NAD(P)H dehydrogenase-like complex (NDH/NDH-1_1/NDH1L)from T.elongatus
+超分子 #1: NAD(P)H dehydrogenase-like complex (NDH/NDH-1_1/NDH1L)from T.elongatus
+分子 #1: NAD(P)H-quinone oxidoreductase subunit 1
+分子 #2: NAD(P)H-quinone oxidoreductase subunit 2
+分子 #3: NAD(P)H-quinone oxidoreductase subunit 3
+分子 #4: NAD(P)H-quinone oxidoreductase chain 4 1
+分子 #5: NAD(P)H-quinone oxidoreductase subunit 4L
+分子 #6: NADH dehydrogenase subunit 5
+分子 #7: NADH-quinone oxidoreductase subunit J
+分子 #8: NAD(P)H-quinone oxidoreductase subunit H
+分子 #9: NAD(P)H-quinone oxidoreductase subunit I
+分子 #10: NAD(P)H-quinone oxidoreductase subunit J
+分子 #11: NAD(P)H-quinone oxidoreductase subunit K
+分子 #12: NAD(P)H-quinone oxidoreductase subunit L
+分子 #13: NAD(P)H-quinone oxidoreductase subunit M
+分子 #14: NAD(P)H-quinone oxidoreductase subunit N
+分子 #15: NAD(P)H-quinone oxidoreductase subunit O
+分子 #16: Proton-translocating NADH-quinone dehydrogenase subunit P NdhP
+分子 #17: Proton-translocating NADH-quinone dehydrogenase subunit Q NdhQ
+分子 #18: Tlr0636 protein
+分子 #19: IRON/SULFUR CLUSTER
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.03 mg/mL | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 6 構成要素:
| ||||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 7 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 15 sec. / 前処理 - 雰囲気: OTHER | ||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV 詳細: incubate on grid for 30 seconds and blot 2.5 seconds before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 25 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-30 / 撮影したグリッド数: 1 / 実像数: 1385 / 平均露光時間: 0.2 sec. / 平均電子線量: 60.0 e/Å2 / 詳細: Three image per hole, focusing once per hole. |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)