+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Co-structure of the Respiratory Syncytial Virus RNA-dependent RNA polymerase with MRK-1 | |||||||||
 マップデータ マップデータ | sharpened map used for model building and real space refinement | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | RNA-BINDING PROTEIN / RSV / RDRP / RNA-DEPENDENT RNA POLYMERASE / PRNTASE / POLYRIBONUCLEOTIDYL TRANSFERASE / RNA CAPPING / VIRAL REPLICATION / VIRAL PROTEIN / REPLICATION | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報NNS virus cap methyltransferase / GDP polyribonucleotidyltransferase / Respiratory syncytial virus genome transcription / Translation of respiratory syncytial virus mRNAs / negative stranded viral RNA replication / Respiratory syncytial virus genome replication / RSV-host interactions / Assembly and release of respiratory syncytial virus (RSV) virions / Maturation of hRSV A proteins / 加水分解酵素; 酸無水物に作用; リン含有酸無水物に作用 ...NNS virus cap methyltransferase / GDP polyribonucleotidyltransferase / Respiratory syncytial virus genome transcription / Translation of respiratory syncytial virus mRNAs / negative stranded viral RNA replication / Respiratory syncytial virus genome replication / RSV-host interactions / Assembly and release of respiratory syncytial virus (RSV) virions / Maturation of hRSV A proteins / 加水分解酵素; 酸無水物に作用; リン含有酸無水物に作用 / Respiratory syncytial virus (RSV) attachment and entry / viral life cycle / virion component / mRNA 5'-cap (guanine-N7-)-methyltransferase activity / host cell cytoplasm / RNA-directed RNA polymerase / RNA-dependent RNA polymerase activity / GTPase activity / ATP binding / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  Human orthopneumovirus (ウイルス) / Human orthopneumovirus (ウイルス) /  Human respiratory syncytial virus A2 (ウイルス) Human respiratory syncytial virus A2 (ウイルス) | |||||||||
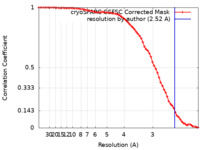
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.52 Å | |||||||||
 データ登録者 データ登録者 | Fischmann TO | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2023 ジャーナル: Commun Biol / 年: 2023タイトル: Conserved allosteric inhibitory site on the respiratory syncytial virus and human metapneumovirus RNA-dependent RNA polymerases. 著者: Victoria A Kleiner / Thierry O Fischmann / John A Howe / Douglas C Beshore / Michael J Eddins / Yan Hou / Todd Mayhood / Daniel Klein / Debbie D Nahas / Bob J Lucas / He Xi / Edward Murray / ...著者: Victoria A Kleiner / Thierry O Fischmann / John A Howe / Douglas C Beshore / Michael J Eddins / Yan Hou / Todd Mayhood / Daniel Klein / Debbie D Nahas / Bob J Lucas / He Xi / Edward Murray / Daphne Y Ma / Krista Getty / Rachel Fearns /  要旨: Respiratory syncytial virus (RSV) and human metapneumovirus (HMPV) are related RNA viruses responsible for severe respiratory infections and resulting disease in infants, elderly, and ...Respiratory syncytial virus (RSV) and human metapneumovirus (HMPV) are related RNA viruses responsible for severe respiratory infections and resulting disease in infants, elderly, and immunocompromised adults. Therapeutic small molecule inhibitors that bind to the RSV polymerase and inhibit viral replication are being developed, but their binding sites and molecular mechanisms of action remain largely unknown. Here we report a conserved allosteric inhibitory site identified on the L polymerase proteins of RSV and HMPV that can be targeted by a dual-specificity, non-nucleoside inhibitor, termed MRK-1. Cryo-EM structures of the inhibitor in complexes with truncated RSV and full-length HMPV polymerase proteins provide a structural understanding of how MRK-1 is active against both viruses. Functional analyses indicate that MRK-1 inhibits conformational changes necessary for the polymerase to engage in RNA synthesis initiation and to transition into an elongation mode. Competition studies reveal that the MRK-1 binding pocket is distinct from that of a capping inhibitor with an overlapping resistance profile, suggesting that the polymerase conformation bound by MRK-1 may be distinct from that involved in mRNA capping. These findings should facilitate optimization of dual RSV and HMPV replication inhibitors and provide insights into the molecular mechanisms underlying their polymerase activities. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29365.map.gz emd_29365.map.gz | 28.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29365-v30.xml emd-29365-v30.xml emd-29365.xml emd-29365.xml | 17.6 KB 17.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_29365_fsc.xml emd_29365_fsc.xml | 6.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_29365.png emd_29365.png | 130.1 KB | ||
| Filedesc metadata |  emd-29365.cif.gz emd-29365.cif.gz | 6.8 KB | ||
| その他 |  emd_29365_half_map_1.map.gz emd_29365_half_map_1.map.gz emd_29365_half_map_2.map.gz emd_29365_half_map_2.map.gz | 28.4 MB 28.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29365 http://ftp.pdbj.org/pub/emdb/structures/EMD-29365 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29365 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29365 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_29365_validation.pdf.gz emd_29365_validation.pdf.gz | 815 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_29365_full_validation.pdf.gz emd_29365_full_validation.pdf.gz | 814.6 KB | 表示 | |
| XML形式データ |  emd_29365_validation.xml.gz emd_29365_validation.xml.gz | 14.2 KB | 表示 | |
| CIF形式データ |  emd_29365_validation.cif.gz emd_29365_validation.cif.gz | 18.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29365 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29365 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29365 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29365 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8fpiMC  8fpjC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29365.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29365.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | sharpened map used for model building and real space refinement | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||
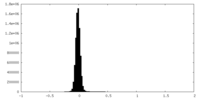
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: half map
| ファイル | emd_29365_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map | ||||||||||||
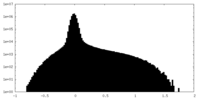
| 投影像・断面図 |
| ||||||||||||
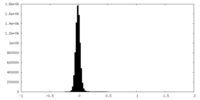
| 密度ヒストグラム |
-ハーフマップ: half map
| ファイル | emd_29365_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map | ||||||||||||
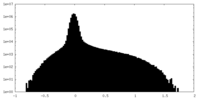
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : RESPIRATORY SYNCYTIAL VIRUS POLYMERASE (L) PROTEIN BOUND BY THE T...
| 全体 | 名称: RESPIRATORY SYNCYTIAL VIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAMERIC PHOSPHOPROTEIN (P) AND COMPLEXED WITH MRK-1 |
|---|---|
| 要素 |
|
-超分子 #1: RESPIRATORY SYNCYTIAL VIRUS POLYMERASE (L) PROTEIN BOUND BY THE T...
| 超分子 | 名称: RESPIRATORY SYNCYTIAL VIRUS POLYMERASE (L) PROTEIN BOUND BY THE TETRAMERIC PHOSPHOPROTEIN (P) AND COMPLEXED WITH MRK-1 タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #2 |
|---|---|
| 由来(天然) | 生物種:  Human orthopneumovirus (ウイルス) Human orthopneumovirus (ウイルス) |
-分子 #1: RNA-directed RNA polymerase L
| 分子 | 名称: RNA-directed RNA polymerase L / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: RNA-directed RNA polymerase |
|---|---|
| 由来(天然) | 生物種:  Human respiratory syncytial virus A2 (ウイルス) Human respiratory syncytial virus A2 (ウイルス) |
| 分子量 | 理論値: 173.267922 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSDYKDHDG DYKDHDIDYK DDDDKGSGSL EVLFQGPMDP IINGNSANVY LTDSYLKGVI SFSECNALGS YIFNGPYLKN DYTNLISRQ NPLIEHMNLK KLNITQSLIS KYHKGEIKLE EPTYFQSLLM TYKSMTSSEQ IATTNLLKKI IRRAIEISDV K VYAILNKL ...文字列: MGSDYKDHDG DYKDHDIDYK DDDDKGSGSL EVLFQGPMDP IINGNSANVY LTDSYLKGVI SFSECNALGS YIFNGPYLKN DYTNLISRQ NPLIEHMNLK KLNITQSLIS KYHKGEIKLE EPTYFQSLLM TYKSMTSSEQ IATTNLLKKI IRRAIEISDV K VYAILNKL GLKEKDKIKS NNGQDEDNSV ITTIIKDDIL SAVKDNQSHL KADKNHSTKQ KDTIKTTLLK KLMCSMQHPP SW LIHWFNL YTKLNNILTQ YRSNEVKNHG FTLIDNQTLS GFQFILNQYG CIVYHKELKR ITVTTYNQFL TWKDISLSRL NVC LITWIS NCLNTLNKSL GLRCGFNNVI LTQLFLYGDC ILKLFHNEGF YIIKEVEGFI MSLILNITEE DQFRKRFYNS MLNN ITDAA NKAQKNLLSR VCHTLLDKTV SDNIINGRWI ILLSKFLKLI KLAGDNNLNN LSELYFLFRI FGHPMVDERQ AMDAV KINC NETKFYLLSS LSMLRGAFIY RIIKGFVNNY NRWPTLRNAI VLPLRWLTYY KLNTYPSLLE LTERDLIVLS GLRFYR EFR LPKKVDLEMI INDKAISPPK NLIWTSFPRN YMPSHIQNYI EHEKLKFSES DKSRRVLEYY LRDNKFNECD LYNCVVN QS YLNNPNHVVS LTGKERELSV GRMFAMQPGM FRQVQILAEK MIAENILQFF PESLTRYGDL ELQKILELKA GISNKSNR Y NDNYNNYISK CSIITDLSKF NQAFRYETSC ICSDVLDELH GVQSLFSWLH LTIPHVTIIC TYRHAPPYIG DHIVDLNNV DEQSGLYRYH MGGIEGWCQK LWTIEAISLL DLISLKGKFS ITALINGDNQ SIDISKPIRL MEGQTHAQAD YLLALNSLKL LYKEYAGIG HKLKGTETYI SRDMQFMSKT IQHNGVYYPA SIKKVLRVGP WINTILDDFK VSLESIGSLT QELEYRGESL L CSLIFRNV WLYNQIALQL KNHALCNNKL YLDILKVLKH LKTFFNLDNI DTALTLYMNL PMLFGGGDPN LLYRSFYRRT PD FLTEAIV HSVFILSYYT NHDLKDKLQD LSDDRLNKFL TCIITFDKNP NAEFVTLMRD PQALGSERQA KITSEINRLA VTE VLSTAP NKIFSKSAQH YTTTEIDLND IMQNIEPTYP HGLRVVYESL PFYKAEKIVN LISGTKSITN ILEKTSAIDL TDID RATEM MRKNITLLIR ILPLDCNRDK REILSMENLS ITELSKYVRE RSWSLSNIVG VTSPSIMYTM DIKYTTSTIS SGIII EKYN VNSLTRGERG PTKPWVGSST QEKKTMPVYN RQVLTKKQRD QIDLLAKLDW VYASIDNKDE FMEELSIGTL GLTYEK AKK LFPQYLSVNY LHRLTVSSRP CEFPASIPAY RTTNYHFDTS PINRILTEKY GDEDIDIVFQ NCISFGLSLM SVVEQFT NV CPNRIILIPK LNEIHLMKPP IFTGDVDIHK LKQVIQKQHM FLPDKISLTQ YVELF UniProtKB: RNA-directed RNA polymerase L |
-分子 #2: Phosphoprotein
| 分子 | 名称: Phosphoprotein / タイプ: protein_or_peptide / ID: 2 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Human respiratory syncytial virus A2 (ウイルス) Human respiratory syncytial virus A2 (ウイルス) |
| 分子量 | 理論値: 29.062895 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MEKFAPEFHG EDANNRATKF LESIKGKFTS PKDPKKKDSI ISVNSIDIEV TKESPITSNS TIINPTNETD DTAGNKPNYQ RKPLVSFKE DPTPSDNPFS KLYKETIETF DNNEEESSYS YEEINDQTND NITARLDRID EKLSEILGML HTLVVASAGP T SARDGIRD ...文字列: MEKFAPEFHG EDANNRATKF LESIKGKFTS PKDPKKKDSI ISVNSIDIEV TKESPITSNS TIINPTNETD DTAGNKPNYQ RKPLVSFKE DPTPSDNPFS KLYKETIETF DNNEEESSYS YEEINDQTND NITARLDRID EKLSEILGML HTLVVASAGP T SARDGIRD AMIGLREEMI EKIRTEALMT NDRLEAMARL RNEESEKMAK DTSDEVSLNP TSEKLNNLLE GNDSDNDLSL ED FKGENKY FQGHHHHHH UniProtKB: Phosphoprotein |
-分子 #3: 4-(2-aminopropan-2-yl)-N'-[4-(cyclopropyloxy)-3-methoxybenzoyl]-6...
| 分子 | 名称: 4-(2-aminopropan-2-yl)-N'-[4-(cyclopropyloxy)-3-methoxybenzoyl]-6-(4-fluorophenyl)pyridine-2-carbohydrazide タイプ: ligand / ID: 3 / コピー数: 1 / 式: Y6L |
|---|---|
| 分子量 | 理論値: 478.515 Da |
| Chemical component information | 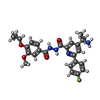 ChemComp-Y6L: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.6 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 平均電子線量: 34.5 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL |
|---|---|
| 得られたモデル |  PDB-8fpi: |
 ムービー
ムービー コントローラー
コントローラー






 Z
Z Y
Y X
X