+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-12177 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | The H/ACA RNP lobe of human telomerase | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | H/ACA RNP / ribonucleoprotein / complex / RNA / RNA BINDING PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報telomere formation via telomerase / box H/ACA scaRNP complex / box H/ACA telomerase RNP complex / telomerase RNA localization to Cajal body / protein localization to Cajal body / Cajal body organization / snoRNA guided rRNA pseudouridine synthesis / box H/ACA snoRNP complex / 異性化酵素; 分子内転位酵素; ムターゼ; その他の基を移すもの / rRNA pseudouridine synthesis ...telomere formation via telomerase / box H/ACA scaRNP complex / box H/ACA telomerase RNP complex / telomerase RNA localization to Cajal body / protein localization to Cajal body / Cajal body organization / snoRNA guided rRNA pseudouridine synthesis / box H/ACA snoRNP complex / 異性化酵素; 分子内転位酵素; ムターゼ; その他の基を移すもの / rRNA pseudouridine synthesis / box H/ACA sno(s)RNA 3'-end processing / pseudouridine synthesis / snRNA pseudouridine synthesis / telomerase RNA stabilization / enzyme-directed rRNA pseudouridine synthesis / box H/ACA snoRNA binding / regulation of telomerase RNA localization to Cajal body / mRNA pseudouridine synthesis / pseudouridine synthase activity / telomerase activity / scaRNA localization to Cajal body / positive regulation of establishment of protein localization to telomere / positive regulation of protein localization to Cajal body / positive regulation of telomerase RNA localization to Cajal body / sno(s)RNA-containing ribonucleoprotein complex / telomerase holoenzyme complex / telomerase RNA binding / rRNA modification in the nucleus and cytosol / positive regulation of double-strand break repair / positive regulation of double-strand break repair via nonhomologous end joining / Association of TriC/CCT with target proteins during biosynthesis / Telomere Extension By Telomerase / RNA folding / positive regulation of double-strand break repair via homologous recombination / telomere maintenance via telomerase / RNA processing / Cajal body / : / positive regulation of telomere maintenance via telomerase / positive regulation of DNA repair / maturation of LSU-rRNA / fibrillar center / rRNA processing / site of double-strand break / histone binding / protein-folding chaperone binding / cytosolic large ribosomal subunit / chromosome, telomeric region / nuclear body / DNA repair / ubiquitin protein ligase binding / protein-containing complex binding / nucleolus / RNA binding / nucleoplasm / identical protein binding / nucleus / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
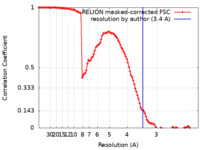
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.4 Å | |||||||||
 データ登録者 データ登録者 | Nguyen THD / Ghanim GE | |||||||||
| 資金援助 |  英国, 英国,  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2021 ジャーナル: Nature / 年: 2021タイトル: Structure of human telomerase holoenzyme with bound telomeric DNA. 著者: George E Ghanim / Adam J Fountain / Anne-Marie M van Roon / Ramya Rangan / Rhiju Das / Kathleen Collins / Thi Hoang Duong Nguyen /   要旨: Telomerase adds telomeric repeats at chromosome ends to compensate for the telomere loss that is caused by incomplete genome end replication. In humans, telomerase is upregulated during embryogenesis ...Telomerase adds telomeric repeats at chromosome ends to compensate for the telomere loss that is caused by incomplete genome end replication. In humans, telomerase is upregulated during embryogenesis and in cancers, and mutations that compromise the function of telomerase result in disease. A previous structure of human telomerase at a resolution of 8 Å revealed a vertebrate-specific composition and architecture, comprising a catalytic core that is flexibly tethered to an H and ACA (hereafter, H/ACA) box ribonucleoprotein (RNP) lobe by telomerase RNA. High-resolution structural information is necessary to develop treatments that can effectively modulate telomerase activity as a therapeutic approach against cancers and disease. Here we used cryo-electron microscopy to determine the structure of human telomerase holoenzyme bound to telomeric DNA at sub-4 Å resolution, which reveals crucial DNA- and RNA-binding interfaces in the active site of telomerase as well as the locations of mutations that alter telomerase activity. We identified a histone H2A-H2B dimer within the holoenzyme that was bound to an essential telomerase RNA motif, which suggests a role for histones in the folding and function of telomerase RNA. Furthermore, this structure of a eukaryotic H/ACA RNP reveals the molecular recognition of conserved RNA and protein motifs, as well as interactions that are crucial for understanding the molecular pathology of many mutations that cause disease. Our findings provide the structural details of the assembly and active site of human telomerase, which paves the way for the development of therapeutic agents that target this enzyme. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_12177.map.gz emd_12177.map.gz | 95.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-12177-v30.xml emd-12177-v30.xml emd-12177.xml emd-12177.xml | 26 KB 26 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_12177_fsc.xml emd_12177_fsc.xml | 10.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_12177.png emd_12177.png | 107.4 KB | ||
| Filedesc metadata |  emd-12177.cif.gz emd-12177.cif.gz | 7.8 KB | ||
| その他 |  emd_12177_half_map_1.map.gz emd_12177_half_map_1.map.gz emd_12177_half_map_2.map.gz emd_12177_half_map_2.map.gz | 80.7 MB 80.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-12177 http://ftp.pdbj.org/pub/emdb/structures/EMD-12177 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12177 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-12177 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_12177_validation.pdf.gz emd_12177_validation.pdf.gz | 933.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_12177_full_validation.pdf.gz emd_12177_full_validation.pdf.gz | 933.1 KB | 表示 | |
| XML形式データ |  emd_12177_validation.xml.gz emd_12177_validation.xml.gz | 17.2 KB | 表示 | |
| CIF形式データ |  emd_12177_validation.cif.gz emd_12177_validation.cif.gz | 21.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12177 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12177 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12177 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-12177 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7bgbMC  7bg9C C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10732 (タイトル: Structure of human telomerase holoenzyme with bound telomeric DNA EMPIAR-10732 (タイトル: Structure of human telomerase holoenzyme with bound telomeric DNAData size: 11.2 TB Data #1: Unaligned multiframe micrographs of human telomerase holoenzyme bound to a telomeric DNA [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_12177.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_12177.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.11 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-ハーフマップ: #1
| ファイル | emd_12177_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
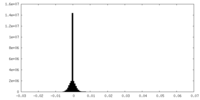
| 投影像・断面図 |
| ||||||||||||
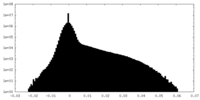
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_12177_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
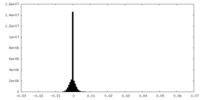
| 投影像・断面図 |
| ||||||||||||
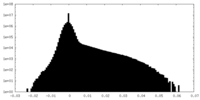
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human telomerase H/ACA RNP lobe
| 全体 | 名称: Human telomerase H/ACA RNP lobe |
|---|---|
| 要素 |
|
-超分子 #1: Human telomerase H/ACA RNP lobe
| 超分子 | 名称: Human telomerase H/ACA RNP lobe / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#6 詳細: The hTR H/ACA motif, which adopts a double-hairpin structure hinged by the H-box and flanked by the ACA box, scaffolds the assembly of two copies each of dyskerin, NHP2, NOP10 and GAR1, one ...詳細: The hTR H/ACA motif, which adopts a double-hairpin structure hinged by the H-box and flanked by the ACA box, scaffolds the assembly of two copies each of dyskerin, NHP2, NOP10 and GAR1, one on each hairpin. TCAB1 binds the CAB box. |
|---|
-超分子 #2: ribonucleoprotein and telomerase complex
| 超分子 | 名称: ribonucleoprotein and telomerase complex / タイプ: complex / ID: 2 / 親要素: 1 / 詳細: 1,2,3,5,6 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-超分子 #3: RNA
| 超分子 | 名称: RNA / タイプ: complex / ID: 3 / 親要素: 1 / 詳細: 4 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Telomerase Cajal body protein 1
| 分子 | 名称: Telomerase Cajal body protein 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 59.35707 KDa |
| 配列 | 文字列: MKTLETQPLA PDCCPSDQDP APAHPSPHAS PMNKNADSEL MPPPPERGDP PRLSPDPVAG SAVSQELREG DPVSLSTPLE TEFGSPSEL SPRIEEQELS ENTSLPAEEA NGSLSEEEAN GPELGSGKAM EDTSGEPAAE DEGDTAWNYS FSQLPRFLSG S WSEFSTQP ...文字列: MKTLETQPLA PDCCPSDQDP APAHPSPHAS PMNKNADSEL MPPPPERGDP PRLSPDPVAG SAVSQELREG DPVSLSTPLE TEFGSPSEL SPRIEEQELS ENTSLPAEEA NGSLSEEEAN GPELGSGKAM EDTSGEPAAE DEGDTAWNYS FSQLPRFLSG S WSEFSTQP ENFLKGCKWA PDGSCILTNS ADNILRIYNL PPELYHEGEQ VEYAEMVPVL RMVEGDTIYD YCWYSLMSSA QP DTSYVAS SSRENPIHIW DAFTGELRAS FRAYNHLDEL TAAHSLCFSP DGSQLFCGFN RTVRVFSTAR PGRDCEVRAT FAK KQGQSG IISCIAFSPA QPLYACGSYG RSLGLYAWDD GSPLALLGGH QGGITHLCFH PDGNRFFSGA RKDAELLCWD LRQS GYPLW SLGREVTTNQ RIYFDLDPTG QFLVSGSTSG AVSVWDTDGP GNDGKPEPVL SFLPQKDCTN GVSLHPSLPL LATAS GQRV FPEPTESGDE GEELGLPLLS TRHVHLECRL QLWWCGGAPD SSIPDDHQGE KGQGGTEGGV GELI UniProtKB: Telomerase Cajal body protein 1 |
-分子 #2: H/ACA ribonucleoprotein complex subunit DKC1
| 分子 | 名称: H/ACA ribonucleoprotein complex subunit DKC1 / タイプ: protein_or_peptide / ID: 2 / コピー数: 2 / 光学異性体: LEVO EC番号: 異性化酵素; 分子内転位酵素; ムターゼ; その他の基を移すもの |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 57.779211 KDa |
| 配列 | 文字列: MADAEVIILP KKHKKKKERK SLPEEDVAEI QHAEEFLIKP ESKVAKLDTS QWPLLLKNFD KLNVRTTHYT PLACGSNPLK REIGDYIRT GFINLDKPSN PSSHEVVAWI RRILRVEKTG HSGTLDPKVT GCLIVCIERA TRLVKSQQSA GKEYVGIVRL H NAIEGGTQ ...文字列: MADAEVIILP KKHKKKKERK SLPEEDVAEI QHAEEFLIKP ESKVAKLDTS QWPLLLKNFD KLNVRTTHYT PLACGSNPLK REIGDYIRT GFINLDKPSN PSSHEVVAWI RRILRVEKTG HSGTLDPKVT GCLIVCIERA TRLVKSQQSA GKEYVGIVRL H NAIEGGTQ LSRALETLTG ALFQRPPLIA AVKRQLRVRT IYESKMIEYD PERRLGIFWV SCEAGTYIRT LCVHLGLLLG VG GQMQELR RVRSGVMSEK DHMVTMHDVL DAQWLYDNHK DESYLRRVVY PLEKLLTSHK RLVMKDSAVN AICYGAKIML PGV LRYEDG IEVNQEIVVI TTKGEAICMA IALMTTAVIS TCDHGIVAKI KRVIMERDTY PRKWGLGPKA SQKKLMIKQG LLDK HGKPT DSTPATWKQE YVDYSESAKK EVVAEVVKAP QVVAEAAKTA KRKRESESES DETPPAAPQL IKKEKKKSKK DKKAK AGLE SGAEPGDGDS DTTKKKKKKK KAKEVELVSE UniProtKB: H/ACA ribonucleoprotein complex subunit DKC1 |
-分子 #3: H/ACA ribonucleoprotein complex subunit 3
| 分子 | 名称: H/ACA ribonucleoprotein complex subunit 3 / タイプ: protein_or_peptide / ID: 3 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 7.719989 KDa |
| 配列 | 文字列: MFLQYYLNEQ GDRVYTLKKF DPMGQQTCSA HPARFSPDDK YSRHRITIKK RFKVLMTQQP RPVL UniProtKB: H/ACA ribonucleoprotein complex subunit 3 |
-分子 #5: H/ACA ribonucleoprotein complex subunit 1
| 分子 | 名称: H/ACA ribonucleoprotein complex subunit 1 / タイプ: protein_or_peptide / ID: 5 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 22.387963 KDa |
| 配列 | 文字列: MSFRGGGRGG FNRGGGGGGF NRGGSSNHFR GGGGGGGGGN FRGGGRGGFG RGGGRGGFNK GQDQGPPERV VLLGEFLHPC EDDIVCKCT TDENKVPYFN APVYLENKEQ IGKVDEIFGQ LRDFYFSVKL SENMKASSFK KLQKFYIDPY KLLPLQRFLP R PPGEKGPP ...文字列: MSFRGGGRGG FNRGGGGGGF NRGGSSNHFR GGGGGGGGGN FRGGGRGGFG RGGGRGGFNK GQDQGPPERV VLLGEFLHPC EDDIVCKCT TDENKVPYFN APVYLENKEQ IGKVDEIFGQ LRDFYFSVKL SENMKASSFK KLQKFYIDPY KLLPLQRFLP R PPGEKGPP RGGGRGGRGG GRGGGGRGGG RGGGFRGGRG GGGGGFRGGR GGGFRGRGH UniProtKB: H/ACA ribonucleoprotein complex subunit 1 |
-分子 #6: H/ACA ribonucleoprotein complex subunit 2
| 分子 | 名称: H/ACA ribonucleoprotein complex subunit 2 / タイプ: protein_or_peptide / ID: 6 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 17.22607 KDa |
| 配列 | 文字列: MTKIKADPDG PEAQAEACSG ERTYQELLVN QNPIAQPLAS RRLTRKLYKC IKKAVKQKQI RRGVKEVQKF VNKGEKGIMV LAGDTLPIE VYCHLPVMCE DRNLPYVYIP SKTDLGAAAG SKRPTCVIMV KPHEEYQEAY DECLEEVQSL PLPL UniProtKB: H/ACA ribonucleoprotein complex subunit 2 |
-分子 #4: RNA (92-MER)
| 分子 | 名称: RNA (92-MER) / タイプ: rna / ID: 4 / コピー数: 1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Kidney Homo sapiens (ヒト) / 器官: Kidney |
| 分子量 | 理論値: 145.477797 KDa |
| 配列 | 文字列: GGGUUGCGGA GGGUGGGCCU GGGAGGGGUG GUGGCCAUUU UUUGUCUAAC CCUAACUGAG AAGGGCGUAG GCGCCGUGCU UUUGCUCCC CGCGCGCUGU UUUUCUCGCU GACUUUCAGC GGGCGGAAAA GCCUCGGCCU GCCGCCUUCC ACCGUUCAUU C UAGAGCAA ...文字列: GGGUUGCGGA GGGUGGGCCU GGGAGGGGUG GUGGCCAUUU UUUGUCUAAC CCUAACUGAG AAGGGCGUAG GCGCCGUGCU UUUGCUCCC CGCGCGCUGU UUUUCUCGCU GACUUUCAGC GGGCGGAAAA GCCUCGGCCU GCCGCCUUCC ACCGUUCAUU C UAGAGCAA ACAAAAAAUG UCAGCUGCUG GCCCGUUCGC CCCUCCCGGG GACCUGCGGC GGGUCGCCUG CCCAGCCCCC GA ACCCCGC CUGGAGGCCG CGGUCGGCCC GGGGCUUCUC CGGAGGCACC CACUGCCACC GCGAAGAGUU GGGCUCUGUC AGC CGCGGG UCUCUCGGGG GCGAGGGCGA GGUUCAGGCC UUUCAGGCCG CAGGAAGAGG AACGGAGCGA GUCCCCGCGC GCGG CGCGA UUCCCUGAGC UGUGGGACGU GCACCCAGGA CUCGGCUCAC ACAUGC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 構成要素:
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: C-flat / 材質: COPPER / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 5 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 12 sec. / 前処理 - 雰囲気: AIR | |||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: Blot for 4-5 seconds before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 78.0 K |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 2 / 実像数: 43639 / 平均露光時間: 1.0 sec. / 平均電子線量: 47.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 81000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: RECIPROCAL / プロトコル: AB INITIO MODEL / 温度因子: 104 |
|---|---|
| 得られたモデル |  PDB-7bgb: |
 ムービー
ムービー コントローラー
コントローラー


























 Z
Z Y
Y X
X