+検索条件
-Structure paper
| タイトル | Structures of ALG3/9/12 reveal the assembly logic of the N-glycan oligomannose core. |
|---|---|
| ジャーナル・号・ページ | Nat Chem Biol, Year 2026 |
| 掲載日 | 2026年3月10日 |
 著者 著者 | J Andrew N Alexander / Shu-Yu Chen / Somnath Mukherjee / Mario de Capitani / Rossitza N Irobalieva / Lorenzo Rossi / Parth Agrawal / Julia Kowal / Matheus A Meirelles / Markus Aebi / Jean-Louis Reymond / Anthony A Kossiakoff / Sereina Riniker / Kaspar P Locher /   |
| PubMed 要旨 | Asparagine-linked glycans are essential for the maturation and function of most eukaryotic secretory proteins. The biosynthesis and transfer of dolichylpyrophosphate-anchored GlcNAcManGlc glycan is a ...Asparagine-linked glycans are essential for the maturation and function of most eukaryotic secretory proteins. The biosynthesis and transfer of dolichylpyrophosphate-anchored GlcNAcManGlc glycan is a highly conserved process occurring in the endoplasmic reticulum (ER) membrane and involving over a dozen membrane proteins whose dysfunction is linked to congenital disorders of glycosylation (CDGs). Three membrane-integral mannosyltransferases, ALG3, ALG9 and ALG12, mediate four consecutive mannosylation reactions that convert GlcNAcMan to GlcNAcMan. Here, using chemoenzymatically synthesized lipid-linked glycan donor and acceptor analogs, we recapitulated this biosynthetic pathway in vitro. High-resolution cryo-electron microscopy structures of pseudo-Michaelis complexes of each step revealed how the branched glycan is accurately synthesized and unwanted side products are averted. Molecular dynamics simulations and mutagenesis studies uncovered a subtle but precise mechanism selecting the dolichylphosphomannose donor substrate over dolichylphosphoglucose, which is also present in the ER membrane. Our results also provide mechanistic explanations for enzyme dysfunction in CDGs and offer opportunities for N-glycan engineering. |
 リンク リンク |  Nat Chem Biol / Nat Chem Biol /  PubMed:41807832 PubMed:41807832 |
| 手法 | EM (単粒子) |
| 解像度 | 2.42 - 3.08 Å |
| 構造データ | EMDB-54629, PDB-9s6r: EMDB-54630, PDB-9s6s: EMDB-54631, PDB-9s6t: EMDB-54632, PDB-9s6u: |
| 化合物 |  PDB-1jma:  ChemComp-Y01:  ChemComp-IZY:  ChemComp-HOH: 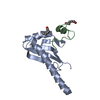 PDB-1jmt:  ChemComp-NAG:  PDB-1jmc:  ChemComp-AV0:  PDB-1jmb: |
| 由来 |
|
 キーワード キーワード | TRANSFERASE / Mannosyltransferase / ternary complex / N-linked glycosylation |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について













 homo sapiens (ヒト)
homo sapiens (ヒト)
