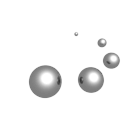2TPT
STRUCTURAL AND THEORETICAL STUDIES SUGGEST DOMAIN MOVEMENT PRODUCES AN ACTIVE CONFORMATION OF THYMIDINE PHOSPHORYLASE
2TPT の概要
| エントリーDOI | 10.2210/pdb2tpt/pdb |
| 分子名称 | THYMIDINE PHOSPHORYLASE, SULFATE ION (2 entities in total) |
| 機能のキーワード | thymidine phosphorylase, transferase, salvage pathway |
| 由来する生物種 | Escherichia coli |
| タンパク質・核酸の鎖数 | 1 |
| 化学式量合計 | 47337.05 |
| 構造登録者 | Pugmire, M.J.,Cook, W.J.,Jasanoff, A.,Walter, M.R.,Ealick, S.E. (登録日: 1997-11-24, 公開日: 1999-03-02, 最終更新日: 2024-02-21) |
| 主引用文献 | Pugmire, M.J.,Cook, W.J.,Jasanoff, A.,Walter, M.R.,Ealick, S.E. Structural and theoretical studies suggest domain movement produces an active conformation of thymidine phosphorylase. J.Mol.Biol., 281:285-299, 1998 Cited by PubMed Abstract: Two new crystal forms of Escherichia coli thymidine phosphorylase (EC 2.4.2.4) have been found; a monoclinic form (space group P21) and an orthorhombic form (space group I222). These structures have been solved and compared to the previously determined tetragonal form (space group P43212). This comparison provides evidence of domain movement of the alpha (residues 1 to 65, 163 to 193) and alpha/beta (residues 80 to 154, 197 to 440) domains, which is thought to be critical for enzymatic activity by closing the active site cleft. Three hinge regions apparently allow the alpha and alpha/beta-domains to move relative to each other. The monoclinic model is the most open of the three models while the tetragonal model is the most closed. Phosphate binding induces formation of a hydrogen bond between His119 and Gly208, which helps to order the 115 to 120 loop that is disordered prior to phosphate binding. The formation of this hydrogen bond also appears to play a key role in the domain movement. The alpha-domain moves as a rigid body, while the alpha/beta-domain has some non-rigid body movement that is associated with the formation of the His119-Gly208 hydrogen bond. The 8 A distance between the two substrates reported for the tetragonal form indicates that it is probably not in an active conformation. However, the structural data for these two new crystal forms suggest that closing the interdomain cleft around the substrates may generate a functional active site. Molecular modeling and dynamics simulation techniques have been used to generate a hypothetical closed conformation of the enzyme. Analysis of this model suggests several residues of possible catalytic importance. The model explains observed kinetic results and satisfies requirements for efficient enzyme catalysis, most notably through the exclusion of water from the enzyme's active site. PubMed: 9698549DOI: 10.1006/jmbi.1998.1941 主引用文献が同じPDBエントリー |
| 実験手法 | X-RAY DIFFRACTION (2.6 Å) |
構造検証レポート
検証レポート(詳細版) をダウンロード
をダウンロード