| 登録情報 | データベース: PDB / ID: 7cqp
|
|---|
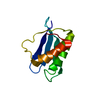
| タイトル | Complex of TRPC4 and Calmodulin_Nlobe |
|---|
 要素 要素 | - Calmodulin-1
- Peptide from Short transient receptor potential channel 4
|
|---|
 キーワード キーワード | SIGNALING PROTEIN / Calmodulin / TRP channel |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
CaMK IV-mediated phosphorylation of CREB / Cam-PDE 1 activation / CREB1 phosphorylation through the activation of CaMKII/CaMKK/CaMKIV cascasde / Glycogen breakdown (glycogenolysis) / Activation of RAC1 downstream of NMDARs / Reduction of cytosolic Ca++ levels / Sodium/Calcium exchangers / Activation of Ca-permeable Kainate Receptor / Synthesis of IP3 and IP4 in the cytosol / CLEC7A (Dectin-1) induces NFAT activation ...CaMK IV-mediated phosphorylation of CREB / Cam-PDE 1 activation / CREB1 phosphorylation through the activation of CaMKII/CaMKK/CaMKIV cascasde / Glycogen breakdown (glycogenolysis) / Activation of RAC1 downstream of NMDARs / Reduction of cytosolic Ca++ levels / Sodium/Calcium exchangers / Activation of Ca-permeable Kainate Receptor / Synthesis of IP3 and IP4 in the cytosol / CLEC7A (Dectin-1) induces NFAT activation / RHO GTPases activate PAKs / Calmodulin induced events / Inactivation, recovery and regulation of the phototransduction cascade / Tetrahydrobiopterin (BH4) synthesis, recycling, salvage and regulation / eNOS activation / Ion transport by P-type ATPases / Calcineurin activates NFAT / Unblocking of NMDA receptors, glutamate binding and activation / Protein methylation / RAF activation / VEGFR2 mediated vascular permeability / RAS processing / gamma-aminobutyric acid secretion / FCERI mediated Ca+2 mobilization / Ca2+ pathway / RHO GTPases activate IQGAPs / Extra-nuclear estrogen signaling / RAF/MAP kinase cascade / store-operated calcium channel activity / PKA activation / Smooth Muscle Contraction / Platelet degranulation / High laminar flow shear stress activates signaling by PIEZO1 and PECAM1:CDH5:KDR in endothelial cells / TRP channels / Stimuli-sensing channels / inositol 1,4,5 trisphosphate binding / Ion homeostasis / calcium ion import / organelle localization by membrane tethering / mitochondrion-endoplasmic reticulum membrane tethering / autophagosome membrane docking / presynaptic endocytosis / regulation of cardiac muscle cell action potential / cortical cytoskeleton / negative regulation of ryanodine-sensitive calcium-release channel activity / oligodendrocyte differentiation / calcineurin-mediated signaling / regulation of ryanodine-sensitive calcium-release channel activity / protein phosphatase activator activity / adenylate cyclase binding / catalytic complex / detection of calcium ion / regulation of cardiac muscle contraction / calcium channel inhibitor activity / cellular response to interferon-beta / regulation of release of sequestered calcium ion into cytosol by sarcoplasmic reticulum / titin binding / voltage-gated potassium channel complex / sperm midpiece / calcium channel complex / calyx of Held / adenylate cyclase activator activity / regulation of heart rate / protein serine/threonine kinase activator activity / sarcomere / regulation of cytokinesis / positive regulation of receptor signaling pathway via JAK-STAT / spindle microtubule / beta-catenin binding / caveola / cellular response to type II interferon / spindle pole / G2/M transition of mitotic cell cycle / cell-cell junction / myelin sheath / basolateral plasma membrane / transmembrane transporter binding / cadherin binding / membrane raft / centrosome / calcium ion binding / protein kinase binding / cell surface / protein-containing complex / nucleoplasm / plasma membrane / cytosol / cytoplasm類似検索 - 分子機能 Transient receptor potential channel, canonical 4 / Transient receptor ion channel domain / Transient receptor ion channel II / Transient receptor ion channel II / Transient receptor potential channel, canonical / EF-hand / : / Recoverin; domain 1 / Ankyrin repeat / EF-hand domain pair ...Transient receptor potential channel, canonical 4 / Transient receptor ion channel domain / Transient receptor ion channel II / Transient receptor ion channel II / Transient receptor potential channel, canonical / EF-hand / : / Recoverin; domain 1 / Ankyrin repeat / EF-hand domain pair / Ankyrin repeats (3 copies) / Ankyrin repeat profile. / Ankyrin repeat region circular profile. / ankyrin repeats / Ankyrin repeat / EF-hand, calcium binding motif / Ankyrin repeat-containing domain superfamily / EF-Hand 1, calcium-binding site / EF-hand calcium-binding domain. / EF-hand calcium-binding domain profile. / EF-hand domain / Ion transport domain / Ion transport protein / EF-hand domain pair / Orthogonal Bundle / Mainly Alpha類似検索 - ドメイン・相同性 Calmodulin-1 / Short transient receptor potential channel 4類似検索 - 構成要素 |
|---|
| 生物種 |   Mus musculus (ハツカネズミ) Mus musculus (ハツカネズミ) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.9 Å 分子置換 / 解像度: 1.9 Å |
|---|
 データ登録者 データ登録者 | Shen, Z.S. |
|---|
| 資金援助 |  中国, 2件 中国, 2件 | 組織 | 認可番号 | 国 |
|---|
| National Natural Science Foundation of China (NSFC) | 31670765 |  中国 中国 | | National Natural Science Foundation of China (NSFC) | 31870746 |  中国 中国 |
|
|---|
 引用 引用 |  ジャーナル: Structure / 年: 2021 ジャーナル: Structure / 年: 2021
タイトル: Calmodulin binds to Drosophila TRP with an unexpected mode.
著者: Chen, W. / Shen, Z. / Asteriti, S. / Chen, Z. / Ye, F. / Sun, Z. / Wan, J. / Montell, C. / Hardie, R.C. / Liu, W. / Zhang, M. |
|---|
| 履歴 | | 登録 | 2020年8月11日 | 登録サイト: PDBJ / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2021年6月23日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2023年11月29日 | Group: Data collection / Database references / Refinement description
カテゴリ: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_initial_refinement_model
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報
 X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 1.9 Å
分子置換 / 解像度: 1.9 Å  データ登録者
データ登録者 中国, 2件
中国, 2件  引用
引用 ジャーナル: Structure / 年: 2021
ジャーナル: Structure / 年: 2021 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 7cqp.cif.gz
7cqp.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb7cqp.ent.gz
pdb7cqp.ent.gz PDB形式
PDB形式 7cqp.json.gz
7cqp.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 7cqp_validation.pdf.gz
7cqp_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 7cqp_full_validation.pdf.gz
7cqp_full_validation.pdf.gz 7cqp_validation.xml.gz
7cqp_validation.xml.gz 7cqp_validation.cif.gz
7cqp_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/cq/7cqp
https://data.pdbj.org/pub/pdb/validation_reports/cq/7cqp ftp://data.pdbj.org/pub/pdb/validation_reports/cq/7cqp
ftp://data.pdbj.org/pub/pdb/validation_reports/cq/7cqp リンク
リンク 集合体
集合体
 要素
要素


 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  SSRF
SSRF  / ビームライン: BL19U1 / 波長: 0.9789 Å
/ ビームライン: BL19U1 / 波長: 0.9789 Å 分子置換
分子置換 解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj















