+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4986 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Influenza A virus (A/NT/60/1968) polymerase Heterotrimer bound to 3'5' vRNA promoter and capped RNA primer | ||||||||||||
 マップデータ マップデータ | None | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード |  Influenza A (A型インフルエンザウイルス) / Influenza A (A型インフルエンザウイルス) /  RNA polymerase (RNAポリメラーゼ) / Influenza polymerase / Influenza dimer / RNA polymerase (RNAポリメラーゼ) / Influenza polymerase / Influenza dimer /  RDRP (RNA依存性RNAポリメラーゼ) / RDRP (RNA依存性RNAポリメラーゼ) /  RNA BINDING PROTEIN (RNA結合タンパク質) RNA BINDING PROTEIN (RNA結合タンパク質) | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報symbiont-mediated suppression of host mRNA transcription via inhibition of RNA polymerase II activity /  キャップスナッチング / 7-methylguanosine mRNA capping / viral transcription / host cell mitochondrion / symbiont-mediated suppression of host cytoplasmic pattern recognition receptor signaling pathway via inhibition of MAVS activity / キャップスナッチング / 7-methylguanosine mRNA capping / viral transcription / host cell mitochondrion / symbiont-mediated suppression of host cytoplasmic pattern recognition receptor signaling pathway via inhibition of MAVS activity /  virion component / virion component /  endonuclease activity / host cell cytoplasm / endonuclease activity / host cell cytoplasm /  加水分解酵素; エステル加水分解酵素 ...symbiont-mediated suppression of host mRNA transcription via inhibition of RNA polymerase II activity / 加水分解酵素; エステル加水分解酵素 ...symbiont-mediated suppression of host mRNA transcription via inhibition of RNA polymerase II activity /  キャップスナッチング / 7-methylguanosine mRNA capping / viral transcription / host cell mitochondrion / symbiont-mediated suppression of host cytoplasmic pattern recognition receptor signaling pathway via inhibition of MAVS activity / キャップスナッチング / 7-methylguanosine mRNA capping / viral transcription / host cell mitochondrion / symbiont-mediated suppression of host cytoplasmic pattern recognition receptor signaling pathway via inhibition of MAVS activity /  virion component / virion component /  endonuclease activity / host cell cytoplasm / endonuclease activity / host cell cytoplasm /  加水分解酵素; エステル加水分解酵素 / 加水分解酵素; エステル加水分解酵素 /  RNA依存性RNAポリメラーゼ / viral RNA genome replication / RNA依存性RNAポリメラーゼ / viral RNA genome replication /  RNA-dependent RNA polymerase activity / RNA-dependent RNA polymerase activity /  nucleotide binding / DNA-templated transcription / host cell nucleus / nucleotide binding / DNA-templated transcription / host cell nucleus /  RNA binding / RNA binding /  metal ion binding metal ion binding類似検索 - 分子機能 | ||||||||||||
| 生物種 |   Influenza A virus (A/nt/60/1968(H3N2)) (A型インフルエンザウイルス) / Influenza A virus (A/nt/60/1968(H3N2)) (A型インフルエンザウイルス) /   Spodoptera frugiperda (ツマジロクサヨトウ) / Spodoptera frugiperda (ツマジロクサヨトウ) /   Influenza A virus (strain A/Northern Territory/60/1968 H3N2) (A型インフルエンザウイルス) Influenza A virus (strain A/Northern Territory/60/1968 H3N2) (A型インフルエンザウイルス) | ||||||||||||
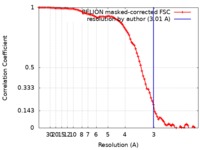
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.01 Å クライオ電子顕微鏡法 / 解像度: 3.01 Å | ||||||||||||
 データ登録者 データ登録者 | Carrique L / Keown JR | ||||||||||||
| 資金援助 |  英国, 3件 英国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2019 ジャーナル: Nature / 年: 2019タイトル: Structures of influenza A virus RNA polymerase offer insight into viral genome replication. 著者: Haitian Fan / Alexander P Walker / Loïc Carrique / Jeremy R Keown / Itziar Serna Martin / Dimple Karia / Jane Sharps / Narin Hengrung / Els Pardon / Jan Steyaert / Jonathan M Grimes / Ervin Fodor /    要旨: Influenza A viruses are responsible for seasonal epidemics, and pandemics can arise from the transmission of novel zoonotic influenza A viruses to humans. Influenza A viruses contain a segmented ...Influenza A viruses are responsible for seasonal epidemics, and pandemics can arise from the transmission of novel zoonotic influenza A viruses to humans. Influenza A viruses contain a segmented negative-sense RNA genome, which is transcribed and replicated by the viral-RNA-dependent RNA polymerase (FluPol) composed of PB1, PB2 and PA subunits. Although the high-resolution crystal structure of FluPol of bat influenza A virus has previously been reported, there are no complete structures available for human and avian FluPol. Furthermore, the molecular mechanisms of genomic viral RNA (vRNA) replication-which proceeds through a complementary RNA (cRNA) replicative intermediate, and requires oligomerization of the polymerase-remain largely unknown. Here, using crystallography and cryo-electron microscopy, we determine the structures of FluPol from human influenza A/NT/60/1968 (H3N2) and avian influenza A/duck/Fujian/01/2002 (H5N1) viruses at a resolution of 3.0-4.3 Å, in the presence or absence of a cRNA or vRNA template. In solution, FluPol forms dimers of heterotrimers through the C-terminal domain of the PA subunit, the thumb subdomain of PB1 and the N1 subdomain of PB2. The cryo-electron microscopy structure of monomeric FluPol bound to the cRNA template reveals a binding site for the 3' cRNA at the dimer interface. We use a combination of cell-based and in vitro assays to show that the interface of the FluPol dimer is required for vRNA synthesis during replication of the viral genome. We also show that a nanobody (a single-domain antibody) that interferes with FluPol dimerization inhibits the synthesis of vRNA and, consequently, inhibits virus replication in infected cells. Our study provides high-resolution structures of medically relevant FluPol, as well as insights into the replication mechanisms of the viral RNA genome. In addition, our work identifies sites in FluPol that could be targeted in the development of antiviral drugs. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4986.map.gz emd_4986.map.gz | 36.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4986-v30.xml emd-4986-v30.xml emd-4986.xml emd-4986.xml | 24.9 KB 24.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_4986_fsc.xml emd_4986_fsc.xml | 8.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4986.png emd_4986.png | 195.4 KB | ||
| Filedesc metadata |  emd-4986.cif.gz emd-4986.cif.gz | 8.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4986 http://ftp.pdbj.org/pub/emdb/structures/EMD-4986 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4986 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4986 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6rr7MC  4660C  4661C  4663C  4664C  4666C  6qnwC  6qpfC  6qpgC  6qwlC  6qx3C  6qx8C  6qxeC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4986.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4986.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | None | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.085 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Influenza A virus (A/NT/60/1968) polymerase Heterotrimer bound to...
+超分子 #1: Influenza A virus (A/NT/60/1968) polymerase Heterotrimer bound to...
+超分子 #2: polymerase Heterotrimer
+超分子 #3: Capped messenger RNA
+超分子 #4: Influenza A 5' and 3' viral RNA promoter
+分子 #1: Polymerase acidic protein
+分子 #2: RNA-directed RNA polymerase catalytic subunit
+分子 #3: Polymerase basic protein 2
+分子 #4: RNA (5'-D(*(M7G))-R(P*AP*AP*UP*CP*U)-3')
+分子 #5: RNA (5'-R(P*GP*CP*CP*UP*GP*CP*UP*UP*UP*UP*G)-3')
+分子 #6: RNA (5'-R(P*AP*GP*UP*AP*GP*AP*AP*AP*CP*AP*AP*GP*GP*C)-3')
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.35 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: Sample was purified in 20 mM HEPES, pH 7.5, 150 mM NaCl with Tween 20 added to a final concentration 0f 0.005% prior to plunging grids. | |||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: GOLD / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 120 sec. | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 298 K / 装置: FEI VITROBOT MARK IV / 詳細: blot for 3.5 sec before plunging. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 0.7000000000000001 µm 最小 デフォーカス(補正後): 0.5 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD  Bright-field microscopy / Cs: 2.7 mm / 倍率(公称値): 130000 Bright-field microscopy / Cs: 2.7 mm / 倍率(公称値): 130000 |
| 特殊光学系 | 位相板: VOLTA PHASE PLATE |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 6203 / 平均露光時間: 2.0 sec. / 平均電子線量: 36.6 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー