+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-30810 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structural basis for ligand binding modes of CTP synthase | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Interconversion of nucleotide di- and triphosphates / larval lymph gland hemopoiesis / CTP synthase (glutamine hydrolysing) / CTP synthase activity / cytoophidium / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / CTP biosynthetic process / glutamine metabolic process / ATP binding ...Interconversion of nucleotide di- and triphosphates / larval lymph gland hemopoiesis / CTP synthase (glutamine hydrolysing) / CTP synthase activity / cytoophidium / 'de novo' CTP biosynthetic process / pyrimidine nucleobase biosynthetic process / CTP biosynthetic process / glutamine metabolic process / ATP binding / identical protein binding / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
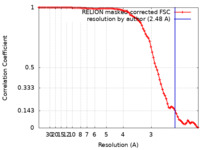
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.48 Å | |||||||||
 データ登録者 データ登録者 | Liu JL / Zhou X / Guo CJ / Chang CC | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2021 ジャーナル: Proc Natl Acad Sci U S A / 年: 2021タイトル: Structural basis for ligand binding modes of CTP synthase. 著者: Xian Zhou / Chen-Jun Guo / Chia-Chun Chang / Jiale Zhong / Huan-Huan Hu / Guang-Ming Lu / Ji-Long Liu /   要旨: Cytidine triphosphate synthase (CTPS), which comprises an ammonia ligase domain and a glutamine amidotransferase domain, catalyzes the final step of de novo CTP biosynthesis. The activity of CTPS is ...Cytidine triphosphate synthase (CTPS), which comprises an ammonia ligase domain and a glutamine amidotransferase domain, catalyzes the final step of de novo CTP biosynthesis. The activity of CTPS is regulated by the binding of four nucleotides and glutamine. While glutamine serves as an ammonia donor for the ATP-dependent conversion of UTP to CTP, the fourth nucleotide GTP acts as an allosteric activator. Models have been proposed to explain the mechanisms of action at the active site of the ammonia ligase domain and the conformational changes derived by GTP binding. However, actual GTP/ATP/UTP binding modes and relevant conformational changes have not been revealed fully. Here, we report the discovery of binding modes of four nucleotides and a glutamine analog 6-diazo-5-oxo-L-norleucine in CTPS by cryo-electron microscopy with near-atomic resolution. Interactions between GTP and surrounding residues indicate that GTP acts to coordinate reactions at both domains by directly blocking ammonia leakage and stabilizing the ammonia tunnel. Additionally, we observe the ATP-dependent UTP phosphorylation intermediate and determine interacting residues at the ammonia ligase. A noncanonical CTP binding at the ATP binding site suggests another layer of feedback inhibition. Our findings not only delineate the structure of CTPS in the presence of all substrates but also complete our understanding of the underlying mechanisms of the allosteric regulation and CTP synthesis. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_30810.map.gz emd_30810.map.gz | 37.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-30810-v30.xml emd-30810-v30.xml emd-30810.xml emd-30810.xml | 16.2 KB 16.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_30810_fsc.xml emd_30810_fsc.xml | 8.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_30810.png emd_30810.png | 65.9 KB | ||
| マスクデータ |  emd_30810_msk_1.map emd_30810_msk_1.map | 59.6 MB |  マスクマップ マスクマップ | |
| その他 |  emd_30810_half_map_1.map.gz emd_30810_half_map_1.map.gz emd_30810_half_map_2.map.gz emd_30810_half_map_2.map.gz | 44.9 MB 44.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-30810 http://ftp.pdbj.org/pub/emdb/structures/EMD-30810 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30810 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-30810 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_30810_validation.pdf.gz emd_30810_validation.pdf.gz | 664.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_30810_full_validation.pdf.gz emd_30810_full_validation.pdf.gz | 664.3 KB | 表示 | |
| XML形式データ |  emd_30810_validation.xml.gz emd_30810_validation.xml.gz | 14.3 KB | 表示 | |
| CIF形式データ |  emd_30810_validation.cif.gz emd_30810_validation.cif.gz | 20.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30810 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30810 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30810 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-30810 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_30810.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_30810.map.gz / 形式: CCP4 / 大きさ: 59.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_30810_msk_1.map emd_30810_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_30810_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_30810_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Drosophila substrate-bound CTP synthase
| 全体 | 名称: Drosophila substrate-bound CTP synthase |
|---|---|
| 要素 |
|
-超分子 #1: Drosophila substrate-bound CTP synthase
| 超分子 | 名称: Drosophila substrate-bound CTP synthase / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #1: CTP synthase
| 分子 | 名称: CTP synthase / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO / EC番号: CTP synthase (glutamine hydrolysing) |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 69.539453 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKYILVTGGV ISGVGKGVIA SSFGTLLKSC GLDVTSIKID PYINIDAGTF SPYEHGEVYV LDDGAEVDLD LGNYERFLDV TLHRDNNIT TGKIYKLVIE KERTGEYLGK TVQVVPHITD AIQEWVERVA QTPVQGSSKP QVCIVELGGT IGDIEGMPFV E AFRQFQFR ...文字列: MKYILVTGGV ISGVGKGVIA SSFGTLLKSC GLDVTSIKID PYINIDAGTF SPYEHGEVYV LDDGAEVDLD LGNYERFLDV TLHRDNNIT TGKIYKLVIE KERTGEYLGK TVQVVPHITD AIQEWVERVA QTPVQGSSKP QVCIVELGGT IGDIEGMPFV E AFRQFQFR VKRENFCLAH VSLVPLPKAT GEPKTKPTQS SVRELRGCGL SPDLIVCRSE KPIGLEVKEK ISNFCHVGPD QV ICIHDLN SIYHVPLLME QNGVIEYLNE RLQLNIDMSK RTKCLQQWRD LARRTETVRR EVCIAVVGKY TKFTDSYASV VKA LQHAAL AVNRKLELVF IESCLLEEET LHSEPSKYHK EWQKLCDSHG ILVPGGFGSR GMEGKIRACQ WARENQKPLL GICL GLQAA VIEFARNKLG LKDANTTEID PNTANALVID MPEHHTGQLG GTMRLGKRIT VFSDGPSVIR QLYGNPKSVQ ERHRH RYEV NPKYVHLLEE QGMRFVGTDV DKTRMEIIEL SGHPYFVATQ YHPEYLSRPL KPSPPFLGLI LASVDRLNQY IQRGCR LSP RQLSDASSDE EDSVVGLAGA TKSLSSLKIP ITPTNGISKS CNGSISTSDS EGACGGVDPT NGHK |
-分子 #2: GUANOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: GUANOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 4 / 式: GTP |
|---|---|
| 分子量 | 理論値: 523.18 Da |
| Chemical component information |  ChemComp-GTP: |
-分子 #3: 6-DIAZENYL-5-OXO-L-NORLEUCINE
| 分子 | 名称: 6-DIAZENYL-5-OXO-L-NORLEUCINE / タイプ: ligand / ID: 3 / コピー数: 4 / 式: DON |
|---|---|
| 分子量 | 理論値: 173.17 Da |
| Chemical component information |  ChemComp-DON: |
-分子 #4: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 4 / コピー数: 4 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-分子 #5: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 5 / コピー数: 12 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #6: [[(2~{R},3~{S},4~{R},5~{R})-3,4-bis(oxidanyl)-5-(2-oxidanyl-4-pho...
| 分子 | 名称: [[(2~{R},3~{S},4~{R},5~{R})-3,4-bis(oxidanyl)-5-(2-oxidanyl-4-phosphonooxy-pyrimidin-1-yl)oxolan-2-yl]methoxy-oxidanyl-phosphoryl] phosphono hydrogen phosphate タイプ: ligand / ID: 6 / コピー数: 4 / 式: 5ZL |
|---|---|
| 分子量 | 理論値: 565.129 Da |
| Chemical component information |  ChemComp-5ZL: |
-分子 #7: water
| 分子 | 名称: water / タイプ: ligand / ID: 7 / コピー数: 96 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 検出モード: SUPER-RESOLUTION / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: DARK FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー



















 Z
Z Y
Y X
X